Tumor Markers in HPB Cancers

The “ideal” tumor marker is economical, easy to estimate in easily accessible body fluids like blood or urine, has high sensitivity and specificity, can be used to screen for a cancer, has prognostic and predictive value at diagnosis, and is reliable during treatment and follow-up. It does not exist as of now. Commonly used tumor markers in gastrointestinal, liver, biliary tract, and pancreatic cancers are alpha fetoprotein (AFP), CA19.9, carcinoembryonic antigen (CEA), and chromogranin A (CgA).
Alpha Fetoprotein (AFP)
Alpha fetoprotein (AFP) is a glycoprotein that is produced in the yolk sac and the fetal liver. It is the most commonly used tumor marker for hepatocellular carcinoma (HCC). AFP may be raised in gonadal tumors, gastric cancer, and benign states like pregnancy, viral hepatitis, and cirrhosis caused by hepatitis C. The normal range is 10–20 ng/ml. Values above 400 ng/ml or a steady rise in serial estimation (even if lower than 400 ng/ml) is highly suggestive of HCC in a patient at risk of developing HCC. Persistent elevation of AFP is more significant than fluctuating levels. AFP levels are usually normal in the fibrolamellar variety of HCC. AFP is a heterogeneous molecule with respect to the carbohydrate moiety. Different AFP glycoforms can be separated and characterized by their affinity for lectins. Lectins are carbohydrate-binding proteins.

AFP level >500 ng/ml predicts high recurrence rate after transplantation, and such patients are not listed in the USA. Rise of AFP while on the wait list is also a poor prognostic factor. AFP >1000 ng/ml appears to be related to poor prognostic factors like microvascular invasion, portal vein invasion, bile duct invasion, and intrahepatic metastasis. In 2012 a French paper reported a model that added AFP to Milan criteria which improved prediction of recurrence and survival after liver transplantation for HCC.
CA 19-9
CA 19-9 is the abbreviation for carbohydrate antigen or cancer antigen 19-9. This tumor marker belongs to the family of mucinous markers. These have a transmembrane protein skeleton and an extracellular side that has glycosylated oligosaccharides. It is a sialylated Lewis blood group antigen. Mucus glands in the pancreas, biliary tree, salivary glands, stomach, colon, and endometrium physiologically secrete CA 19-9, and this is present in small quantities in serum. Higher levels are observed in inflammatory conditions of the pancreas and biliary tree like acute pancreatitis, biliary obstruction, and cholangitis. Overall mean sensitivity and specificity of serum CA 19-9 for diagnosis of pancreatic cancer are 81% and 90% according to one recent review. This study reported these results using 37 KU/l as cutoff of CA 19-9. Serum CA 19-9 seems to fare very poorly and is unsuitable as a screening modality for pancreatic cancer.
In one of the largest reviews of data, positive predictive value for diagnosis of pancreatic cancer was only 0.9%. Another study from Mumbai used CA 19-9 to predict operability in 49 patients with pancreatic cancer. When CA 19-9 was more than twice the normal (37 U/l), 88% were unresectable. Out of the 29 patients considered resectable after contrast-enhanced CT scan of abdomen, 5 patients were found unresectable at operation due to subcentimeter liver or peritoneal metastasis. All these five patients had CA 19-9 level more than three times the normal limit. These investigators suggest that diagnostic/ staging laparoscopy should be used to avoid a non-therapeutic laparotomy if CA 19-9 is more than thrice the normal limit.
Chromogranin A (CgA)
CgA is an acidic glycoprotein that is ubiquitously present in almost all endocrine and neuroendocrine cells of the human body. They are synthesized in these cells, stored along with other hormones /neurotransmitters in vesicles and released from the cells by exocytosis along with other hormones. The granin family consists of eight different substances of which chromogranin A is the best known and the one in clinical use for several decades now. CgA is thus a universal marker for neuroendocrine cell differentiation and activity. Testing its serum level is a marker of neuroendocrine secretory activity in the body. There are numerous limitations for the use of serum chromogranin A for diagnosis or follow-up of gastroenteropancreatic neuroendocrine tumors (GEP-NETs). However, it still remains the preferred tumor marker in these conditions, as it is widely available and less cumbersome to perform and retains a reasonable sensitivity and specificity provided the clinician applies all necessary recommended precautions in performance of the test and interpretation of the results.

Highest levels of CgA in GEP-NETs are obtained in midgut neuroendocrine tumors, previously termed as “carcinoid tumors.” In ileal carcinoids with liver metastasis, level as high as 200 times upper normal limit is reported. GEP-NETs in MEN-1 syndrome could result in chromogranin A values of about 150 times the upper normal limit. CgA levels in pancreatic NETs are about 60–80 times upper normal limit. CgA is elevated in 100% of gastrinomas and 70% of pancreatic NETs. In gastrinoma, very high levels are reported even in the absence of liver metastasis. CgA level of more than 5000 μg/l was found to be an independent prognostic factor for midgut NETs. Median survival was 33 and 57 months below and above the 5000 μg/l cutoff, respectively. This interpretation of CgA level cannot be generalized to all GEP-NETs. Typical exception of high level without any metastatic disease is gastrinoma as mentioned earlier. CgA level does not correlate with the degree of differentiation of GEP-NETs. Diagnostic accuracy of CgA was 73% in well-differentiated NETs and 50% in poorly differentiated NETs. This is probably related to loss of secretory function of poorly differentiated NETs, where this tumor marker is less reliable. CgA level has been reported to fall after all forms of therapy for GEP-NETs. This could be resection of the tumor, liver transplantation for metastatic disease, radionuclide therapy, or treatment with receptor blockade like everolimus.
Perioperative Fluid Management

In the setting of a normal ejection fraction, fluid is only administered when the expectation is that cardiac output will increase, and vasopressors are utilized if the aforementioned devices show fluid will not increase cardiac output. Excess fluid in certain general surgical cases can cause ileus and bowel edema, and in cardiac cases, it can cause hemodilution. Patients randomized to restricted and liberal fluid resuscitation strategies found a clear linear relationship between total fluids administered (and weight gain) and complications following colorectal surgery including pulmonary edema and tissue-healing complications. Further multiple studies exist demonstrating fewer complications with normovolemia than with liberal strategies of fluid resuscitation.
It must be understood that goal-directed therapy does, in no way, mean reduction in fluid administration. For some procedures, it may be necessary to administer more than anticipated fluid volumes (orthopedics), while for others, the opposite may be true (abdominal). Normovolemia is important to maintain perfusion without volume overload. Thus, the idea behind goaldirected therapy is to maintain zero fluid balance coupled with minimal weight gain or loss. Hypovolemia is associated with reduced circulating blood volume, decreased renal perfusion, altered coagulation, microcirculation compromise, and endothelial dysfunction, among other processes. Hypervolemia is associated with splanchnic edema, decreased pulmonary gas exchange secondary to pulmonary edema, impaired wound healing, anastomotic dehiscence, decreased mobility, altered coagulation, and endothelial dysfunction, amidst others processes.
Classroom: Perioperative Medicine
From a recent Cochrane review, there is no evidence that colloids are superior to crystalloid for resuscitation in patients. Therefore, crystalloid fluids should generally be the primary intravenous fluid during the perioperative course. In cardiac surgery, the utilization of 0.9% normal saline solution was associated with hyperchloremia and poor postoperative outcomes, including higher length of stay and increased mortality.118 Further, a more balanced crystalloid, such as Plasma-Lyte, was associated with improved outcomes in 22,851 surgical patients. In this study, there was a 2.05 odds ratio predictor of mortality with normal saline. Other complications such as acute kidney injury, gastrointestinal complications, major hemorrhage, and major infection were also increased in the group of
patients that were hyperchloremic after normal saline administration. Based on such evidence, it would seem prudent to proceed with a more balanced solution, such as PlasmaLyte, to reduce complications.
A especialização e a busca pela excelência

“Onde quer que a arte de curar é amada, também há um amor pela humanidade.” — Hipócrates
A especialização em órgãos e o volume de casos têm sido temas centrais nos últimos anos, revelando uma relação direta entre alto volume de procedimentos e melhores desfechos, conforme evidenciado pela literatura recente. Estudos mostram que a concentração de procedimentos de alto risco, como esofagectomias, pancreatectomias e ressecções hepáticas, em centros especializados pode reduzir significativamente a mortalidade pós-operatória anual. Embora procedimentos como tireoidectomias e ressecções do cólon mostrem um efeito semelhante, mas em menor escala, a redução da mortalidade pós-operatória em 5% pode ser tão eficaz quanto tratamentos adjuvantes tóxicos e deve ser uma prioridade na busca pela mais alta qualidade em cirurgia oncológica e digestiva. Além da redução da morbidade e mortalidade, há evidências de que a especialização pode levar a melhores resultados funcionais e financeiros. Às vezes, a atenção excessiva aos números anuais obscurece o fato de que hospitais menores, com equipes dedicadas, também podem alcançar bons resultados. É provável que não apenas o volume, mas também o treinamento e a especialização resultem em melhores desfechos. Definir um número absoluto de casos pode ser improdutivo e desviar a atenção de fatores essenciais, como reuniões multidisciplinares organizadas, infraestrutura adequada e disponibilidade de técnicas modernas.
O Foco na Otimização do Processo
O foco deve ser direcionado para a análise e otimização de todo o processo de diagnóstico e tratamento, já que este processo pode colocar o paciente em grave risco, especialmente durante o período hospitalar. A prevenção de erros tem recebido atenção significativa, levando ao surgimento do conceito de segurança do paciente. Desde a publicação do relatório To Err Is Human pelo Institute of Medicine, a abordagem para erros mudou drasticamente.
Em vez de focar exclusivamente no indivíduo, a abordagem sistêmica considera as condições em que as pessoas trabalham e tenta construir defesas para mitigar os efeitos dos erros. O modelo de queijo suíço ilustra bem essa abordagem: várias camadas de defesa, cada uma com suas falhas, são colocadas em torno de um procedimento. As falhas ativas e condições latentes criam buracos em cada camada. Em vez de apenas fechar os buracos na última camada de defesa, redesenhar o processo e fechar um buraco em uma camada anterior pode ser mais eficaz.
A análise de causa raiz é essencial para identificar pontos fracos no procedimento. Um exemplo é a colocação incorreta de uma colostomia após uma resseção abdominoperineal. Em vez de culpar o residente por não selecionar a posição correta durante a cirurgia ou marcar o ponto errado no dia anterior, uma solução mais eficaz seria o treinamento adequado do junior ou a marcação do ponto certo por um terapeuta de estomas durante a clínica ambulatorial.
A marcação do local correto no corpo tornou-se uma medida de segurança e o paciente deve ser instruído a exigir essa prática para sua própria segurança. É crucial eliminar a cultura de ‘culpa e vergonha’ e promover um ambiente mais aberto, onde erros e quase erros possam ser relatados. O clima de segurança em um departamento cirúrgico pode ser medido de forma validada e é um elemento essencial para uma cultura onde a segurança do paciente possa prosperar.
O Cuidado com os Detalhes e a Otimização de Resultados
A atenção meticulosa a cada detalhe durante o período pré-operatório e clínico pode reduzir eventos adversos. O que é chamado de “primeira vez em risco” deve ser considerado. Há também exemplos de ações para otimizar resultados que são mais específicas para o câncer. Por exemplo, o uso de técnicas que estimulam a cicatrização de feridas após uma resseção abdominoperineal, como a omentoplastia ou o retal abdominal flap, pode evitar atrasos no tratamento adjuvante para câncer retal.
A atenção cuidadosa à cicatrização de feridas em sarcoma pode evitar o adiamento da necessária radioterapia adjuvante. Omissão de uma tomografia computadorizada com contraste contendo iodo no diagnóstico de câncer de tireoide pode possibilitar um tratamento radioativo com iodo mais precoce, resultando em possíveis melhores resultados. A coleta de um número suficiente de linfonodos em câncer de cólon pode evitar discussões sobre a indicação de quimioterapia adjuvante.
A maioria dos exemplos de segurança do paciente no período clínico está relacionada ao uso ótimo de tratamento multimodal ou aos efeitos gerais da cirurgia. Às vezes, é necessário equilibrar o risco de aceitar um procedimento cirúrgico mais extenso, com uma morbidade mais alta, para alcançar um melhor resultado a longo prazo. O oposto também é possível, quando um bom resultado de curto prazo de uma excisão local em câncer retal deve ser equilibrado com uma maior taxa de recorrência local. A garantia de qualidade para todas as disciplinas participantes (diagnósticas e terapêuticas) é um elemento chave na configuração de ensaios clínicos prospectivos e randomizados.
“A prática é a maior professora, e o mais sábio cirurgião é aquele que aprende a valorizar o conhecimento não apenas pela sua acumulação, mas pela sua aplicação.” — William Osler
Recurrence after Repair of Incisional Hernia

The incidence of recurrence in incisional hernia prosthetic surgery is markedly lower than in direct plasties. Indeed after the autoplasties of the preprosthetic period, the recurrence rate ranged from 35% for ventral hernias. Chevrel and Flament, in 1990, reported on 1,033 patients who had undergone laparotomy. The recurrence rate at 10-year follow-up was 14–24% for patients treated without the use of prostheses but only 8.6% for those in whom a prosthesis was implanted. A similar incidence was reported by Chevrel in 1995: 18.3% recurrence without prostheses, 5.5% with prostheses. Likewise, Wantz, in 1991, noted a recurrence rate of 0–18.5% in prosthetic laparo-alloplasties.
At the European Hernia Society (EHS)-GREPA meeting in 1986, the recurrence rate without prostheses was reported to be between 7.2 and 17% whereas in patients who had been treated with a prosthesis the recurrence was between 1 and 5.8%. A case study published by Flament in 1999 showed a 5.6% recurrence rate for operations with prostheses placed behind the muscles and in front of the fascia, and a 3.6% of such figure consisted of a small-sized lateroprosthetic recurrence. These rates were in contrast to the 26.8% recurrence reported by other surgeons for operations without prostheses.
Studies of recurrence are, of course, influenced by the size of the initial defect and the length of follow-up. Nevertheless, it is beyond dispute that the use of prostheses is associated with a lower rate of recurrence independent of the nature of the incisional hernia. The factors that lead to relapse are recognisable in the original features of the ventral hernia, i.e. combined musculo-aponeurotic parietal involvement, septic complications in the first operation, the nature and appropriateness of treatment, the kind of prosthesis and its position. Also important is whether the surgery was an emergency case and the relation to occlusive phenomena, visceral damage
and whether these problems were addressed at the same time.
Obesity is also an important risk factor for recurrence. In addition to its association with a higher surgical complications rate, related to the high intraabdominal pressure, there are deficits in wound cicatrisation as well as respiratory and metabolic pathologies. In such patients, the laparoscopic approach is very useful to significantly reduce the onset of general and wall complications, and the data concerning recurrence are encouraging, ranging between 1 and 9% in the largest laparoscopic case studies. The important multicentric study of Heniford et al., in 2000, reported a recurrence rate of 3.4% after 23 months. In 2003, the same author, in a study with an average follow-up of 20 months (range 1–96) showed a recurrence rate of 4.7% for different, identifiable causes: intestinal iatrogenic injuries and mesh infection with its removal, insufficient fixation of the prosthesis and abdominal trauma in the first postoperative period.
The incidence of recurrence after laparoscopic treatment may also be related to general patient factors and to the onset of local complications, mistakes in opting for laparoscopic treatment and deficits in implanting and fixing the prosthesis. With respect to the latter, it is very important to allow a large overlap compared to the diameter of the defect. Long-term data analysis, with large case studies, is still needed to obtain detailed information about recurrence, and this is particularly true in the assessment of relatively new techniques.
Management of gallbladder cancer

Gallbladder cancer is uncommon disease, although it is not rare. Indeed, gallbladder cancer is the fifth most common gastrointestinal cancer and the most common biliary tract cancer in the United States. The incidence is 1.2 per 100,000 persons per year. It has historically been considered as an incu-rable malignancy with a dismal prognosis due to its propensity for early in-vasion to liver and dissemination to lymph nodes and peritoneal surfaces. Patients with gallbladder cancer usually present in one of three ways: (1) advanced unresectable cancer; (2) detection of suspicious lesion preoperatively and resectable after staging work-up; (3) incidental finding of cancer during or after cholecystectomy for benign disease.
SURGICAL MANAGEMENT
Although, many studies have suggested improved survival in patients with early gallbladder cancer with radical surgery including en bloc resection of gallbladder fossa and regional lymphadenectomy, its role for those with advanced gallbladder cancer remains controversial. First, patients with more advanced disease often require more extensive resections than early stage tumors, and operative morbidity and mortality rates are higher. Second, the long-term outcomes after resection, in general, tend to be poorer; long-term survival after radical surgery has been reported only for patients with limited local and lymph node spread. Therefore, the indication of radical surgery should be limited to well-selected patients based on thorough preoperative and intra-operative staging and the extent of surgery should be determined based on the area of tumor involvement.
Surgical resection is warranted only for those who with locoregional disease without distant spread. Because of the limited sensitivity of current imaging modalities to detect metastatic lesions of gallbladder cancer, staging laparoscopy prior to proceeding to laparotomy is very useful to assess the
abdomen for evidence of discontinuous liver disease or peritoneal metastasis and to avoid unnecessary laparotomy. Weber et al. reported that 48% of patients with potentially resectable gallbladder cancer on preoperative imaging work-up were spared laparotomy by discovering unresectable disease by laparoscopy. Laparoscopic cholecystectomy should be avoided when a preoperative cancer is suspected because of the risk of violation of the plane between tumor and liver and the risk of port site seeding.
The goal of resection should always be complete extirpation with microscopic negative margins. Tumors beyond T2 are not cured by simple cholecystectomy and as with most of early gallbladder cancer, hepatic resection is always required. The extent of liver resection required depends upon whether involvement of major hepatic vessels, varies from segmental resection of segments IVb and V, at minimum to formal right hemihepatectomy or even right trisectionectomy. The right portal pedicle is at particular risk for advanced tumor located at the neck of gallbladder, and when such involvement is suspected, right hepatectomy is required. Bile duct resection and reconstruction is also required if tumor involved in bile duct. However, bile duct resection is associated with increased perioperative morbidity and it should be performed only if it is necessary to clear tumor; bile duct resection does not necessarily increase the lymph node yield.
Hepatic Surgery: Portal Vein Embolization

INTRODUCTION
Portal vein Embolizations (PVE) is commonly used in the patients requiring extensive liver resection but have insufficient Future Liver Remanescent (FLR) volume on preoperative testing. The procedure involves occluding portal venous flow to the side of the liver with the lesion thereby redirecting portal flow to the contralateral side, in an attempt to cause hypertrophy and increase the volume of the FLR prior to hepatectomy.
PVE was first described by Kinoshita and later reported by Makuuchi as a technique to facilitate hepatic resection of hilar cholangiocarcinoma. The technique is now widely used by surgeons all over the world to optimize FLR volume before major liver resections.
PHYSIOPATHOLOGY
PVE works because the extrahepatic factors that induce liver hypertrophy are carried primarily by the portal vein and not the hepatic artery. The increase in FLR size seen after PVE is due to both clonal expansion and cellular hypertrophy, and the extent of post-embolization liver growth is generally proportional to the degree of portal flow diversion. The mechanism of liver regeneration after PVE is a complex phenomenon and is not fully understood. Although the exact trigger of liver regeneration remains unknown, several studies have identified periportal inflammation in the embolized liver as an important predictor of liver regeneration.

THECNICAL ASPECTS
PVE is technically feasible in 99% of the patients with low risk of complications. Studies have shown the FLR to increase by a median of 40–62% after a median of 34–37 days after PVE, and 72.2–80% of the patients are able to undergo resection as planned. It is generally indicated for patients being considered for right or extended right hepatectomy in the setting of a relatively small FLR. It is rarely required before extended left hepatectomy or left trisectionectomy, since the right posterior section (segments 6 and 7) comprises about 30% of total liver volume.
PVE is usually performed through percutaneous transhepatic access to the portal venous system, but there is considerable variability in technique between centers. The access route can be ipsilateral (portal access at the same side being resected) with retrograde embolization or contralateral (portal access through FLR) with antegrade embolization. The type of approach selected depends on a number of factors including operator preference, anatomic variability, type of resection planned, extent of embolization, and type of embolic agent used. Many authors prefer ipsilateral approach especially for right-sided tumors as this technique allows easy catheterization of segment 4 branches when they must be embolized and also minimizes the theoretic risk of injuring the FLR vasculature or bile ducts through a contralateral approach and potentially making a patient ineligible for surgery.
However, majority of the studies on contralateral PVE show it to be a safe technique with low complication rate. Di Stefano et al. reported a large series of contralateral PVE in 188 patients and described 12 complications (6.4%) only 6 of which could be related to access route and none precluded liver resection. Site of portal vein access can also change depending on the choice of embolic material selected which can include glue, Gelfoam, n-butyl-cyanoacrylate (NBC), different types and sizes of beads, alcohol, and nitinol plus. All agents have similar efficacy and there are no official recommendations for a particular type of agent.
RESULTS
Proponents of PVE believe that there should be very little or no tumor progression during the 4–6 week wait period for regeneration after PVE. Rapid growth of the FLR can be expected within the first 3–4 weeks after PVE and can continue till 6–8 weeks. Results from multiple studies suggest that 8–30% hypertrophy over 2–6 weeks can be expected with slower rates in cirrhotic patients. Most studies comparing outcomes after major hepatectomy with and without preoperative PVE report superior outcomes with PVE. Farges et al. demonstrated significantly less risk of postoperative complications, duration of intensive care unit, and hospital stay in patients with cirrhosis who underwent right hepatectomy after PVE compared to those who did not have preoperative PVE. The authors also reported no benefit of PVE in patients with a normal liver and FLR >30%. Abulkhir et al. reported results from a meta-analysis of 1088 patients undergoing PVE and showed a markedly lower incidence of Post Hepatectomy Liver Failure (PHLF) and death compared to series reporting outcomes after major hepatectomy in patients who did not undergo PVE. All patients had FLR volume increase, and 85% went on to have liver resection after PVE with a PHLF incidence of 2.5% and a surgical mortality of 0.8%. Several studies looking at the effect of systemic neoadjuvant chemotherapy on the degree of hypertrophy after PVE show no significant impact on liver regeneration and growth.
VOLUMETRIC RESPONSE

The volumetric response to PVE is also a very important factor in understanding the regenerative capacity of a patient’s liver and when used together with FLR volume can help identify patients at risk of poor postsurgical outcome. Ribero et al. demonstrated that the risk of PHLF was significantly higher not only in patients with FLR ≤ 20% but also in patients with normal liver who demonstrated ≤5% of FLR hypertrophy after PVE. The authors concluded that the degree of hypertrophy >10% in patients with severe underlying liver disease and >5% in patients with normal liver predicts a low risk of PHLF and post-resection mortality. Many authors do not routinely offer resection to patients with borderline FLR who demonstrate ≤5% hypertrophy after PVE.
Predicting LIVER REMNANT Function
Careful analysis of outcome based on liver remnant volume stratified by underlying liver disease has led to recommendations regarding the safe limits of resection. The liver remnant to be left after resection is termed the future liver remnant (FLR). For patients with normal underlying liver, complications, extended hospital stay, admission to the intensive care unit, and hepatic insufficiency are rare when the standardized FLR is >20% of the TLV. For patients with tumor-related cholestasis or marked underlying liver disease, a 40% liver remnant is necessary to avoid cholestasis, fluid retention, and liver failure. Among patients who have been treated with preoperative systemic chemotherapy for more than 12 weeks, FLR >30% reduces the rate of postoperative liver insufficiency and subsequent mortality.
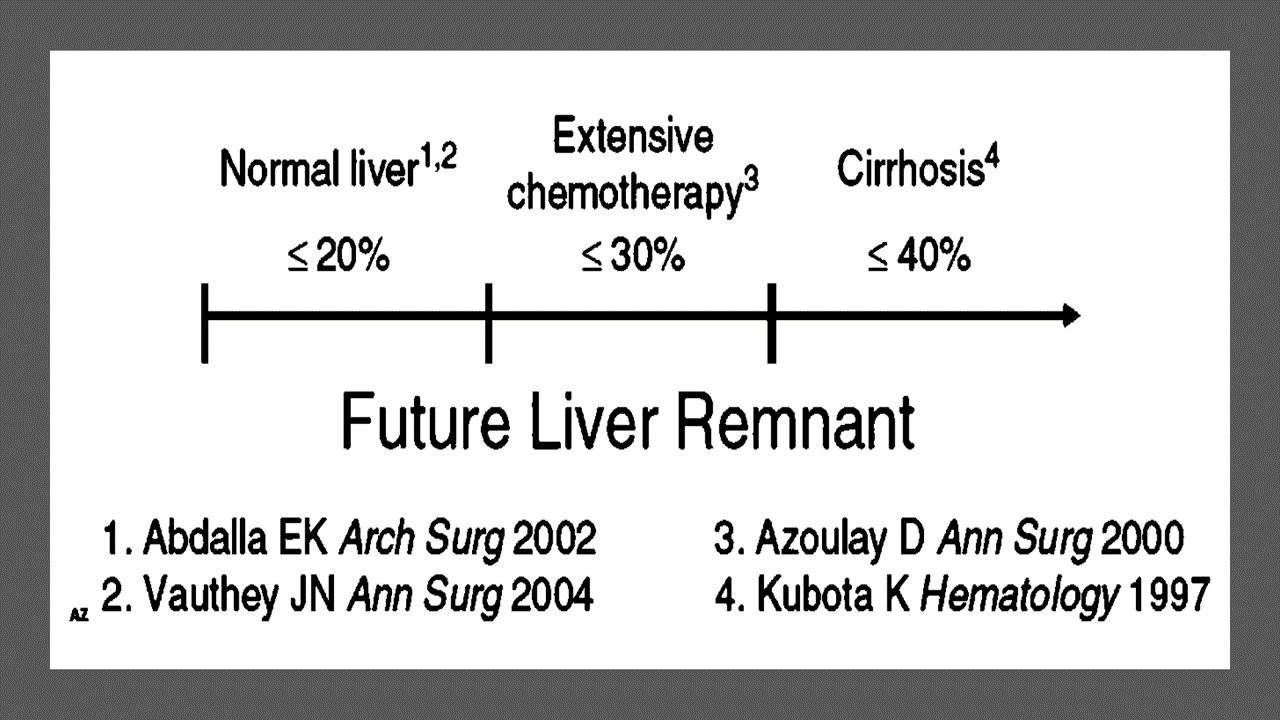
When the liver remnant is normal or has only mild disease, the volume of liver remnant can be measured directly and accurately with threedimensional computed tomography (CT) volumetry. However, inaccuracy may arise because the liver to be resected is often diseased, particularly in patients with cirrhosis or biliary obstruction. When multiple or large tumors occupy a large volume of the liver to be resected, subtracting tumor volumes from liver volume further decreases accuracy of CT volumetry. The calculated TLV, which has been derived from the association between body surface area (BSA) and liver size, provides a standard estimate of the TLV. The following formula is used:
TLV (cm3) = –794.41 + 1267.28 × BSA (square meters)
Thus, the standardized FLR (sFLR) volume calculation uses the measured FLR volume from CT volumetry as the numerator and the calculated TLV as the denominator: Standardized FLR (sFLR) = measured FLR volume/TLV Calculating the standardized TLV corrects the actual liver volume to the individual patient’s size and provides an individualized estimate of that patient’s postresection liver function. In the event of an inadequate FLR prior to major hepatectomy, preoperative liver preparation may include portal vein embolization (PVE).
Classroom: Principles of Hepatic Surgery
Modern Concepts of Pancreatic Surgery
 Operations on the gallbladder and bile ducts are among the surgical procedures most commonly performed by general surgeons. In most hospitals, cholecystectomy is the most frequently performed operation within the abdomen. Pancreatic surgery is less frequent , but because of the close relation between the biliary system and the pancreas, knowledge of pancreatic problems is equally essential to the surgeon. Acute and chronic pancreatitis and cancer of the pancreas are often encountered by surgeons, with apparently increasing frequency; their treatment remains difficult and perplexing. This review demonstrates the modern aspects of pancreatic surgery. Good study.
Operations on the gallbladder and bile ducts are among the surgical procedures most commonly performed by general surgeons. In most hospitals, cholecystectomy is the most frequently performed operation within the abdomen. Pancreatic surgery is less frequent , but because of the close relation between the biliary system and the pancreas, knowledge of pancreatic problems is equally essential to the surgeon. Acute and chronic pancreatitis and cancer of the pancreas are often encountered by surgeons, with apparently increasing frequency; their treatment remains difficult and perplexing. This review demonstrates the modern aspects of pancreatic surgery. Good study.
AULA: PRÍNCIPIOS MODERNOS DA CIRURGIA PANCREÁTICA
Postoperative Delirium

Postoperative delirium is recognized as the most common surgical complication in older adults,occurring in 5% to 50% of older patients after an operation. With more than one-third of all inpatient operations in the United States being performed on patients 65 years or older, it is imperative that clinicians caring for surgical patients understand optimal delirium care. Delirium is a serious complication for older adults because an episode of delirium can initiate a cascade of deleterious clinical events, including other major postoperative complications, prolonged hospitalization, loss of functional independence, reduced cognitive function, and death. The annual cost of delirium in the United States is estimated to be $150 billion. Delirium is particularly compelling as a quality improvement target, because it is preventable in up to 40% of patients; therefore, it is an ideal candidate for preventive interventions targeted to improve the outcomes of older adults in the perioperative setting. Delirium diagnosis and treatment are essential components of optimal surgical care of older adults, yet the topic of delirium is under-represented in surgical teaching.
Postoperative Delirium in Older Adults
A “PROFISSÃO” CIRÚRGICA
 “A arte de curar vem do coração e da mente mais do que das mãos.” – Hipócrates
“A arte de curar vem do coração e da mente mais do que das mãos.” – Hipócrates
Na complexa tapeçaria da sociedade moderna, as profissões desempenham papéis fundamentais na organização dos serviços necessários ao bem-estar coletivo. Definida pelo American College of Surgeons, uma profissão é um campo onde a maestria de um corpo complexo de conhecimento e habilidades é essencial. É uma vocação em que o conhecimento científico ou a prática de uma arte, fundamentada nesse conhecimento, é empregada em benefício dos outros. O compromisso com a competência, a integridade e a moralidade forma a base de um contrato social entre a profissão e a sociedade, que concede à profissão um monopólio sobre o uso de seu conhecimento, considerável autonomia na prática e o privilégio da auto-regulação. Em troca, a profissão deve prestar contas a quem serve e à sociedade como um todo.
Os Elementos Essenciais da Profissão
No cerne de toda profissão estão quatro elementos fundamentais:
- Monopólio do Conhecimento Especializado: Profissionais detêm o direito exclusivo de utilizar conhecimentos e habilidades especializados, o que lhes confere uma posição única na sociedade.
- Autonomia e Auto-Regulação: Em troca deste monopólio, profissionais desfrutam de uma relativa autonomia na prática e são responsáveis pela sua própria regulação.
- Serviço Altruísta: A profissão deve servir tanto indivíduos quanto a sociedade de forma altruísta, colocando o bem-estar do paciente acima de outros interesses.
- Responsabilidade pela Manutenção e Expansão do Conhecimento: Profissionais são responsáveis por atualizar e expandir continuamente seu conhecimento e habilidades.
O Que é Profissionalismo?
Profissionalismo descreve as qualidades cognitivas, morais e colegiais de um profissional. É o conjunto de razões pelas quais um pai se orgulha de dizer que seu filho é um médico e cirurgião. Profissionalismo é mais do que apenas conhecimento técnico; é uma combinação de ética, respeito e dedicação ao ofício e ao paciente.
Por Que Precisamos de um Código de Conduta Profissional?
A confiança é o alicerce da prática cirúrgica. O Código de Conduta Profissional esclarece a relação entre a profissão cirúrgica e a sociedade que serve, frequentemente referido como contrato social. Para os pacientes, o código cristaliza o compromisso da comunidade cirúrgica em relação aos indivíduos e suas comunidades. A confiança é construída, tijolo por tijolo.
O Código de Conduta Profissional
O Código de Conduta Profissional aplica os princípios gerais do profissionalismo à prática cirúrgica e serve como a fundação sobre a qual os privilégios profissionais e a confiança dos pacientes e do público são conquistados. Durante o cuidado pré-operatório, intraoperatório e pós-operatório, os cirurgiões têm a responsabilidade de:
- Advogar Eficazmente pelos interesses dos pacientes.
- Divulgar Opções Terapêuticas incluindo seus riscos e benefícios.
- Divulgar e Resolver Conflitos de Interesse que possam influenciar as decisões de cuidado.
- Ser Sensível e Respeitoso com os pacientes, compreendendo sua vulnerabilidade durante o período perioperatório.
- Divulgar Completamente Eventos Adversos e Erros Médicos.
- Reconhecer Necessidades Psicológicas, Sociais, Culturais e Espirituais dos pacientes.
- Incorporar Cuidados Especiais para Pacientes Terminais.
- Reconhecer e Apoiar as Necessidades das Famílias dos Pacientes.
- Respeitar o Conhecimento, Dignidade e Perspectiva de outros profissionais de saúde.
A Necessidade do Código de Profissionalismo para Cirurgiões
Procedimentos cirúrgicos são experiências extremas que impactam os pacientes fisiológica, psicológica e socialmente. Quando os pacientes se submetem a uma experiência cirúrgica, devem confiar que o cirurgião colocará seu bem-estar acima de todas as outras considerações. O código escrito ajuda a reforçar esses valores, garantindo que a confiança e o compromisso sejam mantidos.
Princípios Fundamentais do Código de Conduta Profissional
- Primazia do Bem-Estar do Paciente: Os interesses do paciente sempre devem vir em primeiro lugar. O altruísmo é central para esse conceito, e é o altruísmo do cirurgião que fomenta a confiança na relação médico-paciente.
- Autonomia do Paciente: Pacientes devem entender e tomar suas próprias decisões informadas sobre o tratamento. Os médicos devem ser honestos para que os pacientes façam escolhas educadas, garantindo que essas decisões estejam alinhadas com práticas éticas.
- Justiça Social: Como médicos, devemos advogar pelos pacientes individuais enquanto promovemos a saúde do sistema de saúde como um todo. Precisamos equilibrar as necessidades dos pacientes (autonomia) sem desviar recursos escassos que beneficiariam a sociedade (justiça social).
“Não há maior coisa a ser conquistada do que a confiança dos pacientes e da sociedade, pois ela é a base sobre a qual construímos nossas práticas e nossa profissão.” – William Osler
FERIDA PÓS-OPERATÓRIA

A avaliação e os cuidados de feridas pós-operatórias deve ser do domínio de todos os profissionais que atuam na clínica cirúrgica. O conhecimento a cerca dos processos relacionados a cicatrização tecidual é importante tanto nos cuidados como na prevenção de complicações, tais como: infecções e deiscência. Como tal, todos os profissionais médicos, sendo eles cirurgiões ou de outras especialidades, que participam do manejo clínico dos pacientes no período perioperatório devem apreciar a fisiologia da cicatrização de feridas e os princípios de tratamento de feridas pós-operatório. O objetivo deste artigo é atualizar os profissionais médicos de outras especialidades sobre os aspectos importantes do tratamento de feridas pós-operatório através de uma revisão da fisiologia da cicatrização de feridas, os métodos de limpeza e curativo, bem como um guia sobre complicações de feridas pós-operatórias mais prevalentes e como devem ser manejados nesta situação.
Esophagectomy: Anastomotic Complications (Leakage and Stricture)

Esophagectomy can be used to treat several esophageal diseases; it is most commonly used for treatment of esophageal cancer. Esophagectomy is a major procedure that may result in various complications. This article reviews only the important complications resulting from esophageal resection, which are anastomotic complications after esophageal reconstruction (leakage and stricture), delayed emptying or dumping syndrome, reflux, and chylothorax.
Causas de conversão da VIDEOCOLECISTECTOMIA

Atualmente, a colecistectomia laparoscópica é a abordagem preferida para o tratamento da litíase biliar, representando cerca de 90% dos procedimentos realizados, uma marca alcançada nos Estados Unidos em 1992. A popularidade dessa técnica se deve a suas vantagens evidentes: menos dor no pós-operatório, recuperação mais rápida, redução dos dias de trabalho perdidos e menor tempo de hospitalização. Apesar de ser considerada o padrão-ouro na cirurgia biliar, a colecistectomia laparoscópica não está isenta de desafios. Entre 2% e 15% dos casos podem exigir a conversão para cirurgia convencional. Os motivos mais comuns para essa conversão incluem dificuldades na identificação da anatomia, suspeita de lesão da árvore biliar e controle de sangramentos. Identificar os fatores que contribuem para uma maior taxa de conversão é essencial para a equipe cirúrgica. Isso não apenas permite uma avaliação mais precisa da complexidade do procedimento, mas também ajuda na preparação do paciente para possíveis riscos e na mobilização de cirurgiões mais experientes quando necessário. Em um cenário onde a precisão e a segurança são cruciais, a compreensão dos desafios e a preparação adequada podem fazer toda a diferença no resultado da cirurgia.
Relacionados ao Paciente: 1. Obesidade (IMC > 35), 2. Sexo Masculino, 3. Idade > 65 anos, 4. Diabetes Mellitus e 5. ASA > 2.
Relacionadas a Doença: 1. Colecistite Aguda, 2. Líquido Pericolecístico, 3. Pós – CPRE, 4. Síndrome de Mirizzi e 5. Edema da parede da vesícula > 5 mm.
Relacionadas a Cirurgia: 1. Hemorragia, 2. Aderências firmes, 3. Anatomia obscura, 4. Fístulas internas e 5. Cirurgia abdominal prévia.
POST-HEPATECTOMY ADVERSE EVENTS
Hepatic resection had an impressive growth over time. It has been widely performed for the treatment of various liver diseases, such as malignant tumors, benign tumors, calculi in the intrahepatic ducts, hydatid disease, and abscesses. Management of hepatic resection is challenging. Despite technical advances and high experience of liver resection of specialized centers, it is still burdened by relatively high rates of postoperative morbidity and mortality. Especially, complex resections are being increasingly performed in high risk and older patient population. Operation on the liver is especially challenging because of its unique anatomic architecture and because of its vital functions. Common post-hepatectomy complications include venous catheter-related infection, pleural effusion, incisional infection, pulmonary atelectasis or infection, ascites, subphrenic infection, urinary tract infection, intraperitoneal hemorrhage, gastrointestinal tract bleeding, biliary tract hemorrhage, coagulation disorders, bile leakage, and liver failure. These problems are closely related to surgical manipulations, anesthesia, preoperative evaluation and preparation, and postoperative observation and management. The safety profile of hepatectomy probably can be improved if the surgeons and medical staff involved have comprehensive knowledge of the expected complications and expertise in their management.
Classroom: Hepatic Resections
The era of hepatic surgery began with a left lateral hepatic lobectomy performed successfully by Langenbuch in Germany in 1887. Since then, hepatectomy has been widely performed for the treatment of various liver diseases, such as malignant tumors, benign tumors, calculi in the intrahepatic ducts, hydatid disease, and abscesses. Operation on the liver is especially challenging because of its unique anatomic architecture and because of its vital functions. Despite technical advances and high experience of liver resection of specialized centers, it is still burdened by relatively high rates of postoperative morbidity (4.09%-47.7%) and mortality (0.24%-9.7%). This review article focuses on the major postoperative issues after hepatic resection and presents the current management.
REVIEW_ARTICLE_HEPATECTOMY_COMPLICATIONS
PANCREATIC PSEUDOCYST
Classroom: Principles of Pancreatic Surgery
The pancreatic pseudocyst is a collection of pancreatic secretions contained within a fibrous sac comprised of chronic inflammatory cells and fibroblasts in and adjacent to the pancreas contained by surrounding structures. Why a fibrous sac filled with pancreatic fluid is the source of so much interest, speculation, and emotion amongst surgeons and gastroenterologists is indeed hard to understand. Do we debate so vigorously about bilomas, urinomas, or other abdominal collections of visceral secretions? Perhaps it is because the pancreatic pseudocyst represents a sleeping tiger, which though frequently harmless, still can rise up unexpectedly and attack with its enzymatic claws into adjacent visceral and vascular structures and cause lifethreatening complications. Another part of the debate and puzzlement about pancreatic pseudocysts is related to confusion about pancreatic pseudocyst definition and nomenclature. The Atlanta classification, developed in 1992, was a pioneering effort in describing and defining morphologic entities in acute pancreatitis. Since then, a working group has been revising this system to incorporate more modern experience into the terminology. In the latest version of this system, pancreatitis is divided into acute interstitial edematous pancreatitis (IEP) and necrotizing pancreatitis (NP), based on the presence of pancreatic tissue necrosis. The fluid collections associated with these two “types” of pancreatitis are also differentiated. Early (<4 weeks into the disease course) peripancreatic fluid collections in IEP are referred to as acute peripancreatic fluid collections (APFC), whereas in NP, they are referred to as postnecrotic peripancreatic fluid collections (PNPFC). Late (>4 weeks) fluid collections in IEP are called pancreatic pseudocysts, and in NP, they are called walled-off pancreatic necrosis (WOPN).
Review of POSTGASTRECTOMY SYNDROMES

The first postgastrectomy syndrome was noted not long after the first gastrectomy was performed: Billroth reported a case of epigastric pain associated with bilious vomiting as a sequel of gastric surgery in 1885. Several classic treatises exist on the subject; we cannot improve on them and merely provide a few references for the interested reader. Surgical procedures on the stomach, performed for reasons such as peptic ulcer disease, cancer, obesity, or gastroesophageal reflux disease, can result in various post-gastrectomy syndromes. These syndromes include chronic symptoms that range from mild discomfort to life-altering conditions. This guide covers the most common syndromes and their characteristics.
GASTRECTOMY VIDEO SURGERY
Dumping Syndrome
Dumping Syndrome is characterized by gastrointestinal and vasomotor symptoms that occur after food intake due to rapid gastric emptying. This syndrome can occur after surgeries that alter the regulation of gastric emptying or gastric compliance, such as gastrectomy, proximal vagotomy, sleeve gastrectomy, fundoplication, pyloroplasty, and gastrojejunostomy (GJ). Depending on the speed of emptying and the osmolarity of gastric contents, symptoms can vary.
- Early Dumping: Occurs within 30 minutes after food intake and is characterized by palpitations, tachycardia, fatigue, a need to lie down after meals, flushing or pallor, sweating, dizziness, hypotension, headache, and possibly syncope. Abdominal symptoms include early satiety, epigastric fullness, abdominal pain, bloating, hypermotility, and splenic blood pooling.
- Late Dumping: Appears 1 to 3 hours after eating, due to reactive hypoglycemia caused by an initially high glucose load leading to an inappropriately high insulin response. Symptoms include sweating, faintness, difficulty concentrating, and altered levels of consciousness.
Diagnosis is confirmed through an oral glucose tolerance test or a gastric emptying scintigraphy study.
Post-Vagotomy Diarrhea
Post-vagotomy diarrhea is a common complication after vagotomy, characterized by frequent episodes of watery diarrhea. It can be attributed to changes in intestinal motility and bile secretion.
Gastric Stasis
Gastric stasis or delayed gastric emptying can occur due to disruption of normal gastric motility. Symptoms include nausea, vomiting, and a feeling of fullness. Diagnosis is confirmed through gastric emptying studies.
Bile Reflux Gastritis
Bile reflux gastritis is caused by the reflux of bile into the stomach, resulting in epigastric pain and bilious vomiting. Diagnosis can be confirmed through upper endoscopy and gastric pH monitoring.
Afferent and Efferent Loop Syndromes
Afferent loop syndrome occurs after Billroth II reconstruction and is characterized by abdominal pain, bilious vomiting, and distention. Efferent loop syndrome occurs when there is an obstruction of the efferent loop, leading to similar symptoms.
Roux Syndrome
Roux syndrome is a complication of Roux-en-Y procedures, characterized by postprandial abdominal pain and vomiting. Diagnosis is made through a contrast gastrointestinal transit study.
Therapeutic Approach
Management of post-gastrectomy syndromes includes dietary modifications, such as eating small frequent meals, separating liquids and solids, increasing protein and fat intake, and reducing simple sugars. In some cases, additional pharmacological or surgical interventions may be necessary. Understanding these syndromes and their therapeutic approaches is crucial to providing effective care and improving the quality of life for post-gastrectomy patients.
This article focuses on the small proportion of patients with severe, debilitating symptoms; these symptoms can challenge the acumen of the surgeon who is providing the patient’s long-term follow-up and care.
POSTGASTRECTOMY_SYNDROMES_REVIEW_ARTICLE
Complications of HEMORROIDH SURGERY
Symptomatic hemorrhoids require a number of therapeutic interventions each of which has its own complications. Office-based therapy such as rubber band ligation carries the risk of pain and bleeding, which are self-limited, but also carries the risk of rare complications such as sepsis, which may be life threatening. Operative treatment of hemorrhoids includes conventional hemorrhoidectomy, stapled hemorrhoidectomy, and the use of energy devices. Complications of pain and bleeding are common but self-limited. Late complications such as stenosis and fecal incontinence are rare. Recurrent disease is related to the initial grade and therapeutic approach. Treatment of recurrent hemorrhoids should be individualized based on previous treatments and the grade of disease. Anesthetic complications, especially urinary retention, are common and related to the anesthetic technique. Practitioners should council their patients as to the risks of the various approaches to treating symptomatic hemorrhoids.
Intra Abdominal Infections
With intra-abdominal infection being one of the most common reasons for surgical consultation, understanding the evaluation and management of these processes becomes paramount in the day- to-day practice of the surgeon. The very broad nature of who is affected coupled with the interplay of patient comorbidities and their medications make dealing with intra-abdominal infections a challenge. As with most complex problems in medicine, it is often useful to break them down into simpler and smaller parts. One useful way to categorize intra-abdominal infections is to divide them into those originating from previous abdominal trauma or operations and those presenting in a “virgin” abdomen.
The latter group most commonly includes those patients presenting with specific organ-based infectious processes such as appendicitis, cholecystitis, or diverticulitis. These individual diseases are covered extensively in other chapters and are discussed only superficially in this chapter. The former are those patients who have sustained intra-abdominal trauma or have undergone previous abdominal interventions and are not recovering in the usual expected course. It is this group that taxes diagnostic and clinical skills and may require the most complex medical decision making.
Several factors should come into play once suspicion for an intra-abdominal infection is entertained. These include resuscitation, antibiotic usage, and source control itself. Patients who present with either a suspected or diagnosed intra-abdominal infection should have some form of volume resuscitation. Even without hypotension, there are several reasons why these patients might be volume depleted. These include nausea and vomiting, fluid sequestration within the abdominal cavity or lumen of the bowel, and poor oral intake. As the process progresses, the patient may develop tachypnea, which results in an evaporative fluid loss. By this time, one can often elicit orthostatic hypotension in most patients.
Fluid resuscitation should begin with the administration of isotonic crystalloid and in general be guided by evidence of end organ perfusion (adequate mental status, urine output, correction of acidosis). There is no utility-using colloid such as albumin or hetastarch in these circumstances, and some data suggest a worse outcome. Should the patient present with hypotension or evidence of poor perfusion, a more aggressive approach to volume resuscitation should be employed. Our recommendation is to follow the current surviving sepsis guidelines, which include fluid challenges, monitoring/assessment of filling pressures, and the potential use of pressors and steroids.
KIDNEY INJURY on perioperative period
ACUTE KIDNEY FAILURE_REVIEW ARTICLE
Alterations in renal function are common after surgical emergencies, trauma, and major operations. In these settings, successful recovery of renal function is dependent on prompt diagnosis and protective management strategies. Acute kidney injury (AKI) is characterized by an acute decrease in glomerular filtration rate (GFR). The true incidence of AKI and acute renal failure (ARF) has been difficult to define, given the broad and various definitions used to quantify and study altered renal function. Relatively recent introduction of consensus definitions, such as RIFLE (risk, failure, loss, and end-stage renal failure) criteria and AKIN (Acute Kidney Injury Network) staging, have provided standard definitions to facilitate more uniform outcome reporting. With use of these definitions, recent studies suggest that AKI occurs in up to two thirds of patients in the intensive care unit (ICU). Moreover, increasing severity of AKI is associated with increasing mortality. AKI is also associated with increased morbidity, such as increased hospital length of stay and cost of care, and has been linked to other in-hospital complications, such as increased difficulty in weaning from mechanical ventilation. Preoperative risk factors for development of AKI include older age, emergent surgery, hepatic disease, obesity, high-risk surgery, vascular disease, and chronic obstructive pulmonary disease (COPD). Prompt recognition of AKI facilitates effective treatment. Although the incidence rate of AKI appears to be rising, overall outcomes from AKI are gradually improving.
The reported mortality rate of AKI is 30% to 60%. If RRT is necessary, reported mortality rates are over 50%. The reason for such high mortality is that AKI now usually occurs as part of a spectrum of multiple organ failure, most often associated with severe sepsis or septic shock. The mortality in this setting is often determined by the underlying septic syndrome, rather than by complications of individual organ failure. Of surviving patients of AKI, a significant number have development of chronic renal insufficiency, which necessitates chronic dialysis. The precise rate of development of chronic renal failure varies greatly in the literature, depending on the patient populations. A recent review of AKI estimates that overall, the risk of necessary chronic dialysis is approximately 12%.
Laparoscopic Surgery for Morbid Obesity
The morbid obesity epidemic continues to spread throughout industrialized nations. It is a condition with a heterogeneous etiology, including genetic, psychosocial, and environmental factors. Prevention methods have currently been unable to halt the further spread of this disease. Obesity has been linked to increased healthcare costs, common physiologic derangements, reduced quality of life, and increased overall mortality. More than one third of adults and almost 17% of children in the United States are obese.
Medical therapy that can cause sustained significant weight loss may be years away. Bariatric surgery, when combined with a multidisciplinary team, continues to be the only proven method to achieve sustained weight loss in most patients. Bariatric procedures modify gastrointestinal anatomy and, in some cases, enteric hormone release to reduce caloric intake, reduce absorption, and alter metabolism to achieve weight loss. Currently, the three most common bariatric operations in the United States are Roux-en-Y gastric bypass, adjustable gastric band, and the vertical sleeve gastrectomy.
GOSSIPIBOMA
O Inimigo Oculto no Bloco Operatório e o Desafio Médico-Legal na Cirurgia Digestiva
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 11 minutos)
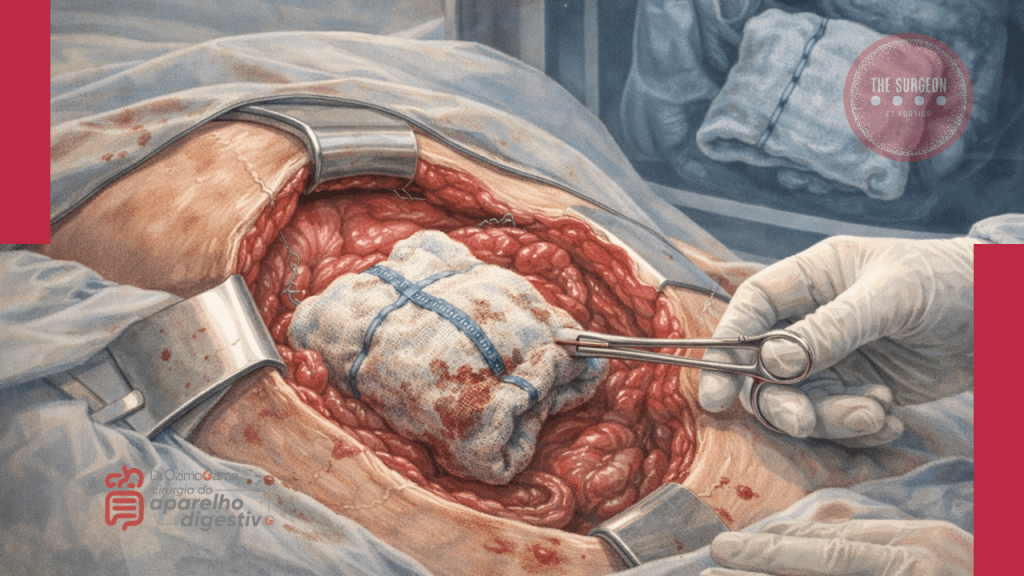
Introdução
No vasto e complexo universo da cirurgia do aparelho digestivo, poucos eventos adversos geram tanta perplexidade clínica e devastação médico-legal quanto o “gossipiboma”. O termo deriva do latim Gossypium (algodão) e do swahili boma (esconderijo), designando uma matriz de matéria têxtil envolvida por uma reação de corpo estranho. Também apelidado de “textiloma”, o seu primeiro caso foi descrito por Wilson em 1884. Embora gazes e compressas sejam as ferramentas mais básicas de qualquer laparotomia, o seu esquecimento no interior da cavidade abdominal transforma um material de hemostase num tumor iatrogénico. A incidência real dos gossipibomas é subnotificada — primariamente devido ao estigma e às pesadas implicações legais da sua deteção —, mas representa uma falha catastrófica nos protocolos de segurança do bloco operatório. Para o cirurgião e para toda a equipa, compreender a fisiopatologia, os fatores de risco e, sobretudo, os métodos de prevenção desta entidade é um dever ético inegociável.
Epidemiologia e Fatores de Risco
Estima-se que a retenção de material têxtil ocorra numa frequência de 1 a cada 1.000 a 1.500 operações intra-abdominais. A cavidade abdominal e pélvica é, de longe, o “esconderijo” mais comum devido à sua vasta anatomia e aos recessos profundos.
O gossipiboma não é um mero fruto do acaso; ele prospera no caos. A literatura científica identifica fatores predisponentes cruciais:
- Cirurgia de Emergência: A incidência é nove vezes maior nestes cenários.
- Mudança de Tática Intraoperatória: Alterações não planeadas no decorrer da intervenção elevam o risco em quatro vezes.
- Fatores do Doente e do Ambiente: Doentes com obesidade mórbida, perdas hemáticas maciças que exigem tamponamento rápido, tempo operatório prolongado e, criticamente, a troca de turnos do pessoal médico e de enfermagem (instrumentistas e circulantes) durante o ato cirúrgico.
Fisiopatologia e Evolução Clínica
O relógio biológico do gossipiboma é imprevisível. O tempo entre a operação primária e as manifestações clínicas pode variar de meros 10 dias a várias décadas. A patologia manifesta-se essencialmente através de duas reações orgânicas distintas:
- Resposta Assética Fibrinosa (Crónica): O material têxtil, se permanecer estéril, induz a produção de fibrina, originando aderências e o encapsulamento do corpo estranho (granuloma). O doente pode permanecer completamente assintomático durante anos, ou apresentar queixas inespecíficas e uma massa abdominal palpável que mimetiza uma neoplasia.
- Resposta Exsudativa (Aguda): Ocorre uma infeção secundária severa, culminando na formação de abcessos e fístulas. O material retido tenta encontrar uma via de exteriorização, podendo fistulizar para órgãos internos (estômago, intestino, cólon, bexiga) ou formar uma fístula externa na parede abdominal. Nestes casos, o doente apresenta um quadro florido: dor abdominal, náuseas, vómitos, febre, sépsis, hemorragia digestiva crómica ou síndrome de má absorção.
Diagnóstico, Tratamento e Prognóstico
A ausência de sintomas precoces ou a sua inespecificidade tornam o diagnóstico um autêntico desafio. O cirurgião deve manter um elevado índice de suspeição perante qualquer massa abdominal num doente com história de laparotomia prévia.
- O Padrão-Ouro Diagnóstico: A Tomografia Computorizada (TC) de abdómen é o exame de eleição. A imagem clássica revela uma lesão cística de aspeto “espongiforme” (padrão em miolo de pão), uma cápsula hiperdensa em camadas concêntricas e, ocasionalmente, calcificações murais. A presença de gás no interior da lesão sem evidência de perfuração intestinal é altamente sugestiva.
- Tratamento: A remoção cirúrgica (seja por via laparoscópica em casos altamente selecionados ou laparotomia) é o único tratamento curativo.
- Prognóstico: A excisão atempada é vital para evitar complicações que elevam a taxa de mortalidade para valores inaceitáveis de 11% a 35%. Se a retenção for crónica, a severidade das aderências pode exigir ressecções intestinais extensas e complexas.
Implicações Médico-Legais e Procedimentos Preventivos
O gossipiboma é indiscutivelmente uma falha grave na prestação de cuidados de saúde (malpractice). Do ponto de vista médico-legal, a responsabilidade é frequentemente partilhada entre o cirurgião principal — o “capitão do navio” — e a equipa de enfermagem responsável pela contagem.
A abordagem definitiva é, e sempre será, a Prevenção. A adoção de protocolos rígidos no bloco operatório salva vidas e carreiras:
- Contagem Meticulosa Universal: São mandatárias quatro contagens rigorosas do material cirúrgico: na montagem da mesa, imediatamente antes da incisão, no início do encerramento da aponevrose e durante a síntese da pele.
- Material Radiopaco: O uso exclusivo de compressas e gazes equipadas com filamentos radiopacos é obrigatório.
- Exploração Ativa: Autores como Dhillon e Park reforçam a necessidade primária da exploração manual e visual dos quatro quadrantes abdominais pelo cirurgião no final do procedimento, independentemente de uma contagem de compressas declarada “correta”.
- Conduta Perante Falha na Contagem: Se a contagem final for divergente, a síntese da cavidade não deve ser concluída até que o material seja localizado (a menos que haja instabilidade hemodinâmica crítica). A realização de uma radiografia intraoperatória imediata é mandatária.
Conclusões Aplicadas
O gossipiboma não é uma complicação inerente e aceitável do ato cirúrgico; é uma falha de sistema e de liderança. O aumento aparente da sua incidência exige que os métodos, a comunicação e a disciplina no interior do bloco operatório sejam revistos e aperfeiçoados. Para os jovens cirurgiões e residentes, a mensagem é clara: a cirurgia de excelência não termina na anastomose perfeita, mas sim na verificação obsessiva e no respeito incondicional pelos protocolos de segurança. A verdadeira destreza cirúrgica repousa na humildade de nunca presumir que a cavidade está vazia sem antes a inspecionar exaustivamente.
“A confiança é um sentimento nobre, mas no bloco operatório, a dupla verificação é a única garantia de segurança. Um erro de omissão pode ensombrar o mais brilhante dos procedimentos cirúrgicos.” — Aforismo da Segurança do Doente Cirúrgico.
Gostou ❔Deixe-nos um comentário ✍️ , partilhe nas suas redes sociais e|ou envie a sua dúvida pelo 💬 Chat On-line na nossa DM do Instagram.
10 Princípios da interação PACIENTE – CIRURGIÃO
Comunicação, Ética e Segurança na Prática Cirúrgica
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 11 minutos)
Introdução
Quando a perspectiva de uma intervenção cirúrgica se impõe — seja para a ressecção de uma neoplasia gástrica, a correção de uma hérnia complexa ou o tratamento metabólico da obesidade —, o medo, a apreensão e a sensação de perda de controle são reações viscerais e universais do ser humano. A visão da dor, o fantasma das complicações e a entrega do próprio corpo ao bisturi de outrem geram uma ansiedade que a mais avançada tecnologia robótica não é capaz de aplacar. No Brasil, onde realizamos milhões de procedimentos cirúrgicos anualmente pelo Sistema Único de Saúde (SUS) e pela Saúde Suplementar, estatísticas dos Conselhos Regionais de Medicina (CRMs) revelam um dado alarmante: mais de 70% das denúncias e processos ético-profissionais por suposto “erro médico” não nascem de falhas técnicas grosseiras, mas da quebra, deterioração ou inexistência de uma relação médico-paciente sólida e transparente. Para o estudante de medicina e o residente de cirurgia, compreender que a destreza manual deve ser precedida pela empatia relacional é o primeiro passo para a maestria.
Os 10 Princípios da Prática Cirúrgica Ética
Para enfrentar os desafios do perioperatório de forma eficaz e blindar a relação terapêutica contra ruídos e frustrações, estruturamos os 10 princípios fundamentais que regem a interação entre o cirurgião e o paciente:
1. Construção da Confiança Mútua
A cirurgia não é um ato comercial; é um pacto de confiança. O cirurgião deve dedicar tempo qualitativo na consulta, evitando o modelo impessoal e apressado (“medicina de linha de montagem”). Um relacionamento humanizado evita que insucessos terapêuticos se transformem em acusações injustas.
2. Clareza e Transparência na Informação
O consentimento deve ser genuinamente esclarecido, não apenas assinado. É imperativo banir o jargão técnico excessivo. Traduzir a fisiopatologia e o plano cirúrgico para uma linguagem acessível reduz o medo do desconhecido e prepara o paciente e seus familiares para o desdobramento natural do pós-operatório.
3. Alinhamento de Expectativas Realistas
Muitas frustrações cirúrgicas nascem do hiato entre a expectativa do paciente e a realidade biológica. É vital discutir os limites da medicina. Prometer “cura absoluta” ou “risco zero” é uma falácia ética.
4. Avaliação Abrangente de Riscos
O Risco Cirúrgico transcende a avaliação cardiológica (Escore de Goldman ou Lee). A avaliação pré-operatória moderna exige uma visão holística: o estado nutricional, a fragilidade (especialmente em idosos), a sarcopenia e, crucialmente, a saúde mental do paciente devem ser exaustivamente investigados.
5. O Papel Estratégico do Anestesiologista
O ato cirúrgico é indissociável do ato anestésico. A escolha da técnica anestésica (bloqueios, anestesia geral, monitorização multimodal) é uma decisão compartilhada. O cirurgião deve fomentar o encontro pré-operatório entre o paciente e a equipe de anestesiologia para dirimir receios e garantir as melhores práticas.
6. Preparação para Mudanças de Rota (O Imprevisto)
O paciente deve entrar no centro cirúrgico ciente de que a tática operatória pode ser alterada. O consentimento para uma laparoscopia deve invariavelmente incluir a possibilidade de conversão para via aberta. Surpresas intraoperatórias (como invasões tumorais insuspeitas) alteram o prognóstico, o tempo de internação e as necessidades de reabilitação.
7. Documentação Exaustiva e Irretocável
O prontuário médico é a testemunha ocular do cuidado. Detalhes das consultas preliminares, opções terapêuticas recusadas pelo paciente e as orientações fornecidas devem estar meticulosamente registrados. Como já abordamos em nosso artigo sobre o método S.O.A.P., documentação é proteção mútua.
8. Descrição Cirúrgica e Rastreabilidade
A descrição do ato operatório deve ser um relato literário da técnica executada. Além disso, a gestão de peças cirúrgicas (envio para exame anatomopatológico) exige rigor logístico. A falha na identificação ou a perda de uma biópsia é uma tragédia diagnóstica inaceitável.
9. Pós-Operatório: Presença e Cuidado Contínuo
O ato cirúrgico não termina no fechamento da pele. O acompanhamento pós-operatório (na UTI, na enfermaria e no ambulatório) exige a presença física e atenciosa do cirurgião principal. Delegar todo o pós-operatório a terceiros é uma das maiores fontes de ressentimento por parte dos pacientes.
10. Atenção ao Estado Emocional
A instabilidade emocional predispõe a uma resposta inflamatória exacerbada e a uma percepção amplificada da dor. Pacientes com ansiedade severa ou depressão pré-existente exigem suporte psicológico ou psiquiátrico adjuvante para garantir resiliência durante a convalescença.
Aplicação na Cirurgia Digestiva
Na cirurgia do aparelho digestivo, estes princípios encontram aplicação diária e visceral:
- Na Cirurgia Bariátrica: O alinhamento de expectativas (Princípio 3) é o alicerce do sucesso. O paciente deve compreender que o bisturi altera a anatomia (Restrição/Incretinas), mas não opera a mente. O reganho de peso é uma possibilidade real se não houver adesão multidisciplinar (Princípio 10).
- Na Cirurgia Oncológica: Informar um paciente sobre a possível necessidade de um estoma (colostomia ou ileostomia) definitivo ou temporário (Princípio 6) exige tato excepcional (Princípio 2). Esconder essa possibilidade para “evitar o sofrimento prévio” destrói a confiança se o paciente acordar com uma bolsa coletora no abdome.
- Na Cirurgia Biliar e Pancreática: Complicações temidas, como a fístula biliar ou pancreática, devem ser discutidas com transparência empática. Quando a complicação ocorre, a presença diária e incansável do cirurgião à beira do leito (Princípio 9) é o que diferencia o abandono do amparo.
Pontos-Chave para a Prática Diária
- Comunicação é Procedimento: Trate a conversa com o paciente e a família com o mesmo rigor técnico que você trata a dissecção de um hilo hepático.
- A Verdade Suportável: Nunca minta, mas adeque a entrega da informação à capacidade de absorção do paciente naquele momento.
- Consentimento Individualizado: Termos de consentimento (TCLE) padronizados e genéricos não possuem força legal. O TCLE deve espelhar as peculiaridades anatômicas e biológicas do paciente específico.
Conclusões Aplicadas
A ética na cirurgia moderna vai imensuravelmente além da destreza técnica, dos nós bem atados e da ausência de complicações infecciosas. Trata-se do respeito à autonomia daquele que se submete à lâmina. A prática cirúrgica de excelência exige que sejamos peritos em fisiologia e mestres em humanidade. O cirurgião do aparelho digestivo que domina estes 10 princípios navega pelas tempestades de uma fístula anastomótica não como um réu diante de um juiz (o paciente), mas como um comandante ao lado de seu companheiro de naufrágio, trabalhando juntos para alcançar a margem segura da cura.
“O bom cirurgião opera com a mão; o cirurgião brilhante opera com o cérebro; mas o cirurgião extraordinário opera com o coração. O bisturi corta tecidos, mas é a compaixão que cicatriza as feridas da alma.” — Adaptado dos princípios humanitários de Sir William Osler, pai da medicina moderna.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
PRINCIPLES OF OSTOMY MANAGEMENT

The creation of a stoma is a technical exercise. Like most undertakings, if done correctly, the stoma will usually function well with minimal complications for the remainder of the ostomate’s life. Conversely, if created poorly, stoma complications are common and can lead to years of misery. Intestinal stomas are in fact enterocutaneous anastomoses and all the principles that apply to creation of any anastomosis (i.e., using healthy intestine, avoiding ischemia and undue tension) are important in stoma creation.
MOST COMMOM POSTOPERATIVE PROBLEMS
Despite good preoperative assessment, surgical and anaesthetic technique and perioperative management, unexpected symptoms or signs arise after operation that may herald a complication. Detecting these early by regular monitoring and surgical review means early treatment can often forestall major deterioration. Managing problems such as pain, fever or collapse requires correct diagnosis then early treatment. Determining the cause can be challenging, particularly if the patient is anxious, in pain or not fully recovered from anaesthesia. It is vital to see and assess the patient and if necessary, arrange investigations, whatever the hour, when deterio-ration suggests potentially serious but often remediable complications. Consider also whether and when to call for senior help.
PREVENTION COMPLICATIONS OF COLON SURGERY
COMPLICATIONS OF COLON SURGERY_REVIEW ARTICLE

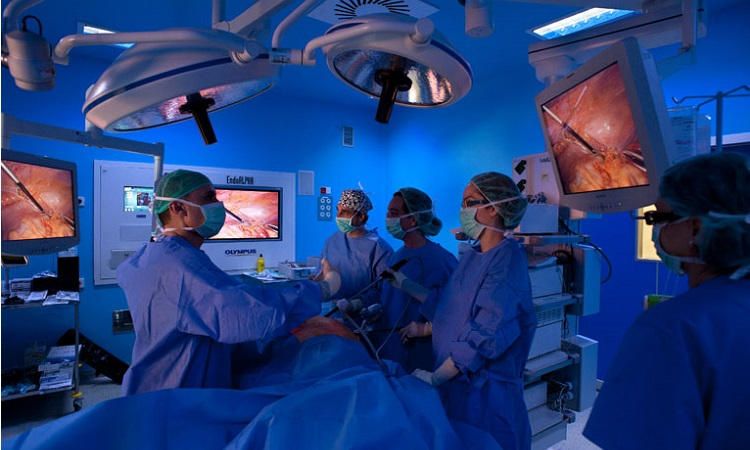
Colon surgery represents a high number of patients treated at a department of gastrointestinal surgery and is not limited to colon cancer. It includes other non-neoplastic pathologies such as inflammatory bowel disease, diverticular disease or colonic volvulus. As with any major procedure, colon surgery patients may present serious or even fatal complications. The incidence of postoperative complications from colon surgery has been estimated at between 10% and 30% according to selected series. Preventive measures against surgical complications include selection of an appropriate procedure for the patient as well as good preoperative care, appropriate surgical technique and good postoperative management. When diagnosis has been established, risks for patient should be assessed according to patient’s health conditions and type of surgery accomplished. When the patient meets the surgical requirements, an appropriate course of preoperative care should be carried out including colon wash antibiotics and antithrombotic prophylaxis. Postoperative period will be equivalent to any major abdominal surgery. Typically, it was considered appropriate to wait a few days before initiating feeding in order to protect anastomosis; however, some authors agree that an early oral diet hours after intervention is not associated with a higher risk of anastomotic dehiscence and other complications.
Sleeve Gastrectomy: Complications and Management
SLEEVE GASTRECTOMY COMPLICATIONS_REVIEW ARTICLE
 Obesity is a common disease affecting adults and children. The incidence of obesity in worldwide is increasing. Laparoscopic sleeve gastrectomy (LSG) is a relatively new and effective procedure for weight loss. Owing to an increase in the number of bariatric surgical procedures, general surgeons should have an understanding of the complications associated with LSG and an approach for dealing with them. Early postoperative complications following LSG that need to be identified urgently include bleeding, staple line leak and development of an abscess. Delayed complications include strictures, nutritional deficiencies and gastresophageal reflux disease. We discuss the principles involved in the management of each complication.
Obesity is a common disease affecting adults and children. The incidence of obesity in worldwide is increasing. Laparoscopic sleeve gastrectomy (LSG) is a relatively new and effective procedure for weight loss. Owing to an increase in the number of bariatric surgical procedures, general surgeons should have an understanding of the complications associated with LSG and an approach for dealing with them. Early postoperative complications following LSG that need to be identified urgently include bleeding, staple line leak and development of an abscess. Delayed complications include strictures, nutritional deficiencies and gastresophageal reflux disease. We discuss the principles involved in the management of each complication.
PERIOPERATIVE FLUID MANAGEMENT IN SURGERY
REVIEW ARTICLE_FLUID MANAGEMENT IN ELECTIVE SURGERY
The purpose of the thesis was to investigate the pathophysiology and functional outcomes of various fluid administration regimens in elective surgical procedures and describe factors of importance in perioperative fluid management. The goal was to create a rational physiologic background on which to design future ran-domized, clinical trials focusing on clinical outcomes aiming to produce evidence-based guidelines for rational perioperative fluid therapy. The main hypothesis of the thesis was thatthe ”liberal” fluid administration regimens seen in daily clinical practice may be detrimental and contribute to increased perioperative morbid-ity primarily due to increased functional demands of the cardi-opulmonary system and gastrointestinal tract as well as de-creased tissue oxygenation (impaired wound healing).
Ebook: Princípios da Cirurgia Hepatobiliar

Cirurgia Hepatobiliar
Considera-se que a cirurgia hepática começou após o advento da anestesia e da anti-sepsia. No entanto, muito antes disso, diversos autores já relatavam suas experiências com ressecções do fígado. As primeiras descrições de “cirurgias hepáticas” consistiam no relato de avulsões parciais ou totais de porções do fígado após lesões traumáticas do abdome. O relato de Elliot (1897) exemplifica muito dos temores dos cirurgiões da época: “O fígado (…) é tão friável, tão cheio de vasos e tão evidentemente impossível de ser suturado que parece ser improvável o manejo bem sucedido de grandes lesões de seu parênquima”.
CIRURGIA HEPATOBILIAR_ASPECTOS BÁSICOS
POSTOPERATIVE ILEUS
POSTOPERATIVE ILEUS_REVIEW ARTICLE
 In systems that try to minimize hospital stay after abdominal surgery, one of the principal limiting factors is the recovery of adequate bowel function, which can delay discharge or lead to readmission. Postoperative ileus (POI) is the term given to the cessation of intestinal function following surgery. Although all surgical procedures put the patient at risk for POI, gastrointestinal tract surgeries in particular are associated with a temporary cessation of intestinal function. The duration of POI varies, lasting from a few hours to several weeks. Prolonged postoperative ileus, also known as pathologic postoperative ileus, can be caused by a myriad of pathologic processes that are treated with limited success by clinical and pharmacologic management. Studies of large administrative databases show that, on average, patients with a diagnosis of POI stay 5 days longer in hospital after abdominal surgery than patients without POI. Over the last decade, substantial efforts have been made to minimize the duration of POI, as there appears to be no associated physiologic benefit, and it is currently the primary factor delaying recovery for most patients. In this review, we define POI, describe the pathogenesis and briefly discuss clinical management before detailing current pharmacologic management options.
In systems that try to minimize hospital stay after abdominal surgery, one of the principal limiting factors is the recovery of adequate bowel function, which can delay discharge or lead to readmission. Postoperative ileus (POI) is the term given to the cessation of intestinal function following surgery. Although all surgical procedures put the patient at risk for POI, gastrointestinal tract surgeries in particular are associated with a temporary cessation of intestinal function. The duration of POI varies, lasting from a few hours to several weeks. Prolonged postoperative ileus, also known as pathologic postoperative ileus, can be caused by a myriad of pathologic processes that are treated with limited success by clinical and pharmacologic management. Studies of large administrative databases show that, on average, patients with a diagnosis of POI stay 5 days longer in hospital after abdominal surgery than patients without POI. Over the last decade, substantial efforts have been made to minimize the duration of POI, as there appears to be no associated physiologic benefit, and it is currently the primary factor delaying recovery for most patients. In this review, we define POI, describe the pathogenesis and briefly discuss clinical management before detailing current pharmacologic management options.
Colonoscopia : Quais as principais complicações?
Colonoscopy is a commonly performed procedure for the diagnosis and treatment of a wide range of conditions and symptoms and for the screening and surveillance of colorectal neoplasia. Although up to 33% of patients report at least one minor, transient GI symptom after colonoscopy, serious complications are uncommon. In a 2008 systematic review of 12 studies totaling 57,742 colonoscopies performed for average risk screening, the pooled overall serious adverse event rate was 2.8 per 1000 procedures. The risk of some complications may be higher if the colonoscopy is performed for an indication other than screening. The colorectal cancer miss rate of colonoscopy has been reported to be as high as 6% and the miss rate for adenomas larger than 1 cm is 12% to 17%. Although missed lesions are considered a poor outcome of colonoscopy, they are not a complication of the procedure per se and will not be discussed further in this document. Over 85% of the serious colonoscopy complications are reported in patients undergoing colonoscopy with polypectomy. An analysis of Canadian administrative data, including over 97,000 colonoscopies, found that polypectomy was associated with a 7-fold increase in the risk of bleeding or perforation. However, complication data are often not stratified by whether or not polypectomy was performed. Therefore, complications of polypectomy are discussed with those of diagnostic colonoscopy. A discussion of the diagnosis and management of all complications of colonoscopy is beyond the scope of this document, although general principles are reviewed.
Risk for POSTOPERATIVE INFECTION
Surgical site infections (SSIs) are a common surgical complication that affects between 2% and 5% of the 30 to 40 million operations that occur in the United States per year. SSIs are the most common nosocomial infection among surgical patients and are consistently the second most common healthcare-associated infection overall. Mortality rates after SSI are markedly higher when compared with patients without an SSI, as are the patient’s length of stay (mean, 7 days), hospital readmission rates, and direct patient costs ($500 to $3000 per infection).
Risk Factors
Development of an SSI requires microorganism contamination at the surgical site. During an operative procedure in which skin is incised, endogenous skin flora, the most common source of pathogens, are introduced into the exposed tissue. Additional sources of bacteria include patient colonization, mucous membrane or hollow viscous pathogens encountered during the operation, surgical personnel, operative instruments, and the operating room environment. An accepted surrogate for bacterial contamination at the surgical site is the wound classification. The risk of SSI increases with the degree of contamination and higher wound classifications. Wounds are classically defined as clean, clean-contaminated, contaminated, or dirty/infected. The NHSN developed a risk index by which the risk of an SSI can be predicted based on three major criteria: wound classification, American Society of Anesthesiologists (ASA) score, and duration of the operation. The SSI risk category is based on the number of factors present at the time of operation, including a wound class of 3 (contaminated) or 4 (dirty), an ASA class of 3 or greater, and an operation lasting longer than the 75th percentile of the duration of the specific operation. Each independent factor is given a single point if present, which determines the NHSN risk index category (0 to 3).
- 1. Smoking
- 2. Diabetes
- 3. COPD: Chronic obstructive pulmonary disease
- 4. CAD: coronary artery disease
- 5. Nutritional status
- 6. Immunosuppression
- 7. Chronic corticosteroid use
- 8. Low serum albumin
- 9. Obesity
- 10. Advanced age
Retromuscular Prefascial Mesh Hernia Repair (Jean RIVES – René STOPPA)
An incisional hernia is usually defined as a chronic postoperative defect of the abdominal wall through which intra-abdominal viscera protrude. Progress in surgical techniques, even with laparoscopic surgery, has not led to the elimination of incisional hernias. On the contrary, the incidence of this complication seems to be increasing as more major and lengthy operations are being performed, especially in elderly patients with concomitant organic disease. The incidence of this condition has been reported to be as high as 11% of all laparotomies. Surgical repair is difficult in the patient with a large abdominal wall defect, especially if the herniated viscera has “lost its right of domain” in the abdominal cavity. It must be remembered that surgical repair of an incisional hernia is not the same thing as closure of a laparotomy. Weakening of the abdominal wall and the consequences of decreased abdominal pressure on diaphragmatic mobility and respiratory function must also be considered. Placement of a prosthetic mesh is essential because without mesh, the recurrence rate is prohibitive, varying from 30% to 60%. The which is the subject of this article, was popularized by Jean Rives and has been used in our department since 1966.
RIVES_STOPPA_HERNIA_REPAIR
Ethics in Surgery : R.I.S.K.
Renewed public attention is being paid to ethics today. There are governmental ethics commissions, research ethics boards, and corporate ethics committees. Some of these institutional entities are little more than window dressing, whereas others are investigative bodies called into being, for example, on suspicion that financial records have been altered or data have been presented in a deceptive manner. However, many of these groups do important work, and the fact that they have been established at all suggests that we are not as certain as we once were, or thought we were, about where the moral boundaries are and how we would know if we overstepped them. In search of insight and guidance, we turn to ethics. In the professions, which are largely self-regulating, and especially in the medical profession, whose primary purpose is to be responsive to people in need, ethics is at the heart of the enterprise.
Responsibility to the patient in contemporary clinical ethics entails maximal patient participation, as permitted by the patient’s condition, in decisions regarding the course of care. For the surgeon, this means arriving at an accurate diagnosis of the patient’s complaint, making a treatment recommendation based on the best knowledge available, and then talking with the patient about the merits and drawbacks of the recommended course in light of the patient’s life values. For the patient, maximal participation in decision making means having a conversation with the surgeon about the recommendation, why it seems reasonable and desirable, what the alternatives are, if any, and what the probable risks are of accepting the recommendation or pursuing an alternative course.
This view of ethically sound clinical care has evolved over the latter half of the 20th century from a doctor-knows-best ethic that worked reasonably well for both patients and physicians at a time when medical knowledge was limited and most of what medicine could do for patients could be carried in the doctor’s black bag or handled in a small, uncluttered office or operating room. What practical steps can be taken by clinicians to evaluate patient attitudes and behavior relative to the patient’s cultural context so that the physician and patient together can reach mutually desired goals of care? Marjorie Kagawa-Singer and her colleagues at the University of California, Los Angeles, developed a useful tool for ascertaining patients’ levels of cultural influence. It goes by the acronym RISK:
Resources: On what tangible resources can the patient draw, and how readily available are they?
Individual identity and acculturation: What is the context of the patient’s personal circumstances and her degree of integration within her community?
Skills: What skills are available to the patient that allow him to adapt to the demands of the condition?
Knowledge: What can be discerned from a conversation with the patient about the beliefs and customs prevalent in her community and relevant to illness and health, including attitudes about decision making and other issues that may affect the physician-patient relationship.
TRATAMENTO DA TROMBOSE HEMORROIDÁRIA
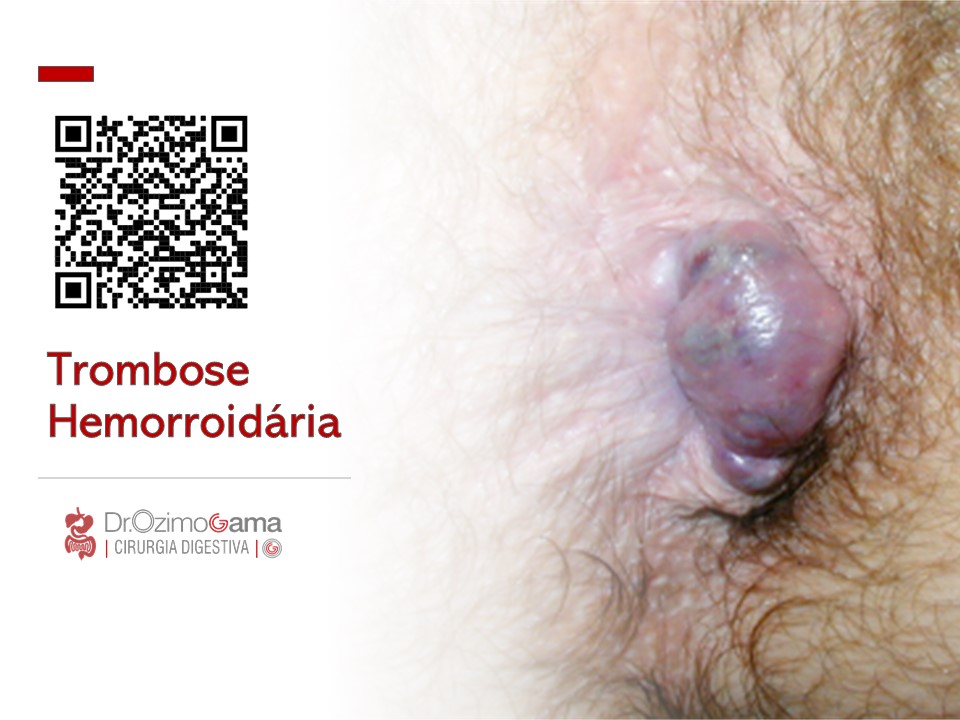
A trombose hemorroidária é uma condição dolorosa e desconfortável que ocorre quando um coágulo de sangue se forma dentro de uma hemorróida. Essa condição é mais comum em gestantes, pessoas com constipação intestinal crônica, e em situações que aumentam a pressão intra-abdominal, como exercícios físicos intensos e levantamento de peso. Neste artigo, exploraremos as causas, sintomas e opções de tratamento para a trombose hemorroidária, ajudando você a entender melhor essa condição e a buscar a melhor abordagem para o seu caso.
Causas da Trombose Hemorroidária
A trombose hemorroidária geralmente está relacionada a fatores de estilo de vida e hábitos pessoais. Os principais gatilhos incluem:
- Obstipação (prisão de ventre): O esforço excessivo para evacuar aumenta a pressão nas veias do ânus, e as fezes endurecidas podem causar traumatismo no tecido anal.
- Gravidez: A pressão adicional no abdômen durante a gravidez pode contribuir para o desenvolvimento da trombose.
- Esforços prolongados e levantamento de peso: Atividades que aumentam a pressão intra-abdominal são fatores de risco.
- Higiene inadequada: A falta de cuidados apropriados na região anal pode exacerbar a condição.
- Fatores adicionais: Permanecer sentado por longos períodos, consumo excessivo de alimentos picantes e bebidas alcoólicas, e prática de sexo anal.
Sintomas da Trombose Hemorroidária
Os principais sinais de trombose hemorroidária incluem:
- Dor intensa na região anal: A dor é geralmente súbita e pode ser bastante severa.
- Sangramento: Frequentemente observado durante a evacuação.
- Inchaço e aumento de volume: Um nódulo na região anal pode se tornar arroxeado ou preto, indicando a presença de um trombo.
Tratamentos Indicados
O tratamento da trombose hemorroidária varia conforme a gravidade da condição. Entre as abordagens recomendadas estão:
- Uso de analgésicos e pomadas anestésicas: Para alívio da dor e desconforto.
- Banhos de assento: Utilizar água morna para aliviar os sintomas e reduzir o inchaço.
- Correção dos hábitos alimentares: Aumentar a ingestão de fibras e líquidos para prevenir a obstipação.
- Tratamento cirúrgico: Em casos mais graves, pode ser necessário realizar uma cirurgia para remover a hemorróida e o trombo.
Se você apresenta sintomas semelhantes, é crucial consultar um médico para uma avaliação adequada e receber o tratamento adequado.
Gostou ❔ Nos deixe um comentário ✍️, ou mande sua dúvida pelo 💬 Chat On-line.
Lembre-se: A informação aqui fornecida é para orientação geral. Sempre consulte seu médico para aconselhamento específico sobre sua situação.
Não Deixe Sua Saúde Esperar! Entre em Contato Conosco Agora!
☎️ CHAT ONLINE 📞
Entre em contato conosco através da nossa central de atendimento dedicada. Nossos especialistas estão prontos para fornecer orientações personalizadas e responder a todas as suas perguntas. Juntos, podemos trabalhar para garantir o melhor para a sua saúde.
🩺(98)991304454 & (98)988664454📲
ATENDIMENTO REMOTO (TELEMEDICINA)
🤳🏻 Agende com os nossos #especialistas pelo WhatsApp ou Telefone
📲 👩🏽⚕️ Clínico: (98) 9 9130 4454
📲 👨🏻⚕️ Cirúrgico: (98) 9 8866 4454
#TromboseHemorroidária #SaúdeDigestiva #TratamentoHemorroidário #BemEstar #CuidadosComASaúde
VEJA AQUI ONDE FAZER UMA AVALIAÇÃO ESPECIALIZADA E RECEBER UMA SEGUNDA OPINIÃO
BILIARY-ENTERIC ANASTOMOSIS
 The operative conduct of the biliary-enteric anastomosis centers around three technical steps: 1) identification of healthy bile duct mucosa proximal to the site of obstruction; 2) preparation of a segment of alimentary tract, most often a Roux-en-Y jejunal limb; and 3) construction of a direct mucosa-to-mucosa anastomosis between these two. Selection of the proper anastomosis is dictated by the indication for biliary decompression and the anatomic location of the biliary obstruction. A right subcostal incision with or without an upper midline extension or left subcostal extension provides adequate exposure for construction of the biliary-enteric anastomosis. Use of retractors capable of upward elevation and cephalad retraction of the costal edges are quite valuable for optimizing visual exposure of the relevant hilar anatomy.
The operative conduct of the biliary-enteric anastomosis centers around three technical steps: 1) identification of healthy bile duct mucosa proximal to the site of obstruction; 2) preparation of a segment of alimentary tract, most often a Roux-en-Y jejunal limb; and 3) construction of a direct mucosa-to-mucosa anastomosis between these two. Selection of the proper anastomosis is dictated by the indication for biliary decompression and the anatomic location of the biliary obstruction. A right subcostal incision with or without an upper midline extension or left subcostal extension provides adequate exposure for construction of the biliary-enteric anastomosis. Use of retractors capable of upward elevation and cephalad retraction of the costal edges are quite valuable for optimizing visual exposure of the relevant hilar anatomy.

Division of the ligamentum teres and mobilization of the falciform ligament off the anterior surface of the liver also facilitate operative exposure; anterocephalad retraction of the ligamentum teres and division of the bridge of tissue overlying the umbilical fissure are critical for optimal visualization of the vascular inflow and biliary drainage of segments II, III, and IV. Cholecystectomy also exposes the cystic plate, which runs in continuity with the hilar plate. Lowering of the hilar plate permits exposure of the left hepatic duct as it courses along the base of segment IVb. In cases of unilateral hepatic atrophy as a result of long-standing biliary obstruction or preoperative portal vein embolization, it is critical to understand that the normal anatomic relationships of the portal structures are altered. In the more common circumstance of right-sided atrophy, the portal and hilar structures are rotated posteriorly and to the right; as a result, the portal vein, which is typically most posterior, is often encountered first; meticulous dissection is necessary to identify the common bile duct and hepatic duct deep within the porta hepatis.
BILIARY-ENTERIC ANASTOMOSIS_THECNICAL ASPECTS
GASTROINTESTINAL STROMAL TUMORS (GIST)
INTRODUÇÃO
GIST, da sigla em inglês gastrointestinal stromal tumors, pertence a um grupo de tumores chamados sarcoma de partes moles. Essa neoplasia se diferencia dos outros tipos de tumores por iniciar-se na parede dos órgãos, junto às camadas musculares do trato gastrointestinal, mais especificamente, nas células do plexo mioenterico, chamadas células de Cajal. Tais células são responsáveis pela motilidade intestinal, sendo consideradas o marca-passo do trato gastrointestinal.
O tumor de GIST é relativamente raro, com estudos atuais mostrando uma prevalência anual em torno de 20 a 40 casos por milhão de habitantes. É mais comum entre pessoas de 50 a 60 anos de idade, sendo extremamente raros até os 20 anos. Por representar um tumor raro, recomenda-se que seja tratado por serviços especializados com cirurgiões do aparelho digestivo, que tenham experiência multidisciplinar na condução e no tratamento dos pacientes com este tumor.
O GIST pode se originar em qualquer local do trato gastrointestinal, do esôfago ao ânus. Em relação à distribuição, 50% a 60% das lesões são provenientes do estômago, 20% a 30% do intestino delgado, 10% do intestino grosso, 5% do esôfago e 5% de outros locais da cavidade abdominal.
DIAGNÓSTICO
A apresentação clínica dos pacientes portadores de GIST não é especifica e depende da localização e do tamanho do tumor. O GIST tem uma característica biológica que é uma mutação genética, com ativação do proto-oncogene Kit e a superexpressão do receptor tirosina quinase (c-Kit). Geralmente, o diagnóstico é feito por uma biópsia da lesão, que a depender da localização, pode ser feita por endoscopia, colonoscopia, ou ecoendoscopia. A tomografia computadorizada do abdômen é importante para avaliação da extensão do tumor e também pode ser utilizada em alguns casos para realização de biópsia do tumor. Não apresentam sinais e/ou sintomas específicos. Podem causar náuseas, vômitos, hemorragias intestinais (vômitos com sangue ou evacuações com sangue ou fezes enegrecidas), sensação de plenitude após alimentação, dor e distensão abdominal, ou presença de uma massa ou tumor palpável no abdômen.
TRATAMENTO
O tratamento padrão para pacientes com GIST não metastático, ou seja, não provenientes de outros órgãos, é a ressecção cirúrgica completa da lesão. Muitas vezes é necessária a cirurgia radical e de grande porte, com a retirada de estruturas e órgãos aderidos, oferecendo a maior chance de cura. O tratamento com imatinib, e mais atualmente ao sunitinib, é utilizado para doença metastática ou irressecável, com intuito de diminuir o tamanho da lesão para que a cirurgia possa ser realizada em melhores condições locais. Tais drogas também podem ser utilizadas após a cirurgia. Para o tratamento sistêmico pode ser necessário estudo genético específico para saber qual a mutação presente no tumor, com intuito de guiar a terapia em relação à dose e tipo de medicação utilizada.
FATORES DE RISCO
Não há fatores de risco diretamente relacionados a essa neoplasia. Manter hábitos de vida saudáveis, uma alimentação balanceada e a prática de exercícios físicos ajudam, de maneira geral, na prevenção do câncer.
PARA MAIS INFORMAÇÕES: http://www.gistsupport.org/
Telas de Baixa Gramatura: PHS e UHS
EVOLUÇÃO HISTÓRICA DA HERNIORRAFIA INGUINAL
As hérnias não diminuem com o tempo, muito pelo contrário – o estado de saúde do paciente só tende a piorar, aumentando o risco cirúrgico – e não existe medicação para tratá-las. Os primeiros registros do tratamento cirúrgico das hérnias abdominais datam de 1500 a.C, mencionadas no Papiro de Ebers. Em 100 d.C. Celso, realizando os primórdios da cirurgia convencional, extirpava o saco herniário e deixava intactos o cordão e o testículo. Já em 700 d.C. , numa conduta mais agressiva, Pablo de Egina, sacrificava o testículo. Utilizando o princípio da cauterização dos tecidos pelo calor, Albucasis em 1000 d.C., expunha o saco herniário e o cauterizava. Com o advento da técnica asséptica registra-se, em 1869, a realização por Lister da primeira hérnia estrangulada em caráter de urgência com princípios antissépticos. O primeiro esboço de padronização da técnica operatória das hérnias abdominais ocorre a partir da publicação dos estudos de Edoardo Bassini, em 1887, primeiro estudo de reparo de hérnias com suturas. A técnica se propaga pelo mundo mas a deficiente comunicação e as múltiplas modificações levam a resultados negativos. Já em 1940, Earle Shouldice, usando quatro planos de reforço, revoluciona a técnica com tensão, principalmente após 1950 com um melhor entendimento da anatomia, porém observam-se ainda recorrências altas, acima de 10%. Em 1967, René Stoppa e Jean Rives, utilizam a técnica pré-peritoneal com a introdução de um novo conceito: a prótese. Uma tela gigante recobrindo todos os possíveis orifícios herniários, obtendo excelente taxa de recidiva, às custas da necessidade de incisão mediana e descolamento amplo pré-peritoneal.
PADRÃO OURO
Somente em 1984 Irving Lichtenstein, por via anterior, utiliza uma tela de polipropileno. Esta técnica foi considerada uma grande evolução e passou, nos anos 90, a ser considerado o Padrão Ouro nos reparos das hérnias inguinais possibilitando, pela primeira vez, o reparo ambulatorial com anestesia local e sedação. Com o inicio da cirurgia videolaparoscópica no início dos anos 90, desenvolveram-se diversas técnicas utilizando-se a tela pela técnica laparoscópica. Devido aos altos custos e complexidade do procedimento cirúrgico e anestésico em comparação à técnica por via aberta, estas não se estabeleceram como melhor opção. Finalmente, em 1997, Arthur Gilbert, inicia o sistema PHS (“Prolene Hernia System”) que reúne as vantagens quanto a recidiva do reparo pré-peritoneal, a simplicidade de fixação da técnica de plug e eficácia da técnica de tela plana através de um reparo tridimensional com uma tela dupla colocada pela via anterior. Dois anos mais tarde, ocorre a publicação dos primeiros resultados do PHS – `Hernia Institute of Florida – USA, firmando o aspecto inovador e a eficácia da tela dupla, otimizando o conforto e segurança do paciente e proporcionando retorno mais precoce às atividades laborativas e utilizando facilmente anestesia local e sedação.
Veja AQUI COMO ESCOLHER A PRÓTESE para seu paciente com Hérnia Abdominal.
Diagnóstico Diferencial dos Tumores do Mediastino
A existência de cistos e tumores primários do mediastino tem vindo a ser relatada com uma incidência crescente. Os avanços das técnicas radiológicas, incluindo a TC e a RM, aumentaram singularmente a capa-cidade de avaliar pré – operatoriamente a natureza e a extensão das lesões do mediastino. Por outro lado, os progressos terapêuticos têm sido relacionados com um diagnóstico mais precoce e com uma maior efetividade dos regimes de radioterapia e de quimioterapia.
ARTIGO DE REVISÃO_TUMORES DO MEDIASTINO
PREVENÇÃO DO TROMBOEMBOLISMO NA CIRURGIA DO CÂNCER DO APARELHO DIGESTIVO
ARTIGO DE REVISÃO_TVP_CÂNCER DO APARELHO DIGESTIVO
Tromboembolismo venoso é complicação frequente após tratamento cirúrgico em geral e, de um modo especial, na condução terapêutica do câncer. A cirurgia do aparelho digestivo tem sido referida como potencialmente indutora desta complicação. Ela tem maior representatividade em determinados segmentos anatômicos e nas condições em que se associam fatores de risco dos pacientes. A prevenção do tromboembolismo é tema de grande importância na prática diária dos cirurgiões. Várias são as formas físicas e medicamentosas que podem ser utilizadas. Nos últimos anos abordagens novas, tanto em relação às manobras físicas como em posologia medicamentosa, têm sido estudadas com boa metodologia. Estes novos enfoques ainda são pouco divulgados e talvez pouco conhecidos pela maioria dos cirurgiões. No câncer a importância desse tema é ainda maior que nas doenças benignas. A Medicina Baseada em Evidências incorpora dados obtidos com base nas mais recentes revisões sistemáticas disponíveis na literatura originando várias formas de contribuições científicas. BOM ESTUDO.
Lesão de Vias Biliares na Colecistectomia: Prevenção e Tratamento
A via laparoscópica tem sido reconhecida como padrão de excelência para a colecistectomias. Phillipe Mouret foi quem primeiro a realizou em 1987, mas outros procedimentos já haviam sido realizados por laparoscopia e foram descritos por ginecologistas. Desenvolvida no final da década de 80 e início dos anos 90, a videolaparoscopia mudou os conceitos de acesso cirúrgico e campo operatório, introduzindo a concepção de “cirurgia minimamente invasiva”.A colecistectomia é um dos procedimentos cirúrgicos mais realizados no mundo. Com o advento da videolaparoscopia, tornou-se uma cirurgia menos traumática, mais estética, com períodos mais curtos de internação. Em contrapartida, observou-se o aumento da incidência de lesões de via biliar extra-hepática quando comparado ao procedimento aberto, fato preocupante devido à morbidade elevada desse tipo de lesão, cuja mortalidade não é desprezível.
Prevenção e Rastreamento do Câncer Colorretal
O Papel Proativo do Cirurgião na Interrupção da Sequência Adenoma-Carcinoma
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 9 minutos)
Introdução
O Câncer Colorretal (CCR) representa um dos maiores paradoxos da oncologia moderna: é uma das neoplasias mais letais e prevalentes no mundo, e, simultaneamente, uma das mais preveníveis. Para o cirurgião do aparelho digestivo, compreender a biologia tumoral e os protocolos de rastreamento (screening) é tão fundamental quanto dominar a técnica de uma retossigmoidectomia com excisão total do mesorreto (TME). A prevenção do CCR não se restringe a orientações dietéticas; ela é um ato intervencionista. Ao compreender e atuar na fisiopatologia da doença, o médico em formação — seja o estudante de medicina ou o residente de cirurgia — assume o protagonismo na redução da morbimortalidade associada a esta patologia.
O Cenário Brasileiro
A relevância do CCR no Brasil exige atenção redobrada. Segundo as estimativas do Instituto Nacional de Câncer (INCA) para o triênio 2023-2025, são esperados cerca de 45.630 novos casos anuais no país. Atualmente, o CCR ocupa a segunda posição entre os cânceres mais incidentes tanto em homens quanto em mulheres (excluindo os tumores de pele não melanoma). As regiões Sul e Sudeste concentram as maiores taxas, refletindo a íntima relação da doença com a urbanização, sedentarismo e ocidentalização da dieta (alto consumo de carne vermelha processada e baixo teor de fibras).
A Janela de Oportunidade Biológica
A pedra angular da prevenção do CCR é a teoria genética da sequência adenoma-carcinoma, descrita classicamente por Vogelstein. Sabemos que mais de 90% dos carcinomas colorretais esporádicos surgem de lesões benignas precursoras (pólipos adenomatosos ou lesões serrilhadas). Esse processo de acúmulo de mutações genéticas (como APC, KRAS, TP53) é lento. Estima-se que a transição de um adenoma inicial para um adenocarcinoma invasivo leve de 10 a 15 anos. Esta progressão insidiosa cria uma “janela de oportunidade” excepcional para a intervenção médica: a detecção e ressecção das lesões precursoras antes que a malignidade se instale.
Fatores de Risco e Prevenção Primária
A prevenção primária foca em evitar o surgimento dos pólipos. Envolve a mitigação de fatores de risco modificáveis:
- Dietéticos: Redução do consumo de carnes processadas e vermelhas; aumento da ingestão de fibras, cálcio e vitamina D.
- Estilo de vida: Combate ao tabagismo, ao etilismo excessivo e à obesidade (o tecido adiposo visceral é um órgão endócrino ativo que promove um estado pró-inflamatório crônico).
Aplicação na Cirurgia Digestiva: O Rastreamento (Prevenção Secundária)
Para o cirurgião endoscopista, a colonoscopia é a arma definitiva. Diferente de outros métodos de rastreio (como a mamografia ou o PSA, que são puramente diagnósticos), a colonoscopia é diagnóstica e terapêutica.
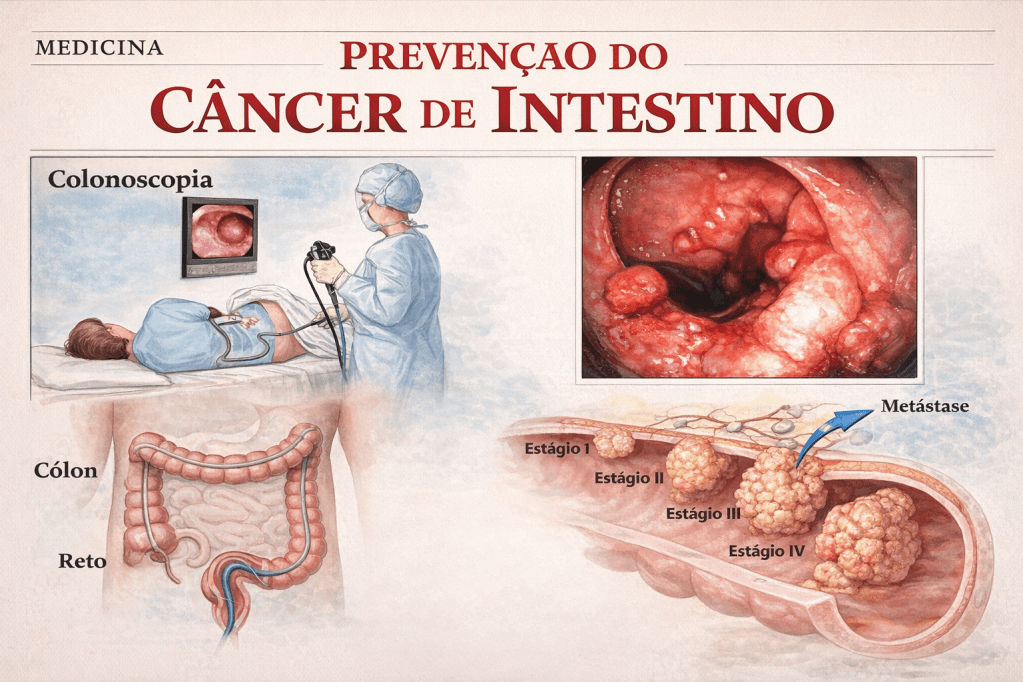
Protocolos de Rastreamento (Screening)
As diretrizes globais sofreram mudanças recentes devido ao aumento alarmante da incidência de CCR em adultos jovens (abaixo dos 50 anos).
- Risco Habitual (População Geral): A Sociedade Americana de Câncer (ACS) e a Força-Tarefa de Serviços Preventivos dos EUA (USPSTF) passaram a recomendar o início do rastreamento aos 45 anos (e não mais aos 50). No Brasil, sociedades médicas (como o CBCD e a SOBED) já endossam essa antecipação. O rastreio pode ser feito através de Colonoscopia (a cada 10 anos) ou Pesquisa de Sangue Oculto nas Fezes (FIT) anualmente, reservando a colonoscopia para os casos positivos.
- Risco Aumentado (Histórico Familiar): Pacientes com parente de 1º grau com CCR ou adenoma avançado devem iniciar o rastreio aos 40 anos, ou 10 anos antes da idade de diagnóstico do familiar mais jovem (o que ocorrer primeiro).
- Alto Risco (Síndromes Hereditárias e DII):
- PAF (Polipose Adenomatosa Familiar): Rastreio inicia aos 10-12 anos de idade com retossigmoidoscopia. A colectomia profilática é a regra.
- Síndrome de Lynch (HNPCC): Colonoscopia anual ou bienal a partir dos 20-25 anos.
- Doenças Inflamatórias Intestinais (Retocolite Ulcerativa e Crohn): Rastreio intensivo com biópsias seriadas após 8 anos de doença ativa devido ao risco de displasia secundária à inflamação crônica.
Pontos-Chave para a Prática Diária
- Idade de Início: Atualize-se sobre a mudança paradigmática do início do rastreamento para os 45 anos na população de risco habitual.
- Polipectomia é Prevenção: A remoção endoscópica de um adenoma tubular (polipectomia, mucosectomia ou ESD) não é apenas um procedimento diagnóstico; é um ato cirúrgico profilático que salva vidas.
- História Clínica: A anamnese detalhada sobre o histórico oncológico familiar é o teste genético mais barato e eficaz à disposição do médico. Nunca negligencie a construção do heredograma.
Conclusões Aplicadas
A cirurgia oncológica colorretal atingiu patamares de excelência técnica com a laparoscopia e a cirurgia robótica. No entanto, o triunfo definitivo do cirurgião do aparelho digestivo não reside na ressecção de grandes massas tumorais, mas sim na sua prevenção. A atuação ativa do especialista na conscientização dos pacientes, na solicitação rigorosa de exames de rastreio nos prazos adequados e na execução meticulosa de colonoscopias profiláticas é o que verdadeiramente altera a curva epidemiológica desta doença devastadora no Brasil e no mundo.
“As nações ocidentais estão cavando suas próprias sepulturas com os próprios dentes. (…) Se você tem um chão inundado por uma torneira aberta, de nada adianta passar um esfregão sem antes fechar a torneira.” — Denis Parsons Burkitt, renomado cirurgião e pesquisador, sobre a importância da dieta e da prevenção nas doenças do trato gastrointestinal.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
AVALIAÇÃO PRÉ-OPERATÓRIA
MEDICINA BASEADA EM EVIDÊNCIA_AVALIAÇÃO PRÉ_OPERATÓRIA

O médico CIRURGIÃO realiza a avaliação pré-operatória e define a necessidade de avaliação complementar, considerando a otimização das condições clínicas do paciente e a realização de exames complementares. Pacientes hígidos, com idade inferior a 40 anos, sem fatores de risco detectados na anamnese e no exame físico, a serem submetidos a cirurgias de pequeno porte, após a avaliação clínica básica poderão ser encaminhados à cirurgia após avaliação do Anestesiologista. Porém, nos casos em que o paciente tenha alguma comorbidade, idade maior de 60 anos, estado físico ASA II ou acima, obesidade, dependência funcional ou cirurgia de médio ou grande porte, estará indicado avaliação pré-operatória mais pormenorizada .
Colostomia Temporária: Quando está indicada a cirurgia de reversão?
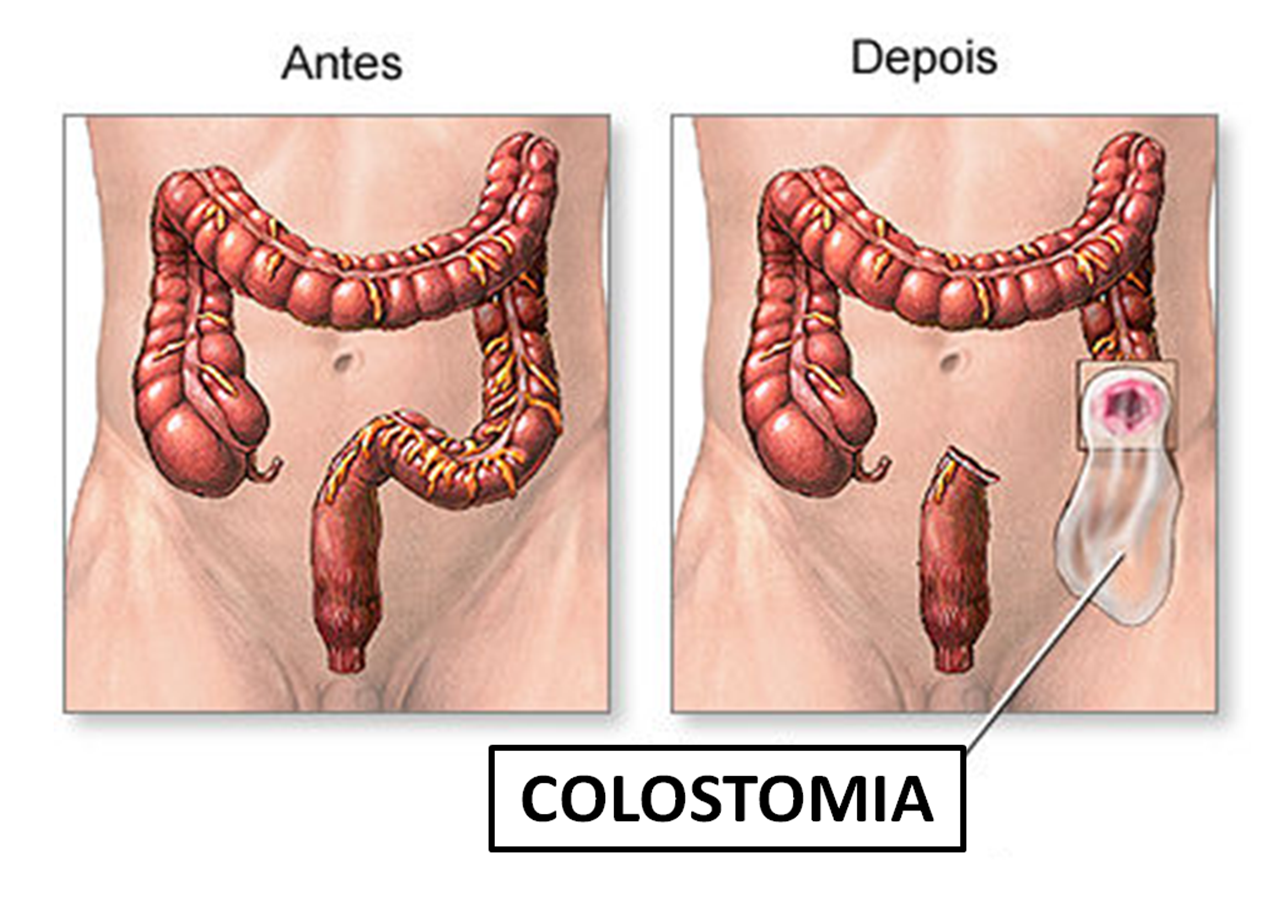
I. INTRODUÇÃO
Apesar de uma diminuição global nas últimas décadas do número de realizações de colostomias temporárias, esta ainda é uma técnica cirúrgica de grande importância no arsenal de opções terapêuticas do CIRURGIÃO DIGESTIVO & COLOPROCTOLOGISTA.
II. EVENTOS ADVERSOS RELACIONADOS
As colostomias, também conhecidas como ostomias, geralmente realizadas em caráter de urgência são desagradáveis para os pacientes e podem trazer uma série de eventos adversos pela sua presença, em especial o risco de infecção de parede abdominal, prolapso (saída) do intestino pela colostomia, oclusão intestinal e as hérnias (enfraquecimento da parede abdominal) para-estomais (ao redor da colostomia), variando a incidência desses eventos adversos em até 60% dos pacientes.
III. RECONSTRUÇÃO DO TRÂNSITO INTESTINAL
Até o momento não se encontra consenso na literatura médica em relação ao tempo ideal de fechamento de uma colostomia temporária. O período clássico de 8 a 12 semanas, encontrado na maioria das publicações, deve ser analisado com grande senso crítico. Os trabalhos científicos especializados identificam taxas de eventos adversos relacionados a cirurgia de fechamento da colostomia ou reconstrução do trânsito intestinal extremamente variadas, com índices que vão de 10% até quase 50% dos casos. O que podemos identificar a partir destes dados é que as cirurgias de decolostomias (cirurgia de reversão de colostomia) são cirurgias complexas e de difícil comparação entre os casos individuais em virtude da especificidade das indicações clínicas. Contudo os fatores inerentes ao próprio paciente, tais como:
1. idade (acima de 60 anos);
2. comorbidades associadas (presença de Diabetes e Hipertensão Arterial);
3. uso crônico de medicações (tais como Corticóides);
4. grau de desnutrição (Albumina sérica menor que 3,0 g/dl); e
5. doença de base que levou a cirurgia de colostomia exercem influência direta no aumento da morbidade (taxa de eventos adversos) dessas operações.
Desta forma, uma diverticulite aguda complicada, um tumor de cólon obstrutivo, uma lesão colônica por projétil de arma de fogo ou arma branca, ou ainda uma perfuração durante um exame endoscópico provocam, dependendo do paciente, respostas metabólicas e endócrinas variáveis, promovendo também efeitos diversos no processo de cicatrização das feridas no pós-operatórios. Portanto quando da programação das cirurgias de restituição do trânsito intestinal uma das avaliações clínicas de grande importância é a total recuperação do trauma cirúrgico anterior que levou a realização da colostomia que é peculiar de paciente para paciente.
IV. AVALIAÇÃO PRÉ-OPERATÓRIA
A programação do fechamento da colostomia através da cirurgia de DECOLOSTOMIA é realizada pela avaliação do estado clínico atual do paciente, assim também como a condição em que se encontram os segmentos intestinais envolvidos, que são apreciados pelos exames radiológicos contrastados (ENEMA OPACO – TRÂNSITO INTESTINAL) e endoscópicos (COLONOSCOPIA) da porção intestinal a ser reconstruída. Outra avaliação importante é que, do ponto de vista técnico, colostomias feitas em caráter de urgência e a presença de aderências intra-abdominais podem resultar na necessidade de ressecções adicionais de segmentos intestinais.
Técnicas de Reconstrução do Trânsito Intestinal
- Anastomose Colorretal
Este procedimento consiste na reconexão do cólon ao reto, permitindo que as fezes sejam eliminadas pelo ânus. Trata-se de uma técnica indicada para determinados pacientes, dependendo das condições específicas e da avaliação do cirurgião. - Rebaixamento do Cólon com Anastomose Coloanal
Essa técnica envolve o rebaixamento de uma parte do cólon e sua conexão direta ao canal anal. É uma alternativa recomendada em casos específicos. A utilização de ferramentas como a manometria anorretal pode auxiliar na indicação dessa abordagem. - Exteriorização do Reto e Anastomose em Segundo Tempo
Em situações em que a cirurgia inicial envolveu a remoção do reto, o cirurgião pode optar por exteriorizar o cólon. Posteriormente, em um segundo procedimento cirúrgico, realiza-se a anastomose entre o canal anal ou reto e o cólon restante, restabelecendo o trânsito intestinal.
Observação Importante
A escolha da técnica mais adequada é altamente individualizada, considerando as condições específicas do paciente, bem como a experiência e o julgamento técnico do cirurgião. Devido à complexidade dessas intervenções, tais procedimentos geralmente são conduzidos por profissionais especializados em CIRURGIA DO APARELHO DIGESTIVO & COLOPROCTOLOGIA.
V. PROGNÓSTICO
A cirurgia de reconstrução do trânsito intestinal após colostomia é um procedimento cirúrgico complexo com expressiva morbimortalidade. Os eventos adversos mais comuns da cirurgia de reversão de colostomia são as INFECÇÕES e os VAZAMENTOS DA ANASTOMOSE (FÍSTULAS). Os resultados da cirurgia de reconstrução intestinal segundo Gomes da Silva (2010) foram: tempo operatório médio de 300 minutos (variando de 180 a 720 minutos); a reconstrução do trânsito intestinal foi alcançado em 93% dos casos; a fístula anastomótica ocorreu em 7% e a infecção de sítio cirúrgico em 22%. A taxa de mortalidade, neste estudo foi de 3,4% ocorrendo principalmente por sepse abdominal ocasionada pela fístula. Dentre os fatores relacionados ao insucesso na reconstrução da colostomia a Hartmann observou-se associação significativa com a tentativa prévia de reconstrução (p = 0,007), a utilização prévia de quimioterapia (p = 0,037) e o longo tempo de permanência da colostomia (p = 0,025).
Referências: Fonseca et al. ABCD, 2017. & Silva et al. ABCD, 2010.
VEJA AQUI ONDE FAZER UMA AVALIAÇÃO ESPECIALIZADA E RECEBER UMA SEGUNDA OPINIÃO
Mais informações: Associação Brasileira de Apoio aos Ostomizados
Safe Surgery Save Lives

Evento Adverso (EA) é definido de acordo com a International Classification for Patient Safety proposta pela World Alliance for Patient Safety da Organização Mundial de Saúde (OMS) como incidente que resulta em dano (harm) ao paciente. Incidente definido como evento ou circunstância que poderia ter causado ou que resultou desnecessariamente em dano ao paciente e evento como algo que acontece com ou envolve o paciente. Os eventos adversos (EAs) têm estimativa de ocorrência em 4 a 16% de todos os pacientes hospitalizados, sendo que mais de metade nos cuidados cirúrgicos, dos quais acima de 50% são evitáveis. A ocorrência de EAs é considerada um problemade importância internacional sendo crescente o envolvimento de pesquisadores,profissionais de saúde e gestores de saúde na avaliação de EAs e inúmeras as instituições,redes de relacionamento e websites referentes ao tema.
Em 2004, expressando a preocupação mundial com a segurança de pacientes, foi criada pela OMS a World Alliance for Patient Safety tendo como elemento central a formulação do Global Patient Safety Challenge, que engloba temas representativos dos principais aspectos dos riscos relacionados com a assistência à saúde, considerados relevantes para os países membros da OMS. O primeiro tema selecionado foi infecção associada à prestação de serviço em saúde, seguido de segurança dos cuidados cirúrgicos,tendo como objetivo prevenir erros, evitar danos e salvar vidas. O número de cirurgias de maior porte realizadas anualmente no mundo foi estimado pela OMS em 234 milhões, o que corresponde a uma cirurgia para cada 25 pessoas.
Cirurgia de maior porte inclui qualquer procedimento realizado na sala de cirurgia envolvendo incisão, excisão, manipulação, ou sutura de tecido que geralmente requer anestesia geral ou regional, ou sedação profunda para controlar a dor. Em países industrializados complicações ocorrem em 3 – 16% dos procedimentos cirúrgicos realizados em pacientes internados, com taxa de mortalidade de 0,4 – 0,8%. Estudos realizados em países em desenvolvimento estimam uma taxa de mortalidade de 5 a 10% em pacientes submetidos à cirurgia de maior porte. A segurança em cirurgia emerge como importante preocupação para a saúde pública global. Cirurgia é um dos mais complexos e caros serviços prestados pelos sistemas de saúde.
Nos países em desenvolvimento , o mau estado da infraestrutura e dos equipamentos; os problemas quanto ao suprimento e à qualidade de medicamentos e de material médico-cirúrgico; as falhas na gestão da organização e no controle de infecção; o desempenho insatisfatório dos profissionais devido à baixa motivação ou à deficiência na capacitação técnica; as falhas no correto diagnóstico pré-operatório; as deficiências na consulta pré-anestésica, e o subfinanciamento dos custos operacionais dos serviços de saúde, tornam a probabilidade de ocorrência de eventos adversos muito maior do que em países industrializados.
Veja alguns dados:
World Alliance for Patient Safety : forward programme. World Health Organization 2004, apud: Harvard Medical Practice Study in 1991
Eventos Adversos na Clínica Cirúrgica
EVENTOS ADVERSOS # COMPLICAÇÕES

Introdução
O termo “Evento Adverso (EA)” cirúrgico é relativamente novo, mas o conceito de monitoramento dos resultados cirúrgicos, incluindo complicações pós-operatórias, é muito antigo. Desde 1732, existem referências a sistemas de coleta de informações hospitalares. Na Grã-Bretanha, estatísticas vitais datam de 1838, e já em 1850, a associação entre higiene das mãos e a transmissão de infecções foi estabelecida. Em 1854, os riscos de má higiene nos hospitais foram destacados, e em 1910, Ernest Codman defendeu a avaliação rotineira dos resultados negativos em cirurgias para melhorar a qualidade da assistência. Nos anos 1990, o interesse em erros e danos relacionados à saúde cresceu, mudando o foco das pesquisas para estratégias de enfrentamento e uma abordagem sistêmica ou organizacional.
Epidemiologia
Os EAs cirúrgicos contribuem significativamente para a morbidade pós-operatória, e sua avaliação e monitoramento frequentemente são imprecisos. Com a redução do tempo de permanência hospitalar e o aumento do uso de técnicas cirúrgicas inovadoras, especialmente minimamente invasivas e endoscópicas, a eficiência no monitoramento dos eventos adversos torna-se crucial. Revisões recentes identificaram que os EAs são desfavoráveis, indesejáveis, prejudiciais, impactam o paciente e estão associados ao processo de assistência à saúde, mais do que a um processo natural de doenças. A análise dos EAs é complexa devido à variabilidade dos sistemas de registro e às diversas definições na literatura científica para complicações pós-operatórias.
Custo e Efeitos de Medicina Legal
As complicações pós-operatórias resultam da interação de fatores dependentes do paciente, sua enfermidade e a atenção à saúde recebida. O estudo dos EAs cirúrgicos é relevante pela sua frequência, impacto considerável sobre a saúde dos pacientes e repercussão econômica no gasto social e sanitário. Além disso, os EAs servem como instrumento de avaliação da qualidade da assistência. Eventos adversos evitáveis, suscetíveis a intervenções de prevenção, são de maior interesse para a saúde pública. EAs cirúrgicos estão relacionados a acidentes intra-operatórios, complicações pós-operatórias imediatas ou tardias e ao fracasso da intervenção cirúrgica.
Nos Estados Unidos, um estudo em hospitais de Colorado e Utah calculou uma taxa de incidência de 1,9% para pacientes internados, e 3,0% para pacientes submetidos a cirurgia ou parto, com 54% dos EAs considerados evitáveis. Em 5,6% dos casos, os EAs resultaram em óbito. Na Austrália, a prevalência de internações cirúrgicas associadas a um EA foi de 21,9%, com 47,6% dos EAs classificados como altamente evitáveis. Na Espanha, um estudo em cirurgias de parede abdominal encontrou complicações em 16,32% dos pacientes.
Diferença entre Complicação e Evento Adverso
Complicações pós-operatórias surgem da interação entre fatores do paciente, da doença e da atenção recebida. Eventos Adversos, por outro lado, são desfavoráveis, indesejáveis e prejudiciais, resultantes do processo de assistência à saúde. Embora ambos afetem a recuperação, os EAs são frequentemente evitáveis com intervenções preventivas.
Conclusão
A segurança em cirurgia no Brasil é preocupante. Em 2003, 52,5% dos hospitais inspecionados pelo Conselho Regional de Medicina de São Paulo apresentaram condições físicas inadequadas. Hospitais de pequeno porte, que representam 62% dos estabelecimentos, enfrentam desafios significativos em termos de complexidade e densidade tecnológica.
Como Ernest Codman sabiamente afirmou: “A melhoria na assistência médica só pode ser alcançada com a análise sistemática dos resultados”. Esta frase histórica ressoa ainda hoje, destacando a importância da avaliação e monitoramento dos EAs cirúrgicos para a melhoria contínua da qualidade e segurança na assistência à saúde.
Tratamento Cirúrgico do HEMANGIOMA HEPÁTICO

Introdução
O hemangioma é o tumor hepático mais comum, identificado em 5% a 7% das necropsias. Sua incidência é maior entre a terceira e a quinta décadas de vida, com prevalência nas mulheres. Este tumor pode aumentar de tamanho durante a gravidez e com o uso de estrogênios.
Conceito
Hemangiomas hepáticos são tumores benignos dos vasos sanguíneos do fígado. Apesar de sua causa não estar completamente esclarecida, há indícios do papel dos hormônios sexuais em seu desenvolvimento. Observações como a presença de receptores de estrogênio em alguns hemangiomas e o aumento de tamanho durante a puberdade, gravidez e uso de anticoncepcionais sugerem essa relação.
Epidemiologia
A maioria dos hemangiomas hepáticos é única e mede menos de 4 cm de diâmetro, com apenas 10% sendo múltiplos e podendo alcançar até 27 cm. Hemangiomas gigantes são definidos como aqueles com mais de 4 cm de diâmetro. Em geral, o tamanho da maioria dos hemangiomas permanece inalterado ao longo do tempo.
Diagnóstico
O diagnóstico de hemangioma hepático é geralmente realizado por exames de imagem, como tomografia computadorizada e ressonância magnética. Esses exames identificam padrões típicos de impregnação nodular periférica e descontínua, com aumento gradual da impregnação. Na ressonância magnética, os hemangiomas tipicamente apresentam um sinal alto nas sequências ponderadas em T2. A cintilografia com hemácias marcadas também é precisa para hemangiomas maiores que 2 cm, mas raramente necessária.
Indicações de Tratamento Cirúrgico
A maioria dos hemangiomas não requer tratamento. Não há evidências para interromper o uso de anticoncepcionais hormonais ou evitar a gravidez em pacientes com hemangioma, mesmo em casos de tumores gigantes. Complicações são raras, mas incluem inflamação, coagulopatia, sangramento e compressão de estruturas vizinhas. O tratamento cirúrgico é indicado apenas em casos de sintomas significativos, crescimento tumoral, síndrome de Kasabach-Merritt, ou quando não é possível excluir malignidade.
Conclusões
Hemangiomas hepáticos, em sua maioria, são assintomáticos e não necessitam de intervenção. O tratamento cirúrgico, apesar de raramente necessário, é realizado em casos selecionados para evitar complicações maiores. A decisão cirúrgica deve ser cuidadosa, considerando os riscos operatórios. Como disse William Osler, “A prática da medicina é uma arte, não um comércio; uma vocação, não um negócio; uma chamada em que seu coração será exercitado igualmente com sua cabeça.”
Tratamento Cirúrgico da COLECISTITE AGUDA
I. INTRODUÇÃO
Os cálculos de vesícula (COLELITÍASE) estão presentes em mais de 10% da população ocidental e esta incidência aumenta com a idade. A colelitíase é a doença do aparelho digestivo com maior número de indicação cirúrgica. Anualmente, cerca de 200.000 colecistectomias são realizadas nos Brasil. Os fatores de risco para o surgimento dos cálculos são: obesidade, diabetes mellitus, uso de estrogênio, gravidez, doença hemolítica, hereditariedade e cirrose. Acomete principalmente as mulheres na idade reprodutiva.
São várias as complicações da colelitíase, entre elas:
1. COLECISTITE AGUDA
2. PANCREATITE AGUDA
3. COLEDOCOLITÍASE
4. FÍSTULAS INTERNAS
5. CÂNCER DA VESÍCULA
VEJA AQUI ONDE REALIZAR A CIRURGIA DE COLECISTECTOMIA COM CIRURGIÃO DO APARELHO DIGESTIVO
II. FISIOPATOLOGIA
A colecistite aguda é uma doença comum em emergências em todo o mundo. Na maioria dos casos, é causada pela inflamação da parede da vesícula secundária à impactação de um cálculo no ducto cístico obstruindo-o, o que causa uma crise repentina de dor abdominal, conhecido como ABDOME AGUDO.
Colecistite litiásica
A colecistite aguda está associada à colelitíase em mais de 90% dos casos. O quadro ocorre devido à obstrução do ducto cístico por um cálculo. Se a obstrução continua, a vesícula se distende e suas paredes tornam-se edematosas. O processo inflamatório inicia-se com espessamento da parede, eritema e hemorragia subserosa. Surgem hiperemia e áreas focais de necrose. Na maioria dos casos, o cálculo se desloca e o processo inflamatório regride. Se o cálculo não se move, o quadro evolui para isquemia e necrose da parede da vesícula em cerca de 10% dos casos. A formação de abscesso e empiema dentro da vesícula é conhecida como colecistite aguda gangrenosa. Com a infecção bacteriana secundária, principalmente por anaeróbios, há formação de gás que pode ocorrer dentro ou na parede da vesícula. Esse é um quadro mais grave conhecido com colecistite enfisematosa.
A colecistite aguda também pode ocorrer sem a presença de cálculos em cerca de 5% dos casos. Tem uma evolução mais rápida e frequentemente evolui para gangrena, empiema ou perfuração. Ocorre em pessoas idosas ou em estado crítico após trauma, queimaduras, nutrição parenteral de longa data, cirurgias extensas, sepses, ventilação com pressão positiva e a terapia com opioides também parece estar envolvida. A etiologia é confusa, mas a estase, a isquemia, a injúria por reperfusão e os efeitos dos mediadores pró-inflamatórios eicosanoides são apontados como causas.
VEJA AQUI ONDE REALIZAR A CIRURGIA DE COLECISTECTOMIA COM CIRURGIÃO DO APARELHO DIGESTIVO
III. QUADRO CLÍNICO
O quadro se inicia com uma cólica biliar caracterizada como dor no hipocôndrio direito com irradiação para escápula direita e região epigástrica. Como sintoma mais comum, o paciente apresenta dor e pressão no hipocôndrio direito, mais duradoura das que nas crises de cólica biliar a que ele frequentemente se refere. Esse é o primeiro sinal de inflamação da vesícula. A dor pode intensificar-se quando a pessoa respira profundamente e muitas vezes estende-se à parte inferior da escápula direita e à região epigástrica. A febre, assim como náuseas e vômitos, que podem ser biliosos, são habituais em 70% dos pacientes. A febre alta, os calafrios e a distensão abdominal com diminuição da peristalse costumam indicar a formação de um abscesso, gangrena ou perfuração da vesícula biliar. Nestas condições, torna-se necessária a cirurgia de urgência. A icterícia pode indicar coledocolitíase ou compressão externa do colédoco pela vesícula inflamada.
IV. AVALIAÇÃO DIAGNÓSTICA
O hemograma habitualmente apresenta leucocitose com desvio para esquerda. O hepatograma está alterado com elevação das transaminases, da fosfatase alcalina, bilirrubinas e amilase. A hiperbilirrubinemia pode ser devido à compressão extrínseca pelo processo inflamatório grave, pela coledocolitíase ou pela síndrome de Mirizzi, que é causada pela impactação de um cálculo no infundíbulo que pode fistulizar para o colédoco e obstruí-lo. A hiperamilasemia pode ocorrer devido à obstrução do ducto pancreático levando à pancreatite concomitante.
A ultrassonografia é o exame inicial e permite a identificação de alterações que não são visíveis no exame físico e permite uma classificação. É considerado o exame “ouro” nesses casos. Tem alta sensibilidade para a detecção de cálculos e o espessamento da parede que é considerado anormal quando maior que 4 mm . Também pode haver visualização de líquido perivesicular, distensão da vesícula, cálculos impactados no infundíbulo e o sinal de Murphy ultrassonográfico. Este sinal é relatado quando, após a identificação da vesícula inflamada, o ultrassonografista comprime o abdômen na topografia da mesma com o transdutor e o paciente refere dor intensa. A ultrassonografia laparoscópica intraoperatória tem sido usada no lugar da colangiografia no diagnóstico da coledocolitíase.
VEJA AQUI ONDE REALIZAR A CIRURGIA DE COLECISTECTOMIA COM CIRURGIÃO DO APARELHO DIGESTIVO
A colecistectomia (retirada cirúrgica da vesícula biliar) é o tratamento definitivo dos pacientes com colelitíase associada à colecistite aguda. Em geral, após sua hospitalização e preparo pré-operatório (hidratação, analgésicos e antibióticos) realiza-se a cirurgia nas primeiras 72 horas de início do quadro. A colecistectomia videolaparoscópica é o tratamento de escolha na colecistite aguda litiásica e alitiásica. A cirurgia videolaparoscópica tem como característica básica diminuir a agressão e consequente trauma cirúrgico. Tem sido demonstrada, nesta abordagem, uma menor repercussão orgânica, representada por menor reação metabólica, inflamatória e imunológica quando comparada a uma cirurgia aberta. Isto representa um grande benefício para o paciente, principalmente àqueles mais graves, já com comprometimento de órgãos e sistemas, mesmo nos pacientes com idade avançada. A taxa de conversão de cirurgia videolaparoscópica para cirurgia aberta é maior nos casos de colecistopatia calculosa aguda do que na crônica, podendo ocorrer até em 30% dos casos. O fator que mais dificulta a realização do procedimento videolaparoscópico é a alteração anatômica ou se não há uma adequada visualização das estruturas. A colecistite aguda associada ao sexo masculino, IMC > 30, idade superior a 60 anos, cirurgia abdominal prévia, ASA elevado, espessamento da vesícula maior que 4 mm e diabetes são considerados fatores de risco para a conversão para a cirurgia aberta.
VI. CONCLUSÃO
A colecistite aguda continua sendo uma doença com a qual o cirugião se depara frequentemente. A cirurgia videolaparoscópica veio mudar o manuseio e evolução dos pacientes tornando o pós-operatório mais curto e menos doloroso. A literatura médica tem levado alguns cirurgiões a retardarem a indicação cirúrgica, entretanto novos trabalhos, inclusive com análise de medicina baseada em evidências, têm demonstrado que a intervenção na primeira semana do início do quadro é a melhor conduta.
VEJA AQUI ONDE REALIZAR A CIRURGIA DE COLECISTECTOMIA COM CIRURGIÃO DO APARELHO DIGESTIVO
PERIOPERATIVE MEDICINE
ARTICLE REVIEW_ PERIOPERATIVE MANAGEMENT
The outcome of patients who are scheduled for gastrointestinal surgery is influenced by various factors, the most important being the age and comorbidities of the patient, the complexity of the surgical procedure and the management of postoperative recovery. To improve patient outcome, close cooperation between surgeons and anaesthesiologists (joint risk assessment) is critical. This cooperation has become increasingly important because more and more patients are being referred to surgery at an advanced age and with multiple comorbidities and because surgical procedures and multimodal treatment modalities are becoming more and more complex. The aim of this review is to provide clinicians with practical recommendations for day-to-day decision-making from a joint surgical and anaesthesiological point of view. The discussion centres on gastrointestinal surgery specifically.

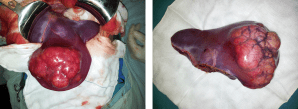

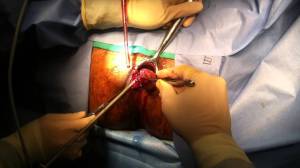
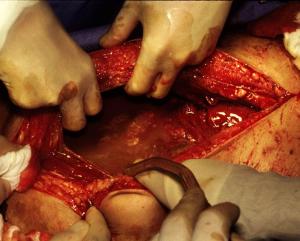
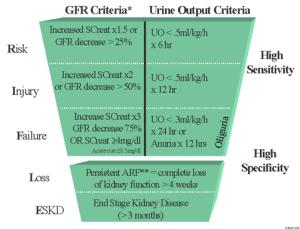


 The risk of complications and mortality in bariatric surgery is associated with certain factors that are common to other patients and procedures, including age above 65 years, the presence of associated diseases (cardiovascular and pulmonary disease, chronic renal failure, liver cirrhosis, etc.), prior abdominal surgery, and the experience of the surgeon and the institution, especially concerning the ability to make an early diagnosis and address complications. The surgical complications observed in the early postoperative period following surgeries performed to treat severe obesity are similar to those associated with other major surgeries of the gastrointestinal tract. However, given the more frequent occurrence of medical comorbidities (such as diabetes, arterial hypertension, and sleep apnea), as well as the difficulty in making an early diagnosis of the complications (due to limitations of the clinical abdominal workup and imaging methods, such as ultrasonography and computed tomography, particularly in highly obese patients with body mass indices >50 kg/m²), these patients require special attention in the early post operative follow-up. Pulmonary thromboembolism, a complication associated with bariatric surgery, also requires greater attention from the medical team given the high mortality rate associated with this condition. Early diagnosis and appropriate treatment of these complications are directly associated with a greater probability of control.
The risk of complications and mortality in bariatric surgery is associated with certain factors that are common to other patients and procedures, including age above 65 years, the presence of associated diseases (cardiovascular and pulmonary disease, chronic renal failure, liver cirrhosis, etc.), prior abdominal surgery, and the experience of the surgeon and the institution, especially concerning the ability to make an early diagnosis and address complications. The surgical complications observed in the early postoperative period following surgeries performed to treat severe obesity are similar to those associated with other major surgeries of the gastrointestinal tract. However, given the more frequent occurrence of medical comorbidities (such as diabetes, arterial hypertension, and sleep apnea), as well as the difficulty in making an early diagnosis of the complications (due to limitations of the clinical abdominal workup and imaging methods, such as ultrasonography and computed tomography, particularly in highly obese patients with body mass indices >50 kg/m²), these patients require special attention in the early post operative follow-up. Pulmonary thromboembolism, a complication associated with bariatric surgery, also requires greater attention from the medical team given the high mortality rate associated with this condition. Early diagnosis and appropriate treatment of these complications are directly associated with a greater probability of control.