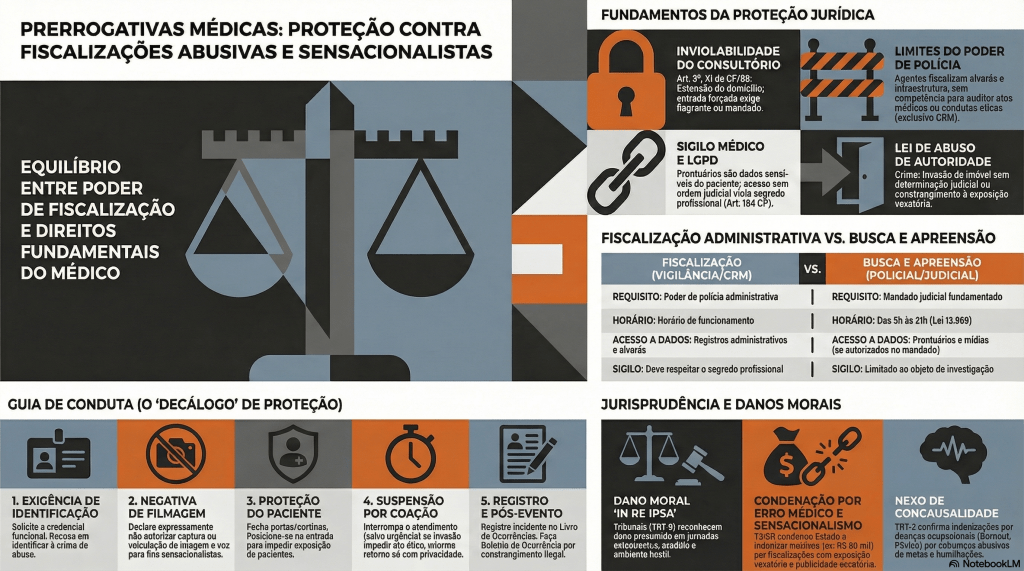
Proteção Médica contra Fiscalizações Invasivas e Sensacionalistas
No atual cenário das unidades de urgência e emergência, observa-se uma crescente e indevida ingerência de agentes externos que, sob o pretexto do escrutínio midiático, submetem o corpo clínico — em especial os profissionais em início de carreira — a constrangimentos e intimidações. Tais condutas, frequentemente pautadas pelo sensacionalismo digital, não apenas desestabilizam o ato médico, como violam preceitos basilares da Bioética e do Direito, notadamente o sigilo profissional e a dignidade do paciente. Diante desse panorama de vulnerabilidade técnica e jurídica, o presente Decálogo de Proteção Profissional Médica emerge como um instrumento essencial de salvaguarda, transpondo a dogmática jurídica para a práxis cotidiana. Este guia oferece diretrizes objetivas de conduta e interlocução, permitindo ao médico exercer sua autonomia com o rigor técnico, a polidez e a segurança jurídica que a complexidade do ambiente hospitalar exige.

I. Manutenção da Postura Ética e Prevenção do Conflito O médico deve manter o controle emocional, adotando postura polida e técnica. É imperativo evitar qualquer embate físico ou agressão verbal com os invasores, neutralizando o objetivo sensacionalista da ação.
- Fundamentação Jurídica e Ética: Código de Ética Médica (Resolução CFM nº 2.217/2018), Capítulo I, Inciso II; Art. 5º, inciso X, da Constituição Federal.
- O que fazer e o que falar: Respire fundo, cruze os braços ou mantenha as mãos visíveis (evitando qualquer gesto que possa ser interpretado como agressão). Não tente tomar o celular ou a câmera do invasor.
- Fala: “Boa noite/dia. Por favor, peço que mantenham a calma e baixem o tom de voz. Estamos em um ambiente hospitalar de respeito e cuidado.”
II. Exigência de Identificação e Recusa Expressa de Filmagem O profissional deve solicitar a identificação da autoridade e declarar, em bom tom (para que fique registrado na própria gravação), que não autoriza o uso, captura ou veiculação de sua imagem e voz.
- Fundamentação Jurídica e Ética: Art. 5º, inciso X, da Constituição Federal; Art. 20 do Código Civil.
- O que fazer e o que falar
- Ação: Olhe diretamente para a pessoa (e não para a câmera). Adote um tom de voz firme, porém sem gritar.
- Fala: “Sou o médico plantonista responsável neste momento. Por gentileza, identifiquem-se. Deixo expressamente claro, e peço que fique registrado em sua gravação, que não autorizo a captura, o uso ou a veiculação da minha imagem e da minha voz.”
III. Acionamento Imediato da Cadeia de Comando Institucional A gestão do fluxo de pessoas não é atribuição do médico assistente. Deve-se delegar a um membro da equipe (enfermagem/técnicos) o acionamento urgente da Segurança Patrimonial, da Chefia de Plantão e do Diretor Técnico da instituição.
- Fundamentação Jurídica e Ética: Resolução CFM nº 2.147/2016.
- O que fazer e o que falar
- Ação: Vire-se calmamente para um colega da equipe multidisciplinar e delegue a função, sem dar as costas totalmente aos invasores.
- Fala: “Enfermeiro(a) [Nome], por favor, acione imediatamente a segurança do hospital, a chefia de plantão e comunique o Diretor Técnico de que temos pessoas não autorizadas e com câmeras no setor.”
IV. Isolamento Físico e Proteção da Intimidade do Paciente A prioridade máxima é salvaguardar o paciente em atendimento. O médico deve fechar portas, fechar cortinas e posicionar-se fisicamente na entrada de consultórios ou enfermarias, bloqueando o acesso visual das câmeras aos enfermos.
- Fundamentação Jurídica e Ética: Art. 5º, inciso X, da Constituição Federal; Art. 73 do Código de Ética Médica.
- O que fazer e o que falar:
- Ação: Caminhe de forma decidida até a porta do consultório ou enfermaria, feche-a e coloque-se à frente dela como um obstáculo físico pacífico.
- Fala: “Os senhores não podem entrar aqui. Temos pacientes desnudos e vulneráveis em atendimento. Exijo que respeitem a privacidade e a intimidade dos enfermos.”
V. Evocação Expressa do Sigilo Médico e Profissional Diante da tentativa de invasão em áreas assistenciais, o médico deve declarar que está sob o imperativo legal do sigilo e que a presença de terceiros não autorizados munidos de câmeras configura quebra indireta de confidencialidade.
- Fundamentação Jurídica e Ética: Art. 154 do Código Penal Brasileiro; Art. 73, parágrafo único, do Código de Ética Médica.
- O que fazer e o que falar:
- Ação: Ignore perguntas médicas ou clínicas sobre qualquer paciente (“por que fulano está esperando?”, “o que aquele paciente tem?”).
- Fala: “Como médico, sou regido pela lei do sigilo absoluto. Não responderei a perguntas sobre casos clínicos e não permitirei filmagens nesta área, pois isso configura crime de quebra de confidencialidade médica.”
VI. Negativa Peremptória de Acesso a Prontuários Médicos O profissional deve negar a entrega, leitura ou auditoria de prontuários por parte de parlamentares ou fiscais não vinculados aos Conselhos de Medicina, informando que o documento pertence exclusivamente ao paciente.
- Fundamentação Jurídica e Ética: Resolução CFM nº 1.638/2002; Art. 89 do Código de Ética Médica.
- O que fazer e o que falar:
- Ação: Feche pastas de prontuários físicos ou bloqueie a tela do computador/sistema eletrônico.
- Fala: “O prontuário é um documento legal e de propriedade exclusiva do paciente. Sem a autorização expressa e por escrito dele, ou sem ordem judicial, os senhores não terão acesso a nenhum documento médico.”
VII. Esclarecimento dos Limites da Competência Fiscalizatória O médico deve esclarecer à autoridade que o exercício de “poder de polícia” parlamentar se restringe à infraestrutura e à administração pública, não abrangendo a fiscalização do ato médico ou da conduta ética, que possuem foro específico.
- Fundamentação Jurídica e Ética: Lei nº 3.268/1957.
- O que fazer e o que falar:
- Ação: Mantenha a compostura caso o político tente dar “ordens” ou fazer “ameaças” usando o cargo.
- Fala: “Reconheço o seu cargo, mas o senhor tem competência para fiscalizar a estrutura administrativa. A fiscalização do ato médico e da conduta profissional é prerrogativa exclusiva do Conselho Regional de Medicina (CRM). Por favor, dirija suas demandas ao Diretor da unidade.”
VIII. Suspensão do Atendimento sob Coação (Garantia de Condições Dignas) Caso as câmeras adentrem o recinto de atendimento e os invasores se recusem a sair, o médico deve suspender temporariamente o ato médico — desde que não seja caso de urgência/emergência — informando que só retornará quando a privacidade for restabelecida.
- Fundamentação Jurídica e Ética: Código de Ética Médica, Capítulo II, Inciso IV (Direitos dos Médicos).
- O que fazer e o que falar:
- Ação: Caso invadam a sala de forma ríspida, interrompa a consulta (se não houver risco de morte), sente-se na cadeira, afaste-se do paciente e aguarde em silêncio a retirada dos invasores pela segurança.
- Fala: “Diante da invasão e da coação com câmeras, informo que não possuo condições dignas e éticas para exercer a medicina neste momento. Retomarei o atendimento imediatamente após os senhores se retirarem e a segurança do paciente for garantida.”
IX. Registro Documental Exaustivo do Incidente Tão logo a situação seja normalizada, o médico deve registrar o fato detalhadamente no Livro de Ocorrências do plantão. Caso a invasão tenha prejudicado ou atrasado o atendimento de algum paciente, tal interferência externa deve constar no prontuário do mesmo.
- Fundamentação Jurídica e Ética: Art. 87 do Código de Ética Médica; Art. 299 do Código Penal.
- O que fazer e o que falar:
- Ação: Escreva de forma objetiva, descrevendo fatos (sem adjetivos emocionais). Cite os nomes dos invasores, a recusa em parar de filmar e os horários exatos.
- Fala (orientação mental e à equipe): “Precisamos registrar tudo. Vamos anotar o nome do vereador/político, o horário exato da invasão, o que foi dito e as paralisações geradas no atendimento para colocar no livro do plantão agora mesmo.”
X. Acionamento das Autoridades Policiais e Desagravo Institucional Ao término do plantão, é fundamental registrar Boletim de Ocorrência Policial e enviar comunicação oficial (Ofício) ao Diretor Técnico e ao Conselho Regional de Medicina (CRM) relatando o constrangimento.
- Fundamentação Jurídica e Ética: Decreto-Lei nº 3.688/1941, Art. 42; Art. 150 do Código Penal; Código de Ética Médica, Capítulo II, Inciso V.
- O que fazer e o que falar:
- Ação: Dirija-se a uma delegacia (ou delegacia virtual) e, nos dias subsequentes, contrate um advogado e/ou assessoria jurídica institucional e/ou do sindicato médico.
- Fala (na Delegacia / no Ofício): “Desejo registrar um Boletim de Ocorrência por constrangimento ilegal, perturbação do ambiente de trabalho e quebra tentada de sigilo médico contra o invasor. Solicitarei também, via ofício, o desagravo público junto ao CRM.”
A nossa missão máxima será sempre a defesa da saúde e da dignidade do doente. Que as orientações sirvam para garantir que nenhum profissional permita a usurpação do seu local de trabalho, assegurando que a nobre arte da Medicina seja sempre exercida em condições de absoluta segurança, privacidade e respeito mútuo.
Prof. Dr. Ozimo Gama
Cuidados Perioperatórios na Cirurgia Laparoscópica
Otimizando a Fisiologia e Acelerando a Recuperação no Aparelho Digestivo
Autor: Prof. Dr. Ozimo Gama Categoria: Cuidados Perioperatórios / Cirurgia Laparoscópica / Cirurgia do Aparelho Digestivo Tempo de Leitura: 10 minutos
Introdução
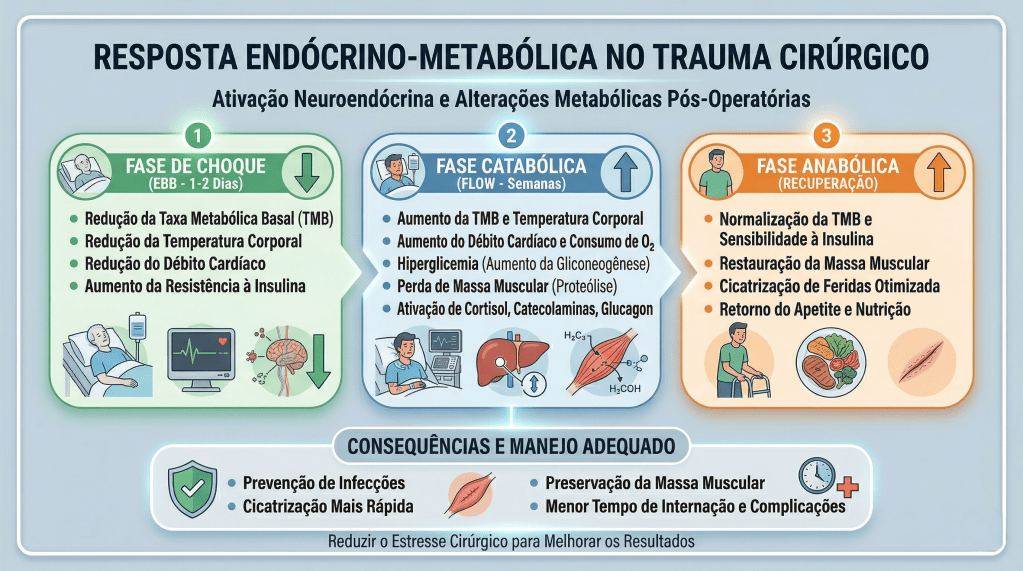
A cirurgia laparoscópica revolucionou a especialidade do aparelho digestivo ao atenuar o trauma cirúrgico, reduzir a resposta inflamatória sistêmica e proporcionar uma recuperação estética e funcional superior. No entanto, para o estudante de medicina, o residente de cirurgia geral e o pós-graduando, é imperativo compreender que incisões milimétricas não isentam o paciente da resposta endócrino-metabólica ao trauma. No Brasil, o Sistema Único de Saúde (SUS) realiza centenas de milhares de procedimentos videolaparoscópicos anualmente, desde colecistectomias até gastrectomias oncológicas complexas. Para maximizar os benefícios da via minimamente invasiva, a excelência no centro cirúrgico deve ser invariavelmente acompanhada por um manejo perioperatório de vanguarda. A transição dos cuidados dogmáticos do passado para protocolos modernos baseados em evidências — como o ERAS (Enhanced Recovery After Surgery) e o Projeto ACERTO (Aceleração da Recuperação Total Pós-Operatória), amplamente adotado e validado em território nacional — é o que define o cirurgião contemporâneo de alta performance.
A Fisiologia do Pneumoperitônio e a Quebra de Paradigmas
O manejo perioperatório na laparoscopia exige um profundo respeito pelas alterações fisiológicas induzidas pelo pneumoperitônio com dióxido de carbono (CO2). A insuflação abdominal eleva a pressão intra-abdominal (usualmente entre 12 e 15 mmHg), acarretando compressão da veia cava inferior, diminuição do retorno venoso, aumento da resistência vascular sistêmica e elevação das pressões das vias aéreas com risco de hipercapnia. A equipe cirúrgico-anestésica deve atuar em sintonia para mitigar estes efeitos.
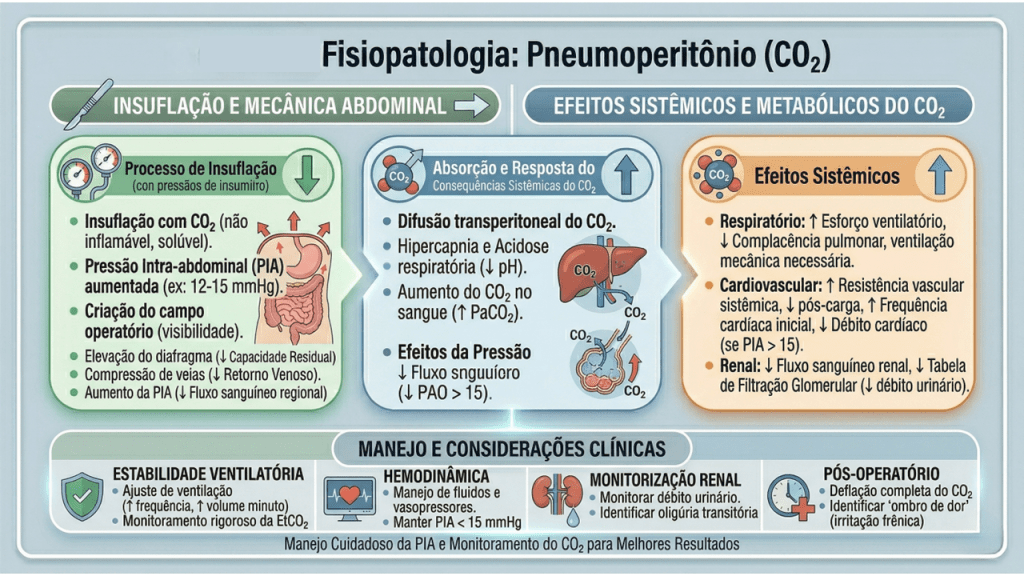
Sob a ótica dos protocolos de aceleração da recuperação, o manejo perioperatório é dividido em três fases cruciais, onde dogmas seculares foram cientificamente derrubados:
- Pré-Operatório (O Fim do Jejum Prolongado): O jejum absoluto de 8 a 12 horas está proscrito. Evidências robustas, corroboradas por dados do Projeto ACERTO no Brasil, demonstram que a oferta de líquidos claros enriquecidos com carboidratos até 2 horas antes da indução anestésica reduz a resistência insulínica pós-operatória, minimiza a perda de massa magra e diminui a ansiedade do paciente.
- Intraoperatório (A Terapia Hídrica Guiada por Metas): A hiper-hidratação venosa, outrora comum, resulta em edema esplâncnico e retardo do esvaziamento gástrico. A fluidoterapia deve ser restritiva ou guiada por metas (avaliando a variação do volume sistólico), garantindo perfusão tecidual sem encharcar o paciente. A analgesia deve ser preemptiva e multimodal, poupadora de opioides.
- Pós-Operatório (Mobilização e Realimentação): O repouso no leito prolongado favorece o tromboembolismo venoso (TEV) e a atelectasia pulmonar. O paciente deve ser encorajado a deambular no mesmo dia da operação.
Aplicação na Cirurgia Digestiva
Na cirurgia do trato gastrointestinal, a aplicação destes cuidados perioperatórios altera drasticamente os desfechos e o tempo de internação:
- Preparo Mecânico do Cólon (PMC): Em cirurgias colorretais laparoscópicas, o uso rotineiro do PMC foi abandonado por grande parte das diretrizes, pois causa desidratação, distúrbios hidroeletrolíticos e não reduz as taxas de deiscência anastomótica ou infecção de sítio cirúrgico (exceto quando associado a antibióticos orais específicos em cirurgias de reto baixo).
- Sondas e Drenos: A utilização profilática de sondas nasogástricas (SNG) e drenos cavitários não encontra mais respaldo na literatura para procedimentos eletivos sem complicações. A SNG prolonga o íleo adinâmico e predispõe a infecções respiratórias. O dreno deve ser uma exceção fundamentada, não a regra.
- Realimentação Precoce: O íleo pós-operatório é inerente à manipulação das alças, mas a dieta por via oral iniciada precocemente (muitas vezes nas primeiras 24 horas) estimula o reflexo gastrocólico, protege a barreira mucosa intestinal contra a translocação bacteriana e acelera a alta hospitalar. Estatísticas brasileiras apontam que a realimentação precoce em ressecções intestinais laparoscópicas reduz o tempo de internação em até 2 a 3 dias.
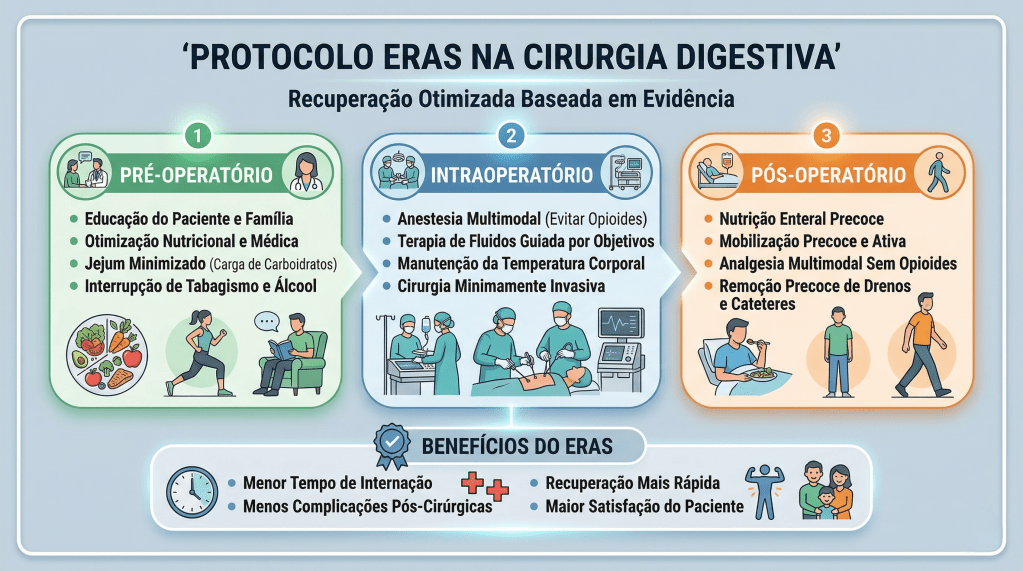
Pontos-Chave
- Avaliação Fisiológica: O pneumoperitônio exige monitorização hemodinâmica rigorosa devido às alterações cardiocirculatórias e ventilatórias.
- Jejum Abreviado: Utilização de maltodextrina a 12,5% até 2 horas antes da cirurgia é uma prática segura e metabolicamente protetora.
- Analgesia Opioid-Sparing: Uso de infiltração dos portais com anestésicos locais, anti-inflamatórios e bloqueios regionais (ex: TAP block) para evitar os efeitos eméticos e obstipantes dos opioides.
- Tromboprofilaxia: O uso de meias elásticas de compressão graduada, compressores pneumáticos intermitentes e heparina de baixo peso molecular é mandatório, dada a estase venosa promovida pela pressão intra-abdominal elevada.
- Racionalização de Dispositivos: Evitar o uso sistemático e prolongado de sondas vesicais de demora (SVD), SNG e drenos cavitários.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
A destreza na dissecção laparoscópica e a precisão das anastomoses intracavitárias perdem parte de seu brilho se o paciente for submetido a um estresse fisiológico não gerenciado. O cirurgião do aparelho digestivo moderno deve compreender que o seu papel transcende a mecânica operatória; ele é o arquiteto da recuperação do paciente. Adoção de protocolos de cuidados perioperatórios como o ACERTO exige uma mudança de cultura institucional e o alinhamento de toda a equipe multidisciplinar (cirurgião, anestesiologista, enfermagem, nutrição e fisioterapia). Ao unirmos a mínima agressão tecidual da videolaparoscopia à máxima otimização metabólica do perioperatório, entregamos não apenas uma cirurgia segura, mas a restituição rápida e plena da qualidade de vida do nosso paciente.
“O principal objetivo da cirurgia moderna não é apenas curar a doença anatômica, mas suprimir a resposta ao trauma cirúrgico, proporcionando uma recuperação sem dor e sem risco.” — Henrik Kehlet, cirurgião dinamarquês e idealizador do protocolo ERAS.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Fístula Pancreática Pós-Operatória
Estratégias de Prevenção, Diagnóstico Precoce e Manejo Terapêutico na Prática Cirúrgica
Autor: Prof. Dr. Ozimo Gama
Categoria: Cirurgia Hepatopancreatobiliar (HPB) / Oncologia Cirúrgica / Complicações Pós-Operatórias
Tempo de Leitura: 11 minutos
Introdução
A duodenopancreatectomia (DP), ou cirurgia de Whipple, representa o ápice da complexidade técnica na cirurgia do aparelho digestivo. Indicada primariamente para neoplasias periampulares, tumores da cabeça do pâncreas e colangiocarcinomas distais, este procedimento viu sua taxa de mortalidade reduzir-se drasticamente em centros de alto volume nas últimas décadas (atualmente abaixo de 3% a 5%). Contudo, a morbidade perioperatória permanece teimosamente elevada, oscilando entre 30% e 50%. O verdadeiro “calcanhar de Aquiles” da cirurgia de Whipple é a Fístula Pancreática Pós-Operatória (POPF – Postoperative Pancreatic Fistula), originada na falha de cicatrização da anastomose pancreatojejunal ou pancreatogástrica. Para o estudante de medicina, o residente em cirurgia geral e o pós-graduando em cirurgia digestiva, dominar a fisiopatologia, a identificação precoce e o fluxograma de tratamento da POPF é o que difere a recuperação oncológica de um desfecho fatal.
Fisiopatologia e a Nova Definição (ISGPS 2016)
Historicamente, a literatura cirúrgica era confusa quanto à definição de uma fístula pancreática, dificultando a comparação entre os serviços. Em 2016, o International Study Group of Pancreatic Surgery (ISGPS) atualizou e padronizou esta definição, mudando o paradigma do diagnóstico.
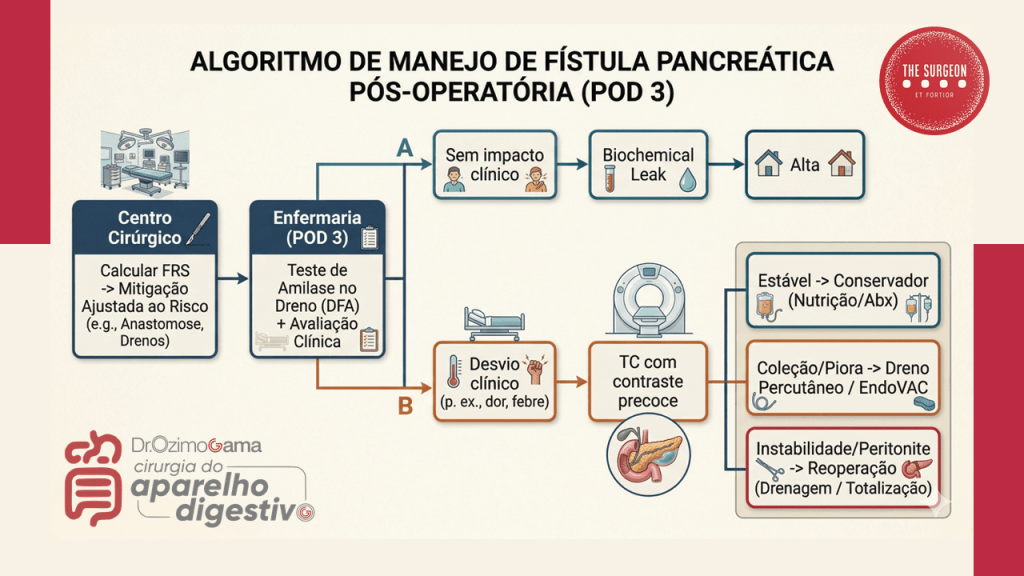
O antigo “Grau A” foi abolido da categoria de fístula verdadeira e passou a ser denominado apenas como Vazamento Bioquímico (Biochemical Leak). Para que uma POPF seja clinicamente diagnosticada (Graus B e C), exige-se a presença de líquido no dreno (ou coleção intra-abdominal) com nível de amilase superior a 3 vezes o limite superior da normalidade sérica, associado a uma mudança obrigatória no curso clínico do paciente (necessidade de jejum prolongado, antibioticoterapia específica, manutenção do dreno por mais de 3 semanas, drenagem percutânea ou reoperação).
Estatísticas e o Cenário Brasileiro: No Brasil, dados do Sistema Único de Saúde (DATASUS) e registros de serviços multicêntricos de cirurgia HPB demonstram que a incidência de POPF clinicamente relevante em grandes centros de referência nacionais varia de 10% a 20%. Essa incidência robusta reforça a premissa de que a cirurgia pancreática deve ser estritamente centralizada em hospitais de alto volume, onde a equipe multidisciplinar está plenamente apta a “resgatar” o paciente da complicação (failure to rescue).
Aplicação na Cirurgia Digestiva
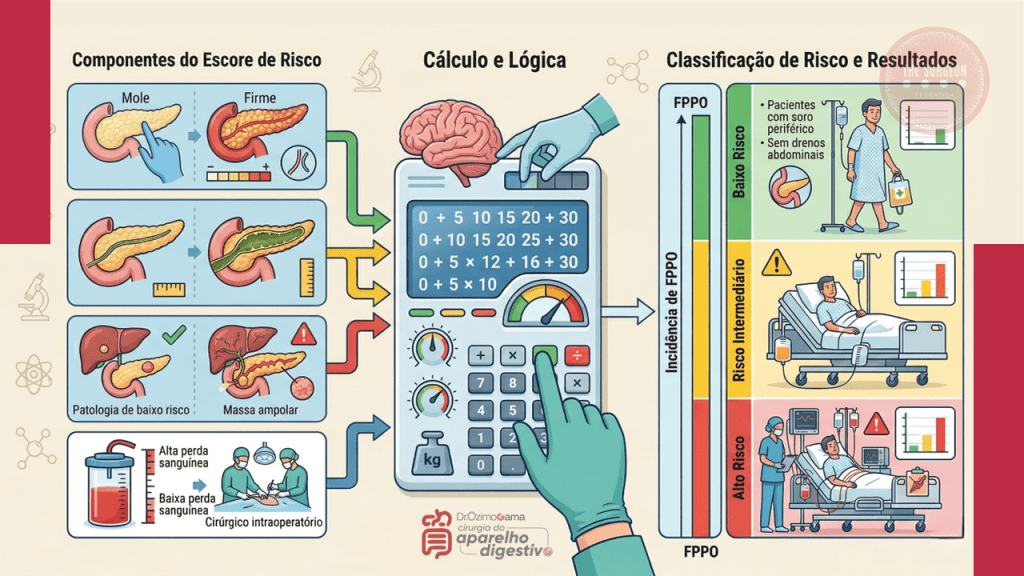
1. Prevenção e Avaliação de Risco Intraoperatório
A prevenção da POPF não começa na síntese, mas na avaliação tátil e visual da glândula. O Fistula Risk Score (FRS) é uma ferramenta validada que estratifica o risco do paciente.
- Fatores de Alto Risco: Uma glândula pancreática de consistência amolecida (infiltração gordurosa) associada a um ducto pancreático principal fino (< 3 mm) compõe a “tempestade perfeita” para o rasgo capsular e a deiscência da sutura. Pacientes com IMC elevado e patologias como o adenocarcinoma de ampola de Vater (que não fibrosam a glândula previamente) têm risco muito maior do que aqueles com pancreatite crônica.
- Tática Cirúrgica: A escolha entre anastomose ducto-mucosa e a técnica de invaginação (dunking) deve respeitar a anatomia do coto e a familiaridade técnica do cirurgião. O uso de fios monofilamentares e agulhas delicadas é imperativo. Estratégias adjuvantes, como a colocação de stents pancreáticos (internos ou externos) para desviar a secreção enzimática da linha de sutura, são valiosas em ductos exíguos. O uso profilático de análogos da somatostatina (octreotida) não é rotina universal, sendo reservado por muitos serviços apenas para o grupo de risco extremo.
2. Diagnóstico Precoce no Dia a Dia da Enfermaria
O diagnóstico da fístula pancreática exige um cirurgião com altíssimo índice de suspeição clínica. O suco pancreático ativado é extremamente cáustico e desencadeia uma resposta inflamatória sistêmica rápida.
- Sinais de Alarme: A taquicardia inexplicada no 3º ou 4º dia de pós-operatório (DPO) é frequentemente o primeiro sinal biológico de vazamento, precedendo a febre, a leucocitose e a dor peritonítica. O retardo do esvaziamento gástrico (gastroparesia) é quase sempre secundário à coleção inflamatória peripancreática adjacente ao estômago.
- O Teste do 3º Dia: A dosagem rotineira da amilase no fluido do dreno no 3º DPO dita o ritmo. Níveis baixos indicam a remoção precoce do dreno (evitando a infecção ascendente e a fístula mecânica induzida pelo próprio dreno). Níveis altos em um paciente com piora clínica impõem a realização imediata de uma Tomografia Computadorizada (TC) de abdome com duplo contraste para mapear coleções fluidas não drenadas.
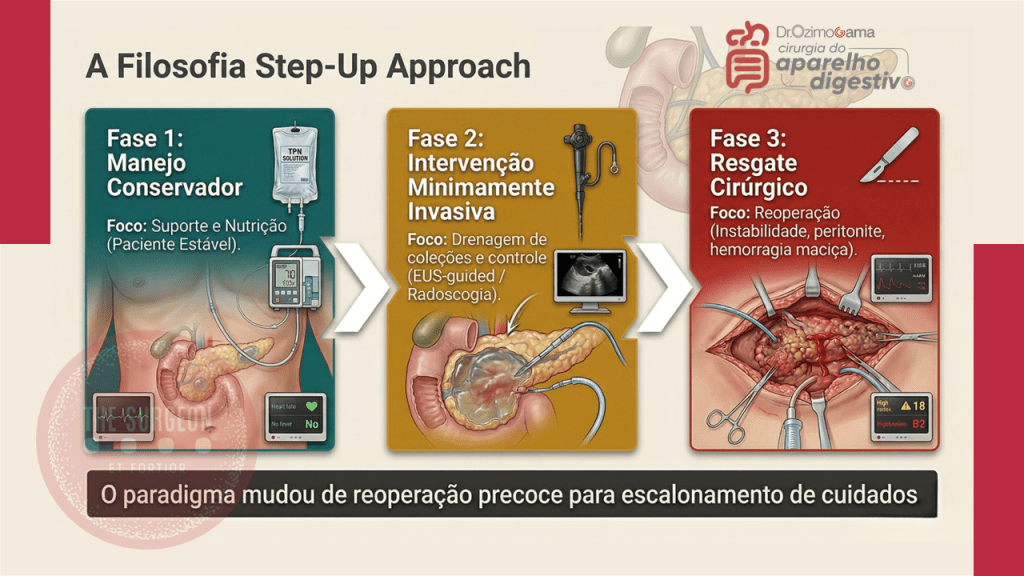
3. A Abordagem Step-Up
A conduta perante uma fístula estabelecida segue um raciocínio de escalonamento (step-up approach):
- Fístula Grau B (Tratamento Clínico/Intervencionista): O pilar é o manejo conservador. Envolve o reposicionamento do dreno cirúrgico ou a inserção de novos drenos percutâneos guiados por TC ou ultrassonografia (Radiologia Intervencionista). Associa-se antibioticoterapia de amplo espectro (focada em translocação entérica), inibidores de bomba de prótons, e rigoroso suporte nutricional (preferencialmente nutrição enteral pós-pilórica ou nutrição parenteral total se o trânsito estiver inviável).
- Fístula Grau C (A Catástrofe e o Resgate Cirúrgico): Representa a falência do tratamento clínico, caracterizada por instabilidade hemodinâmica, disfunção de múltiplos órgãos, sepse não controlada ou hemorragia pós-operatória (decorrente da erosão da artéria gastroduodenal ou hepática pelas enzimas pancreáticas ativadas). A reoperação de urgência é mandatória. Consiste em lavagem ampla da cavidade, múltiplas drenagens calibrosas e hemostasia. Em cenários de desintegração total da anastomose, a tática extrema de salvamento é a totalização da pancreatectomia (remoção do coto pancreático remanescente).
Pontos-Chave
- Definição Atualizada: Vazamento bioquímico não altera conduta. A fístula verdadeira (POPF Grau B/C) exige amilase > 3x o valor sérico no dreno associada a mudança terapêutica (ISGPS 2016).
- Consistência Glandular: Pâncreas mole e ducto fino (<3mm) requerem alerta máximo e técnica cirúrgica de precisão microscópica.
- Vigilância Clínica: Taquicardia isolada no 3º DPO nunca é “normal”; é o principal prenúncio de coleção intracavitária.
- Remoção de Drenos: A prática de manter drenos profiláticos por longos períodos em pacientes sem evidência de vazamento (Amilase no 3º DPO baixa) aumenta a taxa de complicações infecciosas.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
A excelência na execução de uma duodenopancreatectomia não isenta o cirurgião do risco de uma fístula pancreática. O vazamento enzimático é uma realidade inerente à biologia do pâncreas amolecido. Portanto, a verdadeira assinatura de um cirurgião do aparelho digestivo diferenciado não é apenas a técnica de anastomose que ele emprega, mas a sua implacável vigilância no pós-operatório. Compreender o momento exato de acionar a radiologia intervencionista e ter a coragem cirúrgica para reoperar um paciente em deterioração clínica (aplicando adequadamente a filosofia do step-up approach) são as atitudes éticas e técnicas que reduzem a mortalidade. Na cirurgia pancreática, o diagnóstico precoce é o único antídoto contra o desastre.
“A cirurgia pancreática é um exercício contínuo de humildade; o pâncreas é um órgão que não perdoa a manipulação rude, o desrespeito anatômico e a anastomose imprecisa.” — Adaptado dos ensinamentos imortais de Allen O. Whipple, pioneiro da duodenopancreatectomia.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Prevenção Jurídica na Cirurgia Digestiva
As bases das Boas Práticas Jurídicas para o Cirurgião Moderno
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 10 minutos)
Introdução
A prática da cirurgia do aparelho digestivo evoluiu exponencialmente com o advento da cirurgia minimamente invasiva e da robótica. Contudo, essa evolução técnica foi acompanhada por um fenômeno igualmente complexo: a crescente judicialização da medicina. Dados recentes do Conselho Nacional de Justiça (CNJ) apontam um aumento alarmante nas ações judiciais envolvendo supostos erros médicos no Brasil, sendo as especialidades cirúrgicas (incluindo a cirurgia bariátrica e a cirurgia geral) alvos frequentes. Para o estudante de medicina, o residente e o cirurgião já estabelecido, a excelência técnica no centro cirúrgico não é mais suficiente. A proteção jurídica e a gestão de riscos tornaram-se competências inegociáveis. Este artigo traduz as melhores evidências em compliance e prevenção de responsabilidade profissional para a nossa realidade clínica e cirúrgica.
Os Pilares da Proteção Jurídica
A literatura jurídica e de gestão de risco em saúde não prescreve uma “fórmula mágica”, mas estabelece padrões consistentes de governança. A defesa do cirurgião baseia-se na proatividade, ou seja, em ações tomadas antes que o dano ou o litígio ocorram. A mitigação ativa de riscos envolve desde a estruturação de fluxos de atendimento até o amparo em apólices de seguros, garantindo que o profissional exerça sua vocação com autonomia, segurança e paz de espírito.
Práticas Fundamentais
Como aplicamos esses conceitos abstratos na rotina de um serviço de cirurgia digestiva? Abaixo, detalho as boas práticas essenciais baseadas em evidências:
1. Documentação Inatacável e o TCLE
O prontuário médico é a principal (e muitas vezes a única) testemunha de defesa do cirurgião. A documentação deve ser clara, tempestiva e exaustiva. Na cirurgia digestiva, isso se traduz em:
- Descrição Cirúrgica Detalhada: Não economize palavras ao descrever aderências severas, variações anatômicas do trato biliar ou a qualidade dos tecidos ao realizar uma anastomose intestinal.
- Termo de Consentimento Livre e Esclarecido (TCLE): Um TCLE genérico não tem valor jurídico. Ele deve ser individualizado. Vai operar um câncer gástrico? O paciente deve estar ciente (e assinar) sobre os riscos de fístula do coto duodenal, necessidade de CTI e mortalidade associada. O diálogo prévio bem documentado anula a alegação de “falta de informação”.
2. Adesão à Lex Artis e aos Protocolos Clínicos
Agir de acordo com a Lex Artis significa atuar conforme as práticas médicas consagradas e atualizadas. A adesão a diretrizes técnicas (Guidelines) de sociedades como o CBCD, SBCBM ou protocolos internacionais (como o ERAS – Enhanced Recovery After Surgery) é a forma mais eficaz de afastar a culpa (negligência, imprudência ou imperícia).
- Exemplo prático: O uso sistemático do Checklist de Cirurgia Segura da OMS previne a catástrofe médico-legal da cirurgia em paciente ou local errado, além de garantir a profilaxia antimicrobiana no tempo correto.
3. A Comunicação como Escudo Protetor
A ampla maioria dos processos por erro médico nasce de uma quebra na relação médico-paciente. Quando ocorre uma complicação grave — como uma deiscência de anastomose após uma retossigmoidectomia —, a postura do cirurgião dita o desfecho legal. A comunicação proativa, empática, transparente e não conflituosa com o paciente e seus familiares reduz drasticamente o ímpeto litigioso. Abandonar o paciente aos cuidados exclusivos do médico plantonista da UTI após uma complicação é o caminho mais rápido para um tribunal.
4. Governança de Dados e a LGPD
A Lei Geral de Proteção de Dados (LGPD) transformou a gestão de informações médicas. Os controles técnicos de privacidade são mandatórios.
- Cuidado com imagens: Fotografar peças cirúrgicas (como vesículas, tumores) ou exames de imagem e compartilhar em grupos de WhatsApp, mesmo que com intenção didática, sem a anonimização estrita ou o consentimento expresso do paciente, constitui grave infração ética e legal.
5. Seguro de Responsabilidade Profissional e Assessoria Especializada
Operar sem um seguro de responsabilidade civil profissional é expor o patrimônio pessoal a um risco imensurável. É vital compreender as coberturas da apólice, especialmente a cláusula de tail coverage (cobertura de cauda), que garante proteção contra processos instaurados anos após a ocorrência do fato gerador. Além disso, ao primeiro sinal de notificação administrativa (CRM) ou citação judicial, a prática de agir sem o suporte de advogados especialistas em Direito Médico é temerária. A confidencialidade e a estratégia da relação advogado-cliente são irrenunciáveis.
Pontos-Chave para a Prática Diária
- O Prontuário Médico não é apenas uma obrigação burocrática; é a sua armadura legal.
- TCLE é um processo de comunicação, não apenas um pedaço de papel a ser assinado na porta do bloco cirúrgico.
- Aderir estritamente aos Guidelines e Protocolos estabelece um padrão de cuidado defensável.
- Nunca subestime o poder de uma Relação Médico-Paciente baseada na confiança, empatia e presença contínua, especialmente nas adversidades.
Conclusões Aplicadas
A complexidade inerente à cirurgia do aparelho digestivo nos expõe diariamente a riscos biológicos imponderáveis. Fístulas, sangramentos e infecções podem ocorrer mesmo quando a técnica cirúrgica é executada com perfeição. O que diferencia a complicação inerente do ato cirúrgico (o risco aceitável) do ilícito civil ou ético é, fundamentalmente, a nossa conduta preventiva, a clareza da nossa documentação e o rigor ético no trato com o paciente. A proteção jurídica não deve gerar uma “medicina defensiva” prejudicial ao doente (que gera exames e intervenções desnecessárias), mas sim uma medicina preventiva, baseada em compliance, transparência e excelência documental.
“As complicações fazem parte da cirurgia, mas o abandono do paciente e a negligência na documentação são escolhas exclusivas do cirurgião. A verdadeira destreza opera tanto com o bisturi quanto com a caneta.” — Adaptado de preceitos de grandes mestres da cirurgia contemporânea.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Evolução da Medicina Operacional
Lições Eternas para a Logística de Saúde Militar
Prof. Dr. Ozimo Gama
1. O Elo entre o Passado e a Prontidão Operacional
A Medicina Operacional transcende a mera assistência de retaguarda; ela se consolida como um multiplicador de poder de combate indispensável para a manutenção do efetivo combatente. No cenário de defesa contemporâneo, a preservação da integridade física e psíquica da tropa é o fiel da balança que sustenta a viabilidade de campanhas em ambientes de conectividade limitada e logística hostil, como a Região Amazônica, ou em missões sob a égide de organismos internacionais. Aprender com a história militar não é um exercício diletante, mas um imperativo para a Prontidão Operacional. O objetivo é garantir que o apoio de saúde seja resiliente o suficiente para operar sob o atrito do combate, assegurando a “Manutenção do Poder de Combate” — princípio basilar para que o soldado retorne à linha de fogo com a celeridade que a manobra exige. Embora as tecnologias cinéticas evoluam, os princípios de salvar vidas sob fogo permanecem como constantes doutrinárias desde a Antiguidade.
2. Das Cruzadas ao Campo de Batalha Primitivo: O Nascimento do Cuidado sob Fogo
Os conflitos da Idade Média, notadamente as Cruzadas, forçaram a Medicina a migrar do conforto clerical para a brutalidade das intervenções cirúrgicas de campanha. Um exemplo emblemático da “Medicina Operacional” rudimentar ocorreu em agosto de 1097, quando o Duque Godofredo de Bouillon, ao enfrentar um urso selvagem próximo a Antioquia, feriu gravemente a própria perna com sua espada. O sangramento arterial massivo exigiu que os médicos da época agissem minuto a minuto sob extrema pressão. Utilizando técnicas de cauterização com ferro em brasa — inspiradas nos ensinamentos de Albucasis — os cirurgiões estancaram a hemorragia, permitindo que o líder sobrevivesse para retomar o comando meses depois. A organização dos hospitais pela Ordem de São João (Hospitaleiros) em Jerusalém e Acre representou o embrião da triagem e da higiene militar. Estes “xenodóquios” separavam pacientes por diagnóstico, demonstrando que a gestão de leitos e a separação de feridos traumáticos de doentes infectocontagiosos eram vitais para a sustentabilidade da força.
Inteligência Técnica Imediata e Sensível (ITIS): O episódio de Godofredo de Bouillon ilustra que o sucesso do apoio de saúde depende da capacidade de decisão técnica sob estresse. Para o oficial moderno, a lição é clara: sem intervenção imediata no ponto de ferimento, a taxa de retorno ao serviço é nula. A sustentabilidade das campanhas de longo prazo nas Cruzadas só foi possível devido a essa estruturação de cuidados que, embora rudimentar, já visava a preservação do componente humano como recurso estratégico.

3. A Revolução de Dominique Jean Larrey: O Surgimento da Logística Moderna
O Barão Dominique Jean Larrey, cirurgião-chefe da Guarda Imperial de Napoleão, é legitimamente o “pai da medicina operativa moderna”. Sua visão transformou o apoio de saúde de um serviço passivo na Zona de Retaguarda (ZRE) para uma força de intervenção proativa na vanguarda.
- Inovação das Ambulances Volantes: Larrey revolucionou a Evacuação de Feridos (Evoz) ao criar ambulâncias leves que retiravam os feridos ainda sob o fogo inimigo, combatendo a “inatividade administrativa” que abandonava soldados no campo.
- Cirurgia de Urgência e Técnica: Defensor do débridement précoce (debridamento precoce) e das feridas laissées ouvertes (deixadas abertas) para prevenir a gangrena gasosa, Larrey era dotado de uma velocidade técnica prodigiosa, capaz de realizar a desarticulação de um ombro em apenas dois minutos — perícia vital em um Posto de Socorro (PS) operando sem anestesia moderna.
- Ética e Neutralidade: Precursor da Cruz Vermelha, Larrey estabeleceu o “Hôpital destiné à l’ennemi” em Valladolid, tratando prisioneiros espanhóis e ingleses com a mesma dignidade que os franceses.
Napoleão reconheceu sua importância ao declarar: “O homem mais honesto que já conheci… uma imagem do verdadeiro homem de bem”.
ITIS: : A mobilidade de Larrey alterou o moral da tropa (segurança psicológica). No Exército Brasileiro, essa herança reflete-se na busca pela “Hora de Ouro”. O legado de Larrey ensina que o oficial médico deve ser um “chirurgien combattant de l’avant”, integrado à manobra e não apenas um espectador na retaguarda.

4. Século XIX à Era Contemporânea: Da Enfermagem de Nightingale à Evacuação Aeromédica
A Guerra da Crimeia trouxe Florence Nightingale e a revolução da sanidade, mas foi a inovação técnica de Antonius Mathijsen, em 1851, com o gesso (Plaster of Paris), que transformou a logística de saúde. A estabilização eficaz de fraturas permitiu que a Cadeia de Evacuação se tornasse mais resiliente e longa; fraturas estáveis reduziam o risco de embolia gordurosa e trauma secundário durante o transporte, permitindo fluxos logísticos mais audazes. No século XX, o advento dos Mobile Army Surgical Hospitals (MASH) e do helicóptero na Coreia e Vietnã redefiniu a velocidade do apoio. Atualmente, o protocolo Tactical Combat Casualty Care (TCCC) padroniza intervenções salvadoras de vida no ponto de ferimento, focando na tríade: controle de hemorragia, manejo de via aérea e prevenção de hipotermia.
ITIS”: A evolução tecnológica, da tração animal ao Medevac, exige uma coordenação logística impecável de insumos críticos, como sangue e oxigênio. A lição para o planejamento atual é que a tecnologia só é eficaz se houver uma rede de suprimento integrada que acompanhe a velocidade do transporte.

5. O Cenário Brasileiro: Doutrina e o Papel das Forças Armadas
No Brasil, a doutrina é balizada pelo manual MD42-M-04 (Logística de Saúde em Operações Conjuntas), que estabelece os Níveis de Apoio e a interoperabilidade entre o Exército, a Marinha e a Força Aérea. O Corpo de Fuzileiros Navais (CFN), através do seu Batalhão Logístico (BtlLogFuzNav), opera unidades de saúde móveis com alta capacidade expedicionária, aplicando os princípios de Larrey em ambientes litorâneos e ribeirinhos. Na Amazônia, o planejamento exige o uso intensivo de Inteligência Médica (conforme a doutrina NATO AJMEDP-3). Isso significa mais do que tratar doenças; implica mapear a “capacidade hospitalar local” em municípios remotos e monitorar “vetores endêmicos” (como a malária e a leishmaniose). Sem a Inteligência Médica para antecipar ameaças sanitárias, uma força pode ser dizimada antes mesmo do primeiro contato cinético com o inimigo.
ITIS”: A Inteligência Médica é uma ferramenta de antecipação estratégica. Em operações na selva, conhecer o terreno e o perfil epidemiológico local permite ao oficial de saúde dimensionar a Cadeia de Evacuação de forma a garantir que a distância não seja uma sentença de morte para o combatente.

6. Planejamento Logístico Atual
- A Proximidade do Apoio (O Legado do PS): A estabilização deve ocorrer no Nível 1 de apoio, o mais próximo possível da linha de contato, para maximizar a sobrevivência e o retorno à linha de fogo.
- Mobilidade e Evoz: O sistema de saúde deve ser tão ágil quanto a força de manobra. O apoio estático é apoio vulnerável.
- Triagem como Decisão Ética e Tática: Em situações de baixas em massa (MASCAL), a triagem rápida e imparcial é a única ferramenta capaz de otimizar recursos limitados.
- Inteligência Médica (AJMEDP-3): Antecipar ameaças ambientais e mapear a infraestrutura civil local é essencial para a resiliência logística em teatros de operações isolados.
- Unicidade da Cadeia Logística: Do suprimento de sangue à evacuação aeromédica, a logística de saúde deve ser tratada como um sistema unitário e ininterrupto.
7. A Missão Continua
A Medicina Operacional é uma ciência de adaptação, coragem e sacrifício. Do cirurgião que operava sob o frio da Berezina ao oficial médico que planeja o apoio em um Pelotão Especial de Fronteira na Amazônia, o compromisso com a vida do combatente permanece o mesmo. A logística de saúde é o sistema circulatório da força; seu sucesso garante que o Brasil disponha de militares prontos, resilientes e protegidos.
Leitura Recomendada
- BRASIL. Ministério da Defesa. MD42-M-04: Logística de Saúde em Operações Conjuntas. Brasília: MD, 2015.
- GABRIEL, R. A.; METZ, K. S. A History of Military Medicine. New York: Greenwood Press, 1992.
- LARREY, Dominique Jean. Mémoires de chirurgie militarie et campagnes. Baltimore: Joseph Cushing, 1814.
- MCCALLUM, Jack E. Military Medicine: From Ancient Times to the 21st Century. Santa Barbara: ABC-CLIO, 2008.
- MITCHELL, Piers D. Trauma and Surgery in the Crusades. London: University of London, 2002.
- ORGANIZAÇÃO DO TRATADO DO ATLÂNTICO NORTE (NATO). AJMEDP-3: Allied Joint Medical Doctrine for Medical Intelligence. Brussels: NATO Standardization Office, 2015.
- SOUBIRAN, A. Le Baron Larrey: Chirurgien de Napoléon. Paris: Fayard, 1966.
- VAYRE, P.; FERRANDIS, J. J. Dominique Larrey (1766-1842), Chirurgien militaire – Baron d’Empire. e-mémoires de l’Académie Nationale de Chirurgie, v. 3, n. 1, p. 37-46, 2004.
Comunicação Cirúrgica
Padrões, Tensões e Implicações para a Segurança do Paciente na Cirurgia Digestiva
Introdução
A comunicação cirúrgica constitui elemento fundamental da prática operatória contemporânea. Mais do que mera troca de informações técnicas, ela representa o mecanismo central de coordenação relacional entre cirurgião, anestesista, instrumentador, circulante e demais membros da equipe. Na cirurgia digestiva — campo marcado por procedimentos de alta complexidade, como gastrectomias, hepatectomias e colectomias — a qualidade da comunicação influencia diretamente os desfechos clínicos, a formação de residentes e a cultura de segurança do paciente.
Estudos observacionais e revisões sistemáticas recentes demonstram que falhas comunicativas contribuem para mais de 70% dos eventos sentinelas em saúde, conforme dados da The Joint Commission. Na sala de operação, análises de 421 interações revelaram falhas em aproximadamente 30% das trocas entre membros da equipe, gerando ineficiência, tensão e risco aumentado ao paciente (Dingley et al., 2008). Neste artigo examinaremos algunmas evidências científicas sobre o tema, com ênfase em três investigações paradigmáticas, visando oferecer subsídios educativos para cirurgiões digestivos e equipes multidisciplinares.
Padrões de Comunicação Observados em Equipes Cirúrgicas
Pesquisa etnográfica conduzida por Tørring et al. (2019), que acompanhou 39 equipes cirúrgicas (85 profissionais) durante substituições de quadril e joelho — procedimentos com paralelos diretos à cirurgia digestiva —, identificou quatro padrões distintos de interação:
- Comunicação proativa e intuitiva: presente em cirurgias complexas, caracterizada por compartilhamento de objetivos, respeito mútuo e antecipação de problemas.
- Comunicação silenciosa e comum: típica de procedimentos rotineiros, marcada por instruções breves e atmosfera de familiaridade.
- Comunicação desatenta e ambígua: marcada por foco individual, tom ambíguo e, por vezes, ironia ou desrespeito explícito.
- Comunicação contraditória e altamente dinâmica: oscilações rápidas entre respeito e rispidez, levando muitos profissionais ao silêncio estratégico.
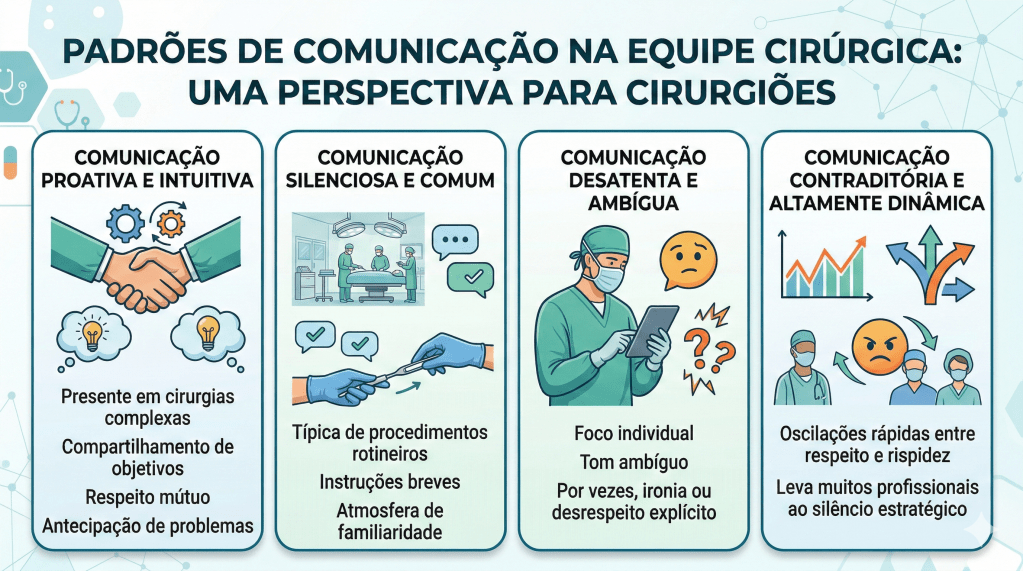
Esses padrões ilustram que a comunicação eficaz transcende palavras: envolve linguagem corporal, tom de voz e alinhamento de expectativas coletivas.
Locais de Tensão Comunicativa e Seus Efeitos Formativos
Lingard et al. (2002), em estudo com 128 horas de observação em 35 procedimentos cirúrgicos, mapearam cinco temas recorrentes de tensão: tempo, segurança/esterilidade, recursos (equipamentos), papéis da equipe e controle da situação. Tais tensões surgem com frequência entre cirurgião sênior e equipe de enfermagem, impactando diretamente os novatos. Os residentes e estudantes reagem predominantemente de duas formas: imitação (mimicry) do estilo autoritário ou retirada (withdrawal), silenciando-se. Ambas as respostas perpetuam ciclos de conflito interprofissional em vez de promover resolução colaborativa. Na cirurgia digestiva, onde o tempo de isquemia, sangramento e integridade anastomótica são críticos, tais dinâmicas podem comprometer a qualidade assistencial e o aprendizado.
Aspectos Emocionais e o Clima da Sala Cirúrgica
Revisão de escopo realizada por Lee et al. (2023), que analisou 10 estudos qualitativos e quantitativos, reforça que o centro cirúrgico é ambiente emocionalmente carregado. O tom e a atitude do líder — geralmente o cirurgião — definem o “clima” da sala. Cultura hierárquica e estresse inibem o speaking up, especialmente entre enfermeiros e residentes. Quando o cirurgião manifesta frustração por meio de gritos ou culpas, instalam-se medo, redução da moral e falhas comunicativas que elevam o risco de eventos adversos. A revisão destaca que o controle emocional não é aspecto acessório, mas competência clínica essencial. Em cirurgias digestivas de grande porte, onde a pressão temporal e a complexidade técnica são elevadas, a regulação emocional do cirurgião torna-se fator protetor da segurança do paciente.
Implicações Práticas para a Cirurgia Digestiva Atual
A integração dos achados demonstra que competência técnica isolada é insuficiente. O cirurgião digestivo contemporâneo deve cultivar inteligência emocional e habilidade retórica para fomentar coordenação relacional. Estratégias como briefing pré-operatório, debriefing estruturado e treinamento em comunicação não-técnica (CRM — Crew Resource Management) reduzem significativamente as falhas identificadas nos estudos citados. Na prática diária, reconhecer os padrões descritos por Tørring, mitigar tensões mapeadas por Lingard e gerir o clima emocional destacado por Lee constitui caminho direto para melhores desfechos, menor burnout da equipe e formação mais robusta de novos cirurgiões.
Conclusão
A comunicação cirúrgica não é mero instrumento operacional; é o alicerce da segurança do paciente e da excelência assistencial na cirurgia digestiva. Os estudos analisados evidenciam que padrões comunicativos saudáveis, gestão de tensões e controle emocional reduzem riscos, otimizam processos e fortalecem o desenvolvimento profissional. Investir nesse domínio representa avanço científico e ético irrenunciável.
“A cirurgia não é um desempenho individual, mas um trabalho de equipe.” Sir Berkeley Moynihan (1865-1936)
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Prof. Dr. Ozimo Gama
Cirurgião do Aparelho Digestivo
Editor Científico – The Surgeon: A Cirurgia Digestiva Atual
Engenharia de Prompt na Educação Médica
Dissecando a Nova Fronteira Tecnológica na Cirurgia Digestiva
1. A Evolução do Estetoscópio ao Algoritmo
A prática médica contemporânea atravessa uma metamorfose digital que exige mais do que a simples adaptação: exige o domínio da técnica. A ascensão dos Modelos de Linguagem Gerativa (GLMs), como o ChatGPT e o Google Bard, não representa apenas a disponibilidade de novos bancos de dados, mas sim uma mudança sísmica na síntese do conhecimento clínico. Neste contexto, a Engenharia de Prompt emerge como a competência estratégica definitiva para o médico do século XXI. Conforme definido por Heston e Khun (2023), trata-se de uma abordagem sistemática de comunicação com IAs para obter resultados de alta precisão. Não se trata de uma conversa informal, mas de uma instrumentação precisa da inteligência artificial.
Para compreendermos o “salto qualitativo” desta ferramenta, basta observar a evolução técnica: o GPT-1 (2018) operava com 117 milhões de parâmetros; o GPT-4 (2023) é estimado em 1 trilhão. Essa expansão colossal mudou o paradigma da simples busca por informação (o modelo “indexador”) para a síntese complexa de conhecimento. Para o cirurgião, isso significa que a IA deixou de ser um dicionário para se tornar um consultor de lógica, exigindo que a instrução dada pelo médico seja tão precisa quanto o plano de clivagem em uma dissecção oncológica.
Esta transição da intuição para a estrutura técnica é o que separa o uso recreativo da IA da sua aplicação acadêmica e clínica de alto nível.
2. A Anatomia de um Prompt de Alta Precisão: Estrutura e Componentes
Na sala de operação, a improvisação é o terreno do erro; na Engenharia de Prompt, a vagueza é a raiz da alucinação. Estruturar uma entrada para a IA não é meramente fazer uma pergunta, mas sim redigir um protocolo de intenção. Podemos comparar a precisão de um prompt bem construído ao rigor técnico necessário em uma colecistectomia: cada componente tem seu “tempo cirúrgico” e função específica.
Para garantir resultados consistentes, um prompt estruturado deve conter quatro pilares fundamentais:
- Contexto: A descrição de quem está perguntando (ex: “Sou um preceptor de residência em cirurgia digestiva”).
- Solicitação Geral: O objetivo macro da interação (ex: “Necessito de uma revisão de condutas”).
- Persona/Papel: Como a IA deve se comportar (ex: “Atue como um Professor Titular de Gastroenterologia Cirúrgica”).
- Formato de Saída: A estrutura final do dado (ex: “Gere uma lista de verificação,” “tabela comparativa,” ou “resumo em tópicos”).
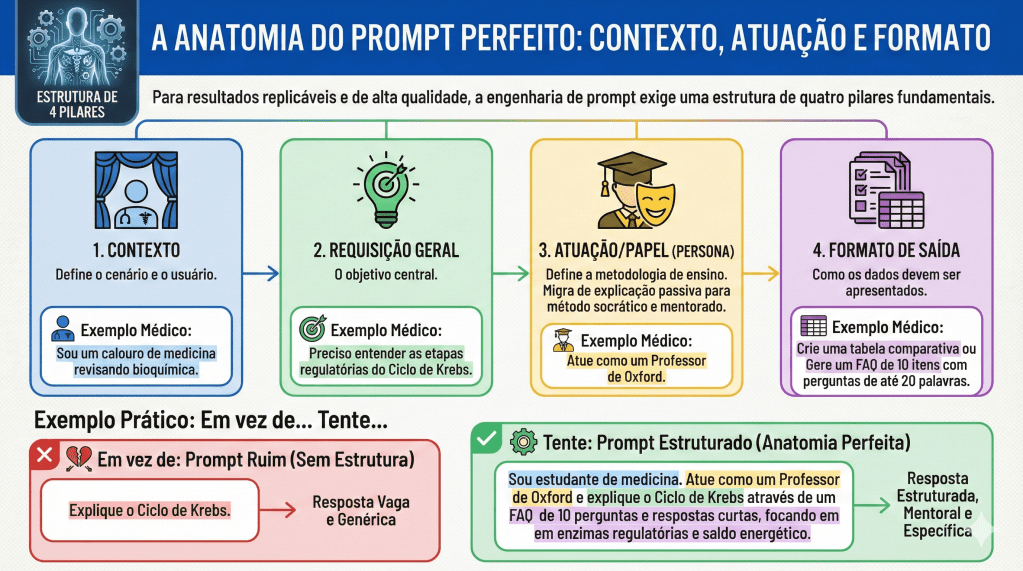
Comparativo de Eficiência: Prompts Vagos vs. Alta Precisão
| Tipo de Prompt | Exemplo Vago | Exemplo de Alta Precisão (Padrão Ouro) |
| Objetivo | Informação Geral | FAQ de Estadiamento Acadêmico |
| Entrada | “Fale sobre câncer gástrico.” | “Como Professor Doutor de Cirurgia, forneça um FAQ de 10 itens sobre o estadiamento do adenocarcinoma gástrico para residentes do R3. Foque no TNM 8ª edição, critérios de ressecabilidade e manejo perioperatório do paciente bariátrico. Entregue em formato de tabela.” |
| Resultado | Texto genérico e superficial. | Guia técnico, hierarquizado e pronto para discussão em round clínico. |
Essa estrutura permite que a IA realize uma triagem interna em seu vasto banco de parâmetros, ajustando o nível de complexidade para a realidade do interlocutor, seja ele um estudante de graduação ou um cirurgião experiente.
3. Níveis de Complexidade: Do Zero-Shot à Decomposição Lógica
No cotidiano acadêmico, a sofisticação da resposta da IA é diretamente proporcional à técnica de prompting utilizada. Podemos escalonar a interação em níveis que desafiam a capacidade de processamento do modelo:
- Zero-Shot vs. Few-Shot: O Zero-Shot é uma solicitação sem exemplos prévios. O Few-Shot é o fornecimento de modelos de comportamento dentro do prompt (ex: “Crie um caso clínico de isquemia mesentérica seguindo rigorosamente este modelo: [Exemplo]”).
- Hierarquia de Lawton (Níveis 1 a 4): Evoluímos de perguntas simples (Nível 1) até o Nível 4, definido como a desconstrução de solicitações complexas em componentes lógicos (Chain of Thought).
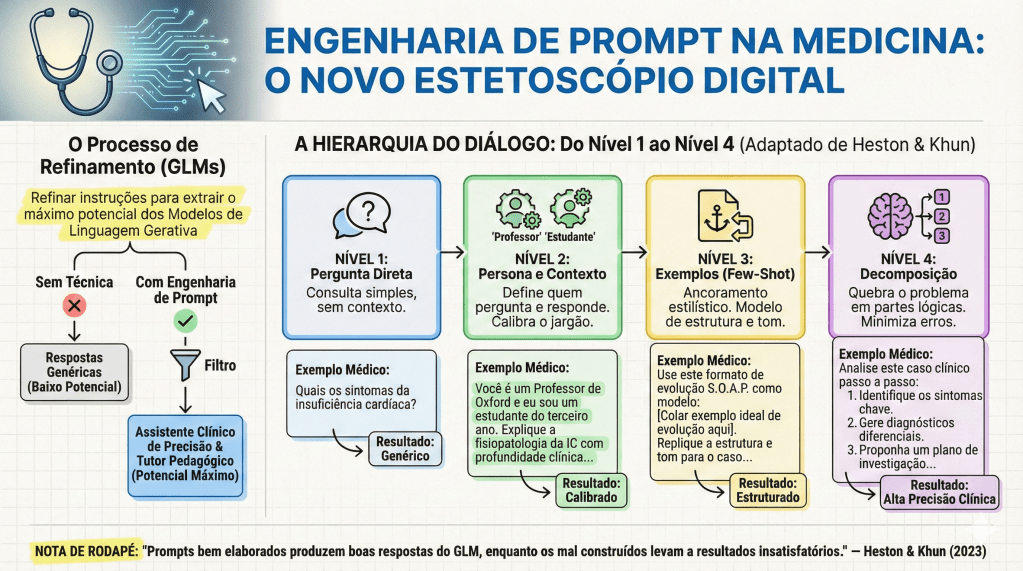
O impacto clínico mais relevante desta última técnica, ativada pelo comando “Pense passo a passo” (Think step by step), é a mitigação de erros catastróficos. Um exemplo clássico do texto de Heston e Khun (2023) ilustra isso: ao perguntar sobre um malabarista que tem 16 bolas, sendo que metade são bolas de golfe e metade das bolas de golfe são azuis, o GPT-3.0 pode falhar se responder instantaneamente. Ao ser instruído a pensar passo a passo, a IA decompõe o problema: total (16) -> metade são golfe (8) -> metade das de golfe são azuis (4). No ambiente cirúrgico, essa lógica é o que previne a iatrogenia em cálculos farmacológicos complexos ou em lógicas de estadiamento multinível.
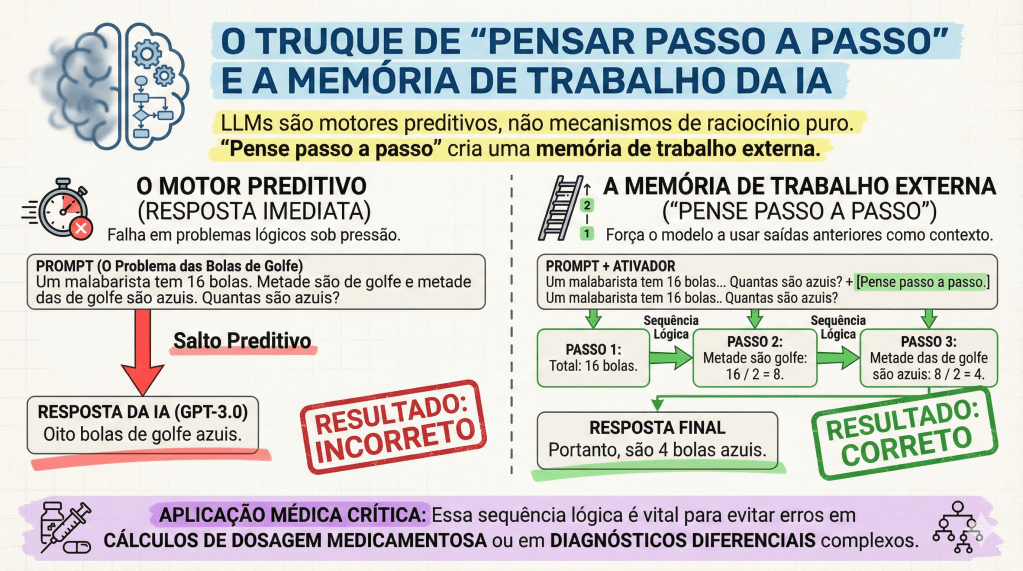
A eficácia do aprendizado, portanto, não reside em receber a resposta pronta, mas em observar o “raciocínio” da máquina, permitindo ao estudante identificar falhas lógicas e consolidar o conhecimento.
4. Aplicação no Ensino-Aprendizado e a Realidade Brasileira (Enare/Enamed)
No cenário brasileiro, marcado pela altíssima competitividade do Enare (Exame Nacional de Residência) e do Enamed, a IA deve ser encarada como um “cérebro periférico”. A densidade do conteúdo cirúrgico exige ferramentas que otimizem a densidade temporal do estudo.
Aplicações Práticas para o Estudante de Alto Desempenho:
- Mnemônicos Cirúrgicos: Criação de fórmulas personalizadas para critérios de gravidade em pancreatite aguda ou escalas de Alvarado.
- Simulação de Pacientes Realistas: Uso de GLMs para simular “Virtual Patients”, permitindo que o estudante treine a anamnese antes do contato real (conforme princípios da AAMC).
- Bancos de Questões De Novo: Geração de simulados inéditos baseados nos exames anteriores do MEC.
A realidade curricular está mudando drasticamente. Segundo dados do Curriculum SCOPE Survey (AAMC), houve um crescimento acentuado na inserção de IA nos currículos das escolas médicas entre 2023 e 2024. No Brasil, essa tendência impacta diretamente a competitividade: o candidato que domina a Engenharia de Prompt processa evidências científicas com uma agilidade que os métodos tradicionais de leitura passiva não conseguem acompanhar. Contudo, este potencial exige uma advertência: a tecnologia deve fortalecer a mente, não atrofiar o raciocínio clínico original.
5. Riscos, Alucinações e a Ética na Medicina Digital
A precisão cirúrgica exige o reconhecimento dos riscos. O maior perigo dos GLMs são as “alucinações”, onde a IA gera informações falsas com um tom de autoridade inquestionável, incluindo referências bibliográficas totalmente inventadas no formato Vancouver.
Checklist de Segurança de Dados e Integridade:
- Verificação de Citações: Jamais utilize uma referência gerada sem conferir o DOI ou a base primária.
- Privacidade: É imperativo nunca inserir dados identificáveis de pacientes reais em prompts de IA.
- Senso Crítico: O cirurgião nunca deve abdicar de sua responsabilidade ética em favor do algoritmo.
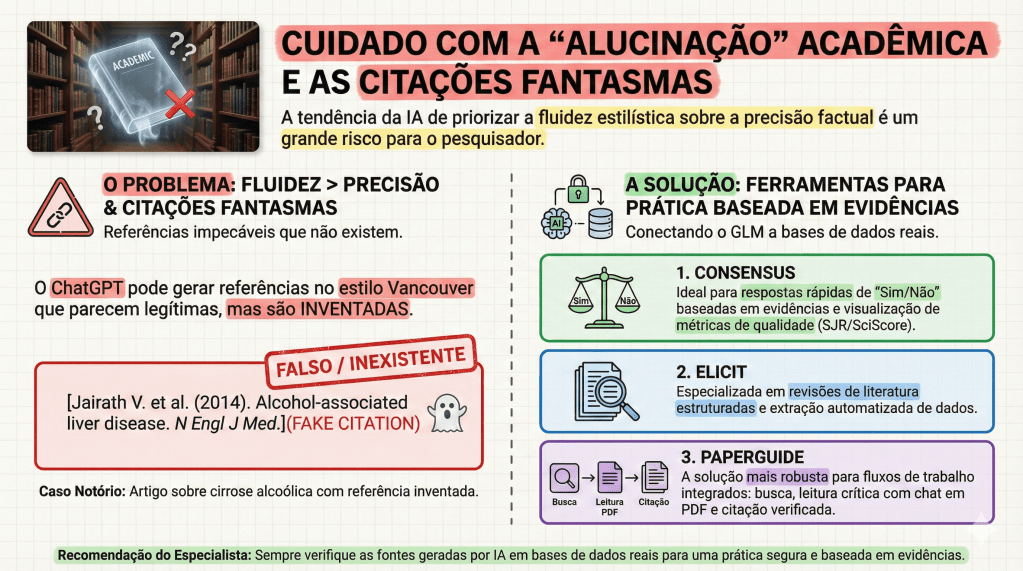
Para o fluxo de trabalho do pesquisador, é vital diferenciar as ferramentas. Modelos de chat puro (como o ChatGPT) são excelentes para síntese, mas para revisões sistemáticas, deve-se integrar ferramentas de evidência real como Elicit e Consensus. Especial destaque deve ser dado ao Paperguide: uma ferramenta “all-in-one” que, além de busca semântica, oferece suporte a múltiplos idiomas — uma vantagem estratégica para o estudante brasileiro que precisa transitar entre a literatura internacional e a prática local. O uso institucional da IA deve, portanto, ser pautado por uma cultura de ética inegociável.
6. Conclusões e Perspectivas Futuras
A Engenharia de Prompt deixará de ser um diferencial para se tornar um requisito básico, tão essencial ao cirurgião digestivo quanto o domínio da estatística básica ou do inglês técnico. Ela é a ponte entre a explosão de dados médicos e a aplicação prática à beira do leito. A mensagem central é clara: a IA deve ser utilizada para fortalecer a compreensão humana, mitigando a falha e ampliando o cuidado, sem jamais criar dependência ou o que chamamos de “pensamento fraco”. O futuro da nossa especialidade pertence àqueles que souberem interrogar a realidade — e a inteligência artificial — com a maior clareza e precisão.
#EngenhariaDePrompt #EducacaoMedica #CirurgiaDigestiva #IAnaMedicina #ResidenciaMedica
——————————————————————————–
“O sucesso da educação médica não reside apenas na transferência de fatos, mas na formação de uma mente capaz de interrogar a realidade com precisão.” — Adaptado dos princípios de William Osler
Gostou ❔ Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
A Cirurgia Digestiva Atual
Autoridade Cirúrgica
A Prerrogativa da Autoridade Cirúrgica sob a Égide da Incerteza Fiscal: Uma Reflexão sobre a Evolução do Prestígio e a Prática Contemporânea
Por: Prof. Dr. Ozimo Gama
O Conceito de Autoridade e a Evolução do Prestígio Médico
O prestígio da profissão médica, historicamente alicerçado em um modelo de prática liberal e em um paternalismo inquestionável, atravessa uma metamorfose estrutural profunda. Sob a égide da contemporaneidade, o cenário de autonomia plena foi substituído por um ambiente de pressões administrativas e incerteza fiscal. Como salientou o Dr. Jesse M. Ehrenfeld, ex-presidente da American Medical Association (AMA), a transição das práticas independentes para os sistemas corporativos é emblemática do estresse econômico enfrentado pela classe. Urge salientar que essa evolução é indissociável da realidade financeira da formação médica. Enquanto na década de 1980 — como recorda o Dr. Weigel — o custo total de quatro anos de medicina girava em torno de US32.000, o cirurgião hodierno egressa com um endividamento médio de US 246.659, podendo ultrapassar os US$ 300.000 em instituições privadas. Concomitantemente, a “Autoridade Cirúrgica” deve ser ressignificada: ela não representa mero poder hierárquico, mas uma responsabilidade derivada da expertise técnica e de um contrato de confiança renovado, essencial para a subsistência ética da especialidade.
Desafios Econômicos e a Realidade da Prática Médica
A análise da medicina atual revela uma insatisfação latente quanto à valorização profissional. Segundo o Medscape Physician Compensation Report 2025, a remuneração média subiu apenas 2,9%, acompanhando parcamente a inflação, enquanto 52% dos médicos manifestam não se sentirem compensados de forma justa. A disparidade entre gerações é notória: em 1985, a vasta maioria dos médicos era proprietária de seu próprio negócio, gerindo equipes e processos. Hoje, o cirurgião é, majoritariamente, um elo em grandes sistemas de saúde, onde a autonomia administrativa é mitigada por métricas corporativas. Os principais vetores de estresse e erosão do prestígio incluem:
• Incerteza Fiscal e Econômica: Oscilações que dificultam o planejamento de carreira a longo prazo.
• Cortes Estatutários de Pagamento: Reduções em sistemas de reembolso (como o Medicare) que não acompanham a complexidade dos atos.
• Burocracia Administrativa e Custos Operacionais: Uma carga intrusiva que desvia o cirurgião de sua atividade fim, exacerbada pelo aumento constante dos custos de manutenção das práticas.
A Autoridade na Cirurgia do Aparelho Digestivo: Expertise e Autonomia
Dentro da hierarquia nosocomial, a Cirurgia do Aparelho Digestivo preserva um “clout” (influência política e social) diferenciado. No entanto, é necessário compreender que esse poder político, como observa Barnett, está profundamente enraizado em um sistema de reembolso não baseado estritamente na saúde da população, mas na valorização de procedimentos de alta complexidade que geram receita crítica para os sistemas hospitalares. A fundamentação da autoridade do cirurgião repousa sobre sua “expertise esotérica”. Jenkins, em suas pesquisas, demonstrou que cirurgiões que operam neonatos de 500g ou realizam duodenopancreatectomias complexas desfrutam de um nível de confiança pública superior. Diferente do pediatra geral, que muitas vezes enfrenta questionamentos constantes sobre condutas rotineiras — como a segurança de vacinas —, o cirurgião digestivo lida com situações de risco vital onde as decisões são técnicas e imediatas. Essa especificidade confere maior autonomia organizacional e confiança do paciente, resultando em um paradoxo interessante: embora o cirurgião trabalhe mais horas e em maior intensidade, os índices de burnout tendem a ser menores do que em especialidades menos procedimentais. A valorização social e a percepção de utilidade crítica atuam como um escudo psicossocial para o especialista.
A Nova Configuração do Contrato Médico-Paciente
O declínio do modelo “Marcus Welby” de paternalismo médico deu lugar a uma era de consumismo em saúde e ceticismo científico, exacerbada pela democratização desenfreada da informação via internet. O contrato médico, outrora um pacto sagrado entre indivíduos, foi reescrito pela burocracia e pelo big business. A autoridade contemporânea deve, portanto, acolher a diversidade e a inclusão como pilares de sua legitimidade. O prestígio moderno não se mede mais pela deferência cega, mas pela busca de equilíbrio, sustentabilidade e autopreservação do profissional.
Aplicação na Prática e Pontos-Chave
No cenário brasileiro, o desafio é análogo. O endividamento do recém-formado em instituições privadas pode variar entre R500.000 e R 800.000, criando uma pressão financeira imediata. Com aproximadamente 5.000 especialistas titulados em Cirurgia do Aparelho Digestivo, enfrentamos uma severa saturação nos grandes centros, o que demanda uma gestão de carreira mais estratégica e técnica.
Pontos-Chave para o Residente e Pós-Graduando:
• Expertise Técnica: O domínio de procedimentos complexos e de alto risco é o fundamento de sua soberania clínica e influência hospitalar.
• Gestão da Autonomia: É imperativo aprender a navegar em sistemas corporativos preservando a integridade da decisão médica frente às pressões administrativas.
• Relação de Confiança: Substitua o paternalismo obsoleto por uma transparência baseada na erudição técnica, gerenciando as expectativas do paciente-consumidor.
• Sustentabilidade da Carreira: A longevidade profissional depende de uma prática que valorize a autopreservação e o equilíbrio ético-financeiro.
Em última análise, a missão do cirurgião permanece como um chamado de serviço. Devemos retomar a visão de Weigel, sentindo-nos como “pastores de nosso rebanho”, responsáveis diretos por vidas que nos são confiadas em momentos de extrema vulnerabilidade. A medicina evoluiu, e o prestígio agora exige mais do que títulos; exige resiliência e adaptação. Como preconizou Theodor Billroth, mestre da cirurgia digestiva:
“O cirurgião deve ter o coração de um leão e as mãos de uma dama.”
A autoridade reside, precisamente, na virtude de equilibrar a força da decisão técnica com a delicadeza do compromisso ético.
The Surgeon – A Cirurgia Digestiva Atual – Et Fortior
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
#CirurgiaDigestiva #ResidenciaMedica #AutoridadeCirurgica #EducaçãoMédica #TheSurgeon
Estilo e Brio Cirúrgico
A Ciência da Comunicação Não Verbal na Liderança Cirúrgica
1. A Ontologia do Brio no Bloco Operatório
No teatro de alta complexidade que caracteriza a cirurgia do aparelho digestivo, a excelência técnica, embora imperativa, é apenas o estrato basal da competência. O que verdadeiramente distingue o mestre do técnico é o “Surgical Panache” — ou brio cirúrgico. Longe de ser um adereço estético, o brio é uma competência transformadora fundamentada na ciência da comunicação não verbal. A literatura contemporânea em liderança cirúrgica e comportamento organizacional sublinha que os seres humanos possuem um imperativo biológico para processar mensagens não verbais com extrema celeridade, realizando julgamentos sociais eficientes antes mesmo da primeira incisão. A eficácia de um líder depende da congruência: o alinhamento absoluto entre o rigor do discurso técnico e a presença executiva. É fundamental desmistificar a interpretação vulgar do modelo de Mehrabian: embora as palavras sejam o veículo das instruções técnicas, o canal não verbal domina 93% do clima emocional e da percepção de confiança da equipe. Sem essa harmonia, a confiança organizacional se dissolve, e a comunicação ineficaz manifesta-se não como um erro acessório, mas como uma complicação clínica gravíssima.
2. A Dualidade da Liderança: Receptividade e Formidabilidade
A mobilização do contingente humano em procedimentos complexos exige o domínio da teoria dos sinais de status, conforme a estrutura de Keating. O cirurgião deve projetar uma imagem binária que ative simultaneamente dois sistemas motivacionais na equipe:
• Receptividade (Calor e Atratividade): Sinaliza abertura e convite à colaboração (sistema de approach). É a vertente que garante a segurança psicológica, permitindo que um instrumentador ou anestesista comunique intercorrências sem temor de retaliação.
• Formidabilidade (Competência e Poder): Transmite agência, autoridade e domínio técnico (sistema de avoidance). É a projeção de distância profissional necessária para manter a hierarquia e o rigor em momentos críticos.
O carisma cirúrgico reside na capacidade de transitar entre esses sinais duplos. Um líder puramente formidável silencia a equipe; um líder exclusivamente receptivo compromete o tempo operatório. A maestria está em ser, simultaneamente, um porto seguro e uma autoridade inquestionável.
3. Kinésica e Oculésica: A Arquitetura da Autoridade e Espaço
A taxonomia dos sinais não verbais oferece diretrizes práticas para o refinamento da postura operatória:
• Kinésica (Postura e Gestual): A adoção de posturas expansivas comunica controle. De acordo com o estudo de Holler e Beatie, o uso de gestos intencionais e fluidos aumenta o valor da mensagem falada em 60%. Deve-se eliminar comportamentos nervosos (fidgeting), que corroem a credibilidade.
• Oculésica (O Olhar): O olhar é o regulador supremo da interação. Aplico rigorosamente a regra de manter contato visual durante 50% do tempo ao falar e 70% ao ouvir. Isso estabelece persuasão e engajamento, permitindo “ler o ar” da sala.
• Vocalização (Vocalics): A gestão paralinguística é vital. Em uma intercorrência hemorrágica durante uma duodenopancreatectomia, o cirurgião deve contra-atacar a sobrecarga do sistema nervoso simpático da equipe através de uma voz de tom grave, volume controlado e ritmo pausado. A calma do líder deve ser auditível para ser contagiante.
4. Aplicação na Cirurgia Digestiva e a Realidade Brasileira
A segurança do paciente é o objetivo teleológico de toda comunicação. Estatísticas globais revelam que 86% das falhas no ambiente de trabalho são atribuídas à comunicação ineficaz. Na cirurgia do aparelho digestivo, onde procedimentos como esofagectomias demandam sincronia absoluta, esse dado é alarmante. No contexto brasileiro, classificado como uma cultura de alto contexto (High-Context), a habilidade de interpretar pistas sutis e nuanças não verbais é ainda mais vital do que em ambientes anglo-saxões ou germânicos. No Brasil, a liderança é exercida através do relacionamento e da percepção de brio; o silêncio de um assistente pode significar uma dúvida técnica que o cirurgião deve ser capaz de decifrar visualmente. Ademais, a educação médica continuada em 2026 exige o domínio da “presença digital”. Em boards clínicos virtuais, a Chronemics (gestão do tempo) e a pontualidade tornaram-se indicadores de prioridade organizacional. O enquadramento da câmera deve ser preciso, mantendo o olhar na lente e as mãos visíveis para preservar a transparência e a autoridade virtual.
5. Pontos-Chave para a Prática do Cirurgião Digestivo
Para os alunos, residentes e pós-graduandos sob minha orientação, estabeleço as seguintes prerrogativas:
1. Domínio do Quadro: “Seja dono da sala”. Use posturas expansivas e movimentos deliberados para sinalizar que o ambiente está sob controle técnico e emocional.
2. Estratégia Dual: Não busque ser apenas amado ou apenas temido. Seja formidável na competência e receptivo na colaboração.
3. Monitoramento Ativo: Realize a “análise muda” de suas performances. Assista a vídeos de suas cirurgias sem áudio para identificar vícios gestuais e falhas de congruência.
4. Inteligência Cultural: Adapte sua comunicação ao estrato da equipe. Em culturas de alto contexto, o brio cirúrgico é o que preenche as lacunas do que não foi dito, mas precisa ser compreendido.
6. O Cirurgião como Líder Corporificado
O brio não é um dom estático, mas uma disciplina dinâmica refinada pela autoconsciência e pelo rigor. Projetar uma presença física autêntica, confiante e empática é o diferencial definitivo para a liderança de alto impacto. O cirurgião que negligencia sua comunicação não verbal é apenas um executor de técnicas; o cirurgião que domina seu brio é um comandante de destinos, capaz de tratar a falha de comunicação com o mesmo rigor científico com que trata uma fístula anastomótica.
——————————————————————————–
“O cirurgião deve ter mãos de dama, olhos de águia e coração de leão; contudo, é a sua presença que confere à equipe a têmpera necessária para a vitória sobre a patologia.” — Baseado no legado de William Stewart Halsted

Gostou ❔ Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
The Surgeon A Cirurgia Digestiva Atual Et Fortior
#CirurgiaDigestiva #BrioCirurgico #LiderançaMedica #EducacaoMedica #TheSurgeon
Segurança em Foco
A Evolução da Cultura de Segurança e o Desafio da Burocratização na Cirurgia do Aparelho Digestivo
1. A Gênese do Risco na Medicina e Cirurgia
A gênese da prática cirúrgica moderna está intrinsecamente vinculada a uma audácia que, aos olhos contemporâneos, beira a temeridade. Em seus primórdios, a medicina não dispunha de comitês de ética, protocolos de conduta ou salvaguardas administrativas; o progresso era esculpido em tempo real, frequentemente à beira do leito e sob um custo humano excruciante. A introdução de tecnologias disruptivas como o éter e o clorofórmio exemplifica essa tensão dialética: embora tenham viabilizado a revolução do ato operatório, enfrentaram resistências ferrenhas sob o pretexto de serem substâncias perigosas e incontroláveis. Esse padrão de rejeição institucional repetiu-se com Ignaz Semmelweis, cuja demonstração empírica da eficácia da higiene das mãos foi ignorada por desafiar identidades profissionais e normas vigentes. Aquela era, magistralmente retratada na série The Knick, exibe uma medicina criativa e heróica, porém caótica e, por vezes, deletéria. Aprendemos, por meio de um processo histórico doloroso, que a inovação desmedida gera danos, mas reconhecemos que, naquele período de obscuridade técnica, a assunção do risco era o único vetor possível para o avanço da ciência.
2. O Surgimento da Segurança como Bússola Moral
Como resposta necessária ao caos da era heróica, a segurança emergiu como a bússola moral da medicina do século XX. A transição para a era da padronização e dos protocolos buscou transformar a arte cirúrgica em uma ciência de alta confiabilidade. O advento do Checklist Cirúrgico consolidou-se como o marco definitivo desta evolução, mitigando erros catastróficos, como intervenções em locais incorretos, e reduzindo drasticamente as complicações evitáveis. A segurança estabeleceu-se como nossa âncora ética sob o aforismo Primum non nocere. Contudo, observamos hoje que este preceito tem sido distorcido: em vez de guiar a prudência clínica, é frequentemente invocado para justificar a inação diante de riscos calculados e necessários. A medicina não deve ser a busca utópica pela anulação do risco a qualquer custo, mas sim o sopesamento rigoroso entre danos e benefícios, sempre pautado pela soberania dos valores do paciente.
3. Quando a Segurança se Torna Burocracia
Assistimos, na atualidade, a uma patologia sistêmica de ordem administrativa: a “fossilização” da segurança em estruturas burocráticas estáticas. O que deveria proteger o paciente transmutou-se em mecanismos de proteção institucional e conformidade legal. Um sintoma alarmante dessa realidade foi o caso de um residente sênior norte-americano que, a seis meses de sua graduação, jamais havia realizado uma drenagem de tórax de forma autônoma — um reflexo direto de sistemas que priorizam a ausência de intercorrências administrativas em detrimento da formação de competência técnica real. No cenário brasileiro, essa estagnação é agravada por infraestruturas hospitalares rígidas e prontuários eletrônicos (EHRs) deficientes, que impõem as seguintes consequências:
• Dreno de Intelecto: Residentes de Cirurgia do Aparelho Digestivo e de Terapia Intensiva gastam, em média, 50% de sua jornada diária em tarefas clericais e documentação redundante, sacrificando o raciocínio clínico e o treinamento em técnica cirúrgica.
• Engessamento da Pesquisa: Processos de governança para estudos de baixo risco podem levar meses ou anos para aprovação, priorizando a prevenção de riscos hipotéticos sobre o aprendizado derivado de pacientes reais.
• Desvio de Finalidade: A documentação clínica passou a servir mais ao faturamento e à auditoria do que à comunicação entre a equipe e ao cuidado direto.
4. O “Stress Test” da Inteligência Artificial (IA) na Prática Cirúrgica
A Inteligência Artificial atua hoje como um teste de estresse que revela as falhas de governança do nosso sistema de saúde. A barreira para a adoção da IA não é de ordem técnica, mas sim uma incapacidade de adaptação das instâncias decisórias. O paradoxo é flagrante: algoritmos de IA são prontamente implementados quando o objetivo é otimizar códigos de faturamento e captura de receita. No entanto, ferramentas de IA como escribas clínicos, que reduzem a carga documental, ou sistemas de suporte ao raciocínio clínico e triagem de imagens, enfrentam barreiras instransponíveis sob o pretexto da privacidade — ainda que sejam mais seguros do que os “atalhos” improvisados por cirurgiões em seus dispositivos pessoais para contornar sistemas hospitalares obsoletos. A resistência atual é uma falha de governança disfarçada de segurança do paciente.
5. Aplicação Prática na Cirurgia Digestiva
Para o cirurgião do aparelho digestivo em formação, o conceito de “Custo do Atraso” deve ser central. Estatísticas demonstram que, em média, transcorrem 14 anos para que uma evidência científica consolidada chegue efetivamente ao leito do paciente. Para um residente que inicia sua trajetória hoje, esse hiato significa que ele poderá estar na metade de sua carreira antes de dominar as inovações que já estão disponíveis agora. É imperativo compreender que a inação não é um porto seguro; ela possui consequências invisíveis, mas mensuráveis. A espera por uma segurança absoluta e estática é, em si, uma forma de dano. Na residência médica e na pós-graduação, a inovação tecnológica deve ser integrada não como um acessório, mas como um pilar da segurança do paciente e da eficiência clínica.
6. Pontos-Chave para o Residente e Pós-Graduando
1. A segurança deve ser adaptativa, não estática: Protocolos que não evoluem com a tecnologia tornam-se obstáculos ao exercício da excelência cirúrgica.
2. Inação também gera dano: O perigo invisível da espera e o atraso na adoção de novas técnicas são formas reais de prejuízo ao paciente.
3. O cirurgião como avaliador e tradutor: O cirurgião não é um usuário passivo, mas um filtro crítico que absorve incertezas para que o sistema de saúde possa aprender e evoluir com segurança.
7. Perspectivas Futuras
A segurança que não evolui torna-se, inexoravelmente, insegura. O desafio da Cirurgia Digestiva contemporânea é resgatar a coragem intelectual de nossos predecessores, temperada pelo rigor científico atual. Devemos atuar como early adopters responsáveis, integrando novas ferramentas de forma monitorada e contínua. A tradição, que outrora serviu para proteger o enfermo, não pode ser reduzida a um mecanismo que protege as instituições contra a mudança. Somente através de uma cultura de aprendizado contínuo e da superação da burocracia fóssil poderemos assegurar que a próxima geração de cirurgiões esteja plenamente capacitada para os desafios de sua era.
Como bem asseverou Lord Lister, o mestre da antissepsia: “O sucesso de uma operação depende da atenção cuidadosa a cada detalhe.” Que essa atenção aos detalhes transcenda o campo operatório e alcance a gestão crítica da tecnologia e dos sistemas que regem nossa profissão. O zelo pelo paciente exige, agora mais do que nunca, zelo pela evolução do sistema.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
The Surgeon A Cirurgia Digestiva Atual Et Fortior
#CirurgiaDigestiva #SegurancaDoPaciente #EducacaoMedica #IAnaMedicina #ResidenciaMedica
A Revolução da Inteligência Artificial no Aprendizado e na Pesquisa em Cirurgia do Aparelho Digestivo
1. O Novo Paradigma da Educação Médica
A evolução da Inteligência Artificial (IA) no seio da medicina contemporânea transcendeu a mera aplicação subsidiária em diagnósticos por imagem para consolidar-se como um pilar epistemológico na pesquisa e no aprendizado. O cirurgião moderno defronta-se com um desafio multifacetado, por vezes sísifo: a imperiosa necessidade de conciliar uma extenuante carga operatória com a produção científica de alto impacto e a gestão de um volume oceânico de literatura especializada. Neste cenário, a Inteligência Artificial Generativa (GenAI) e os Modelos de Linguagem de Grande Escala (LLMs) emergem não como substitutos do intelecto, mas como catalisadores de um fluxo de trabalho otimizado. É fundamental compreendermos que a maestria cirúrgica hoje exige, além da destreza manual, a competência digital para navegar nesta nova fronteira tecnológica com idoneidade e rigor acadêmico.
2. Ferramentas de IA e Categorização Funcional
A fundamentação científica para a adoção dessas tecnologias repousa em evidências recentes e robustas. O estudo seminal de Valencia-Coronel et al. (2026) realizou uma avaliação qualitativa rigorosa de 43 plataformas de IA, fornecendo um arcabouço para a seleção criteriosa de ferramentas no pipeline da pesquisa cirúrgica.
Dentre as categorias funcionais identificadas, destacam-se:
• Mecanismos de Busca Acadêmica: Superando os buscadores genéricos, plataformas como Consensus AI, Elicit e EvidenceHunt focam na síntese de evidências baseadas em revisão por pares. Ressalto a relevância do Manus AI, projetado especificamente para lidar com tópicos cirúrgicos complexos e desfechos heterogêneos, auxiliando inclusive na estruturação de protocolos e tabelas prontas para publicação.
• Interação com Documentos: Ferramentas como AskYourPDF e ChatPDF permitem um diálogo heurístico com manuscritos complexos, facilitando a extração de dados técnicos e a análise metodológica profunda.
• Análise de Literatura: A visualização de redes de citações através de algoritmos (ex: Connected Papers e Litmaps) permite mapear a trajetória de um tema e identificar conexões semânticas fundamentais.
• Assistentes de Escrita e Síntese: Modelos como ChatGPT (em sua versão GPT-4) e ClaudeAI auxiliam na estruturação de rascunhos. Para sínteses profundas, o modo “Deep Research” do Perplexity AI destaca-se por realizar varreduras exaustivas em múltiplos repositórios. No design, o Napkin AI converte conceitos complexos em diagramas técnicos precisos.
O ganho de eficiência é estatisticamente substancial. Conforme demonstrado no estudo de Trad et al. (2024), a aplicação de fluxos baseados em LLM reduziu o tempo de triagem em revisões sistemáticas de 564,4 para 25,5 horas. Mais relevante que a celeridade é a precisão: o estudo reportou um índice de falso-negativo de 0% e uma especificidade de 99,6%, superando o crivo humano em termos de consistência.
3. Aplicação Prática na Cirurgia do Aparelho Digestivo
Para o residente ou o pós-graduando em Cirurgia do Aparelho Digestivo, a integração destas ferramentas deve ser metódica. Imaginemos o preparo para um Journal Club: o acadêmico pode utilizar o Consensus AI para identificar o estado da arte sobre uma técnica de anastomose, empregar o Litmaps para visualizar a rede de citações do ensaio clínico seminal e, finalmente, interpelar a metodologia do artigo através do ChatPDF para identificar possíveis vieses.
O fluxo de trabalho idealizado integra ciclicamente: (1) Busca em mecanismos especializados; (2) Interação conversacional com documentos para extração de dados; (3) Análise de redes de citações para contextualização histórica; (4) Escrita assistida por modelos generativos e (5) Design gráfico para comunicação visual dos resultados.
4. O Papel da Supervisão Humana
Embora a tecnologia seja fascinante, o rigor acadêmico nos impõe cautela. Devemos atentar para o conceito de “débito cognitivo”. Pesquisas conduzidas por Kosmyna et al. (2024) revelam que a dependência excessiva e exclusiva de IAs reduz o engajamento neural e a retenção de conteúdo. Em contrapartida, a sequência “cérebro primeiro, IA depois” — em que a conceituação inicial e o esboço partem do cirurgião — resulta em um aumento de 50% a 200% na conectividade neural através de bandas de EEG, preservando a capacidade de recordação e o pensamento crítico.
No âmbito ético, as diretrizes de entidades como ICMJE, COPE e WAME são peremptórias:
1. Veto à Autoria: Sistemas de IA não possuem personalidade jurídica ou intelectual para figurar como autores.
2. Transparência Radical: Todo uso de GenAI deve ser declarado explicitamente na seção de Métodos ou Agradecimentos.
3. Auditoria e Registros: Seguindo as orientações da JAMA Network, o pesquisador deve manter um registro de todos os prompts (comandos) relevantes utilizados, para fins de auditoria ética e científica.
A IA jamais substituirá o julgamento clínico soberano ou a responsabilidade ética do cirurgião sobre o dado publicado.
BOX DE DESTAQUE: ESSENCIAL PARA A PRÁTICA ACADÊMICA
• Eficiência Paradigmática: Redução drástica no tempo de triagem bibliográfica com precisão cirúrgica (0% de falso-negativos).
• Rigor Científico: Obrigatoriedade de verificação manual das referências para mitigar “alucinações” do modelo.
• Metodologia “Brain-First”: Priorizar a reflexão intelectual antes da assistência tecnológica para evitar o débito cognitivo.
• Ética e Transparência: Registro de prompts e declaração formal do uso de ferramentas conforme diretrizes internacionais.
6. Conclusões Aplicadas à Prática
A Inteligência Artificial é um catalisador de produtividade sem precedentes na história da medicina. Contudo, o cirurgião deve permanecer como o árbitro final da precisão científica. O futuro da educação médica continuada no Brasil exige o desenvolvimento de habilidades digitais que permitam ao médico não apenas consumir tecnologia, mas governá-la sob a égide do rigor científico. Dominar estas ferramentas é, hoje, um requisito para a excelência acadêmica e clínica.
“O cirurgião que conhece apenas a técnica é um artesão; o que domina a ciência por trás dela é um mestre. A IA é nossa nova ferramenta de maestria.”
Gostou? ❔ Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e/ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
——————————————————————————–
Palavras-chave: Inteligência Artificial na Cirurgia, Educação Médica, Cirurgia do Aparelho Digestivo, Pesquisa Cirúrgica, LLMs na Medicina, Residência Médica.
Hashtags: #CirurgiaDigestiva #InteligenciaArtificial #MedicinaAcademica #TheSurgeon #EducacaoMedica
PROF. DR. OZIMO GAMA
The Surgeon
A Cirurgia Digestiva Atual
Et Fortior
A Origem da Cirurgia Abdominal
A História da Primeira Laparotomia de Sucesso

1.0 Um Olhar Sobre o Abismo do Passado Cirúrgico
Hoje, um cirurgião pode remover um grande tumor ovariano em um procedimento seguro, utilizando um eletrocautério para uma cirurgia sem sangue e clipes de plástico para ligar os vasos. É um feito notável, mas que se torna assombroso quando contrastado com a brutal realidade cirúrgica de 1809. Naquele mundo, o interior do abdômen era um santuário inviolável. O que aconteceu na cidade fronteiriça de Danville, Kentucky, não foi uma evolução, mas uma metamorfose. Foi, nas palavras de Shakespeare, “a sea change into something rich and strange” — uma transformação profunda e maravilhosa.
Voltemos a esse tempo. Não existia anestesia — o éter só seria usado 33 anos depois. Os princípios da antissepsia de Joseph Lister só surgiriam em 1865. Transfusões de sangue eram algo para mais de um século no futuro, e a penicilina de Alexander Fleming só seria descoberta em 1928. Qualquer tentativa de abrir a cavidade abdominal era considerada uma sentença de morte.
Foi neste cenário desolador que um cirurgião visionário, Dr. Ephraim McDowell, e uma paciente de coragem extraordinária, Jane Todd Crawford, se uniram para realizar o impossível. Juntos, eles conduziram um “experimento” que não apenas salvou uma vida, mas fundou a cirurgia abdominal. Esta é a crônica desse evento marcante — uma lição fundamental de inovação, diagnóstico e coragem para todos os estudantes e cirurgiões contemporâneos.
2.0 A Crônica de um Milagre Cirúrgico
2.1 O Cenário Cirúrgico do Século XIX: O Dogma da Peritonite Fatal
No início do século XIX, a comunidade médica, especialmente a europeia, operava sob um dogma inabalável: qualquer violação da cavidade peritoneal resultaria invariavelmente em peritonite e morte. Cirurgiões renomados, como o anatomista escocês William Hunter, consideravam a remoção de ovários uma prática incurável e perigosa. Desafiar essa crença não exigia uma evolução do pensamento, mas uma completa revolução. Apesar do medo paralisante, a ideia já havia sido aventada. John Bell, professor de McDowell e um dos cirurgiões mais famosos da Europa, havia falado sobre a possibilidade teórica de tal operação em suas aulas, embora nunca tenha ousado tentar realizá-la. O abismo entre a teoria e a prática era, até então, intransponível.
2.2 Os Protagonistas: Um Cirurgião Visionário e uma Paciente de Coragem Extraordinária
Dr. Ephraim McDowell: Nascido em 1771, McDowell era um cirurgião competente e respeitado na fronteira americana. Sua formação incluiu um aprendizado com o Dr. Alexander Humphreys e estudos na Universidade de Edimburgo, onde foi influenciado por John Bell. Ao retornar para Danville, estabeleceu uma reputação por realizar cirurgias complexas para a época, como a remoção de cálculos vesicais de 23 pacientes sem uma única fatalidade. Um desses pacientes foi um jovem chamado James K. Polk, que mais tarde se tornaria o 11º presidente dos Estados Unidos.

Jane Todd Crawford: Nascida em 1763, Jane era uma mulher de 45 anos, mãe de quatro filhos, que vivia em uma cabana de toras a 60 milhas (quase 100 km) de Danville. Por meses, ela sofreu com um inchaço abdominal persistente e enorme. Seus médicos locais, perplexos, diagnosticaram-na erroneamente como estando em uma gravidez gemelar que já havia passado do tempo. Sua coragem e fortitude seriam postas à prova de uma forma que ninguém poderia imaginar.
2.3 O Diagnóstico e a Decisão Audaciosa
Em 13 de dezembro de 1809, McDowell cavalgou até a casa de Crawford. Seu relato do encontro demonstra uma impressionante acuidade clínica. Ele escreveu:
“Ao exame, per vaginam, não encontrei nada no útero, o que me induziu à conclusão de que deveria ser um ovarium aumentado.”
Sem nenhuma tecnologia, apenas com seu conhecimento de anatomia e o exame físico, McDowell descartou a gravidez e diagnosticou corretamente um tumor ovariano gigante. O passo seguinte foi ainda mais notável. Em um dos primeiros exemplos de consentimento informado, ele explicou a Crawford sua perigosa situação e que a única chance, uma operação, seria um “experimento” nunca antes realizado com sucesso. Ele prometeu tentar se ela estivesse disposta a ir até sua casa em Danville.
A resposta de Jane Todd Crawford foi um ato de coragem monumental. Durante o rigoroso inverno do Kentucky, ela viajou as 60 milhas a cavalo, uma jornada de vários dias, equilibrando o enorme tumor sobre a sela de seu cavalo para se submeter a um procedimento que muito provavelmente a mataria.
2.4 A Operação: Um Marco na História em 25 de Dezembro de 1809
No dia de Natal de 1809, em um quarto no andar de cima da casa de McDowell, a cirurgia foi realizada. Não havia anestesia; a mesa de operação era uma mesa comum de madeira. Para se acalmar durante o procedimento de 25 minutos, Jane Todd Crawford recitava salmos e cantava hinos. A cena, conforme descrita por McDowell, desafia a imaginação moderna. Ele realizou uma incisão de 9 polegadas no lado esquerdo do abdômen, realizando a primeira laparotomia eletiva da história. Com a súbita liberação da pressão, os intestinos “correram para fora sobre a mesa”. Preenchido pelo tumor, o abdômen não podia contê-los. As alças intestinais, segundo o próprio McDowell, “permaneceram de fora por cerca de vinte minutos e, sendo dia de Natal, ficaram tão frias” que ele precisou lavá-las com água morna antes de recolocá-las. Em meio a esse caos controlado, ele passou uma ligadura forte na trompa de Falópio, incisou o tumor, removeu 15 libras de “substância gelatinosa suja” e, em seguida, o saco tumoral de 7,5 libras. Finalmente, fechou a incisão com sutura interrompida, deixando a ponta da ligadura para fora. A recuperação de Crawford foi tão milagrosa quanto a cirurgia. Cinco dias depois, McDowell a encontrou “fazendo sua cama”. Em 25 dias, ela estava saudável o suficiente para fazer a viagem de 60 milhas de volta para casa, novamente a cavalo. Jane Todd Crawford viveu por mais 33 anos, superando seu cirurgião em 12 anos.

2.5 Publicação e Reconhecimento Tardio
Com modéstia, McDowell só publicou seu feito em 1817, no Eclectic Repertory and Analytical Review, após realizar com sucesso mais duas operações semelhantes. A reação da comunidade médica europeia foi de ceticismo e desprezo. James Johnson, editor do influente London Medico-Chirurgical Review, expressou sua incredulidade com um desdém mordaz: “Credat Judoeus, non ego” (Conte isso a outra pessoa, não a mim). Anos depois, ao relutantemente aceitar o feito, sua retratação revelou o preconceito geográfico e racial que McDowell enfrentava: “…todas as mulheres operadas no Kentucky, exceto uma, eram negras, e como essas pessoas suportam cortes com quase, se não total, impunidade como cães e coelhos, nossa admiração diminui…”. O reconhecimento de McDowell como o “Pai da Cirurgia Abdominal” veio postumamente, em grande parte devido aos esforços do Dr. Samuel D. Gross.
3.0 Aplicação e Legado para a Cirurgia Digestiva
Qual a importância deste evento para nós, cirurgiões do aparelho digestivo? A resposta é simples e profunda: tudo. O feito de McDowell foi a refutação prática e definitiva do dogma de que a cavidade peritoneal era intocável. Sua coragem não criou apenas um novo procedimento; ela criou a possibilidade de toda a nossa especialidade. A cirurgia de estômago, fígado, pâncreas e intestino simplesmente não existiria sem aquele primeiro passo revolucionário. É crucial também clarificar a terminologia. O procedimento não foi uma “ovariotomia” — termo que tecnicamente significa apenas incisar o ovário. O que McDowell realizou foi uma laparotomia (a abertura da cavidade abdominal) com uma salpingo-ooforectomia (a extração do ovário e da trompa de Falópio). Usar o termo impreciso diminui a magnitude de seu feito, que não foi apenas remover um órgão, mas sim invadir e manejar com sucesso o santuário proibido do abdômen. A ousadia de McDowell ressoa em sua própria voz, vinte anos depois do evento, em uma carta de 1829:
“Portanto, parece-me uma mera bobagem sobre o perigo da inflamação peritoneal tão falada pela maioria dos cirurgiões.”
4.0 Pontos-Chave para a Prática do Cirurgião Digestivo
A história de McDowell e Crawford oferece lições atemporais para a prática médica moderna:
- Inovação Contra o Dogma: A medicina avança quando profissionais questionam verdades estabelecidas. McDowell transcendeu o “padrão de cuidado” de sua época, confiando em seu julgamento clínico e conhecimento anatômico para fazer o que era considerado impossível.
- A Primazia do Diagnóstico Clínico: A habilidade de McDowell em realizar um diagnóstico preciso baseado unicamente no exame físico e no raciocínio clínico é uma lição poderosa. É um lembrete contundente de que, na ausência de tecnologia, a verdadeira excelência reside no raciocínio anatômico e na sensibilidade do exame clínico — habilidades que jamais devem ser atrofiadas.
- A Aliança Cirurgião-Paciente: O sucesso da empreitada dependeu de uma confiança mútua extraordinária. O consentimento informado de Crawford, mesmo em sua forma mais rudimentar, foi o pilar que sustentou a realização de um procedimento de altíssimo risco.
- Coragem e Responsabilidade: McDowell demonstrou a coragem necessária para ser o primeiro, assumindo total responsabilidade pelo resultado. Ele sabia que, em caso de falha, o peso do fracasso recairia inteiramente sobre ele.
5.0 O Legado Imortal de McDowell e Crawford
A cirurgia realizada em um quarto de uma cidade fronteiriça não foi um avanço evolutivo; foi um salto revolucionário. Nasceu da visão de um homem e da coragem de uma mulher, que juntos mudaram o curso da história da medicina. Não foi o produto de uma “escola” cirúrgica ou de anos de pesquisa, mas um ato de genialidade e audácia que surgiu de novo. Com sua genialidade, Ephraim McDowell devolveu a vida a Jane Todd Crawford; ela, em troca, garantiu-lhe a imortalidade. O que eles realizaram juntos foi, de fato, o início de uma nova era para a medicina.
#HistóriaDaMedicina #CirurgiaAbdominal #Laparotomia #EphraimMcDowell #CirurgiaDigestiva
Anatomia Cirúrgica da Região Inguinal
1.0 Introdução
A anatomia da região inguinal é notoriamente complexa, representando um desafio constante até mesmo para os cirurgiões mais experientes. Como afirmado de forma sucinta por Skandalakis et al. no início de seu trabalho seminal, a anatomia da região inguinal é “enigmática e confusa” (enigmatic and confusing). Este artigo tem como objetivo desmistificar essa complexidade, focando nas estruturas anatômicas cruciais e em suas relações, a fim de fornecer um guia claro e prático para estudantes de medicina, residentes e cirurgiões que atuam no reparo de hérnias inguinais. Uma compreensão precisa desta topografia não é apenas um exercício acadêmico, mas a fundação para a excelência cirúrgica.
2.0 Desvendando as Estruturas Anatômicas
2.1 As Paredes do Canal Inguinal
O canal inguinal é uma passagem oblíqua através das camadas inferiores da parede abdominal. Suas paredes são formadas por diversas estruturas musculoaponeuróticas, como visto na ilustração anatômica. Os limites são:
• Parede Anterior: Formada pela aponeurose do músculo oblíquo externo e, em sua porção lateral, reforçada pelo músculo oblíquo interno.
• Parede Posterior: Considerada a mais importante do ponto de vista anatômico e cirúrgico, é composta primariamente pela fusão da aponeurose do músculo transverso do abdome com a fáscia transversal. Em 23-25% dos indivíduos, é formada apenas pela fáscia transversal.
• Parede Superior (Teto): Composta pelas fibras arqueadas dos músculos oblíquo interno e transverso do abdome e suas aponeuroses.
• Parede Inferior (Assoalho): Constituída pelo ligamento inguinal e, mais medialmente, pelo ligamento lacunar.
A reconstrução desta parede posterior, especialmente quando deficiente, é o objetivo central de qualquer herniorrafia inguinal bem-sucedida.
2.2 As Camadas Musculoaponeuróticas Fundamentais
A parede abdominal é composta por três camadas de músculos planos. De superficial para profundo, temos o oblíquo externo, o oblíquo interno e o transverso do abdome. Embora todos sejam importantes, o músculo transverso do abdome assume um papel de destaque. De acordo com McVay, ele é a camada mais importante da parede abdominal. A integridade deste músculo e sua aponeurose é o que, em última análise, previne a formação de hérnias. Consequentemente, a mobilização e o uso da aponeurose deste músculo são manobras essenciais para um reparo anatômico e duradouro.
2.3 A Crucial Fáscia Transversal
A fáscia transversal é a lâmina de tecido conjuntivo que reveste a superfície interna da musculatura da cavidade abdominal. Ela é uma estrutura fundamental, contribuindo para a formação da fáscia espermática interna no funículo espermático e, como já mencionado, compondo a parede posterior do canal inguinal. Sua integridade é vital para a contenção visceral. Portanto, a dissecção e o reparo desta fáscia não são opcionais, mas sim o alicerce fundamental de uma herniorrafia sem tensão.
2.4 O “Mito” do Tendão Conjunto
O termo “tendão conjunto” é amplamente utilizado, mas sua existência anatômica como uma fusão distinta das fibras inferiores do oblíquo interno e do transverso do abdome é extremamente rara. A evidência anatômica mostra que essa configuração é mais uma exceção do que uma regra.
• Hollinshead considerou sua existência em apenas 5% dos corpos.
• Condon relatou uma incidência de apenas 3%.
• McVay acreditava que o “tendão conjunto” era um artefato de dissecação.
Por essa razão, o conceito de “área conjunta” (conjoined area) é um termo mais preciso e clinicamente relevante. Esta área refere-se à região medial da parede posterior, que inclui estruturas como o ligamento de Henle, a aponeurose do transverso do abdome e a borda lateral da bainha do reto, que são de fato utilizadas no reparo de hérnias.
2.5 Pontos de Referência Cirúrgicos Essenciais
A navegação segura na região inguinal exige o reconhecimento de marcos anatômicos chave:
• Triângulo de Hesselbach: É o local onde ocorre a maioria das hérnias inguinais diretas. Suas bordas, na definição moderna, são: os vasos epigástricos inferiores (borda superior), a bainha do músculo reto abdominal (borda medial) e o ligamento inguinal (borda lateroinferior).
• Ligamento de Cooper: Estrutura robusta formada pelo periósteo do ramo superior do púbis. É reforçado por múltiplas camadas, incluindo contribuições da fáscia transversal, do trato iliopúbico e da aponeurose do transverso do abdome. É um ponto de ancoragem fundamental em diversas técnicas de herniorrafia, como a de McVay.
• Trato Iliopúbico: Uma banda aponeurótica densa que se estende do arco iliopectíneo até o ramo superior do púbis, formando a margem inferior da camada musculoaponeurótica profunda. Condon o encontrou presente em 98% das dissecações. É uma estrutura profunda, paralela ao ligamento inguinal (que é mais superficial), e um marco essencial em reparos laparoscópicos e abertos.
3.0 Aplicação na Cirurgia Digestiva
3.1 Fisiologia e Mecanismos de Contenção da Hérnia
A integridade do canal inguinal normal é mantida por dois mecanismos fisiológicos dinâmicos:
1. Ação Esfincteriana: A fáscia transversal forma um “sling” (alça) ao redor do anel inguinal interno. A contração do músculo transverso do abdome tensiona essa alça, fechando o anel sob a borda muscular do oblíquo interno.
2. Ação de Obturador (“Shutter Action”): Durante a contração da musculatura abdominal (por exemplo, ao tossir), o arco aponeurótico do músculo transverso do abdome se move em direção ao trato iliopúbico e ao ligamento inguinal, reforçando e obliterando qualquer fraqueza na parede posterior.
3.2 Implicações Diretas na Herniorrafia
O conhecimento anatômico se traduz diretamente na estratégia cirúrgica. Como mencionado, a parede posterior é anatomicamente deficiente em 23-25% dos indivíduos, carecendo do suporte da aponeurose do músculo transverso. Nesses casos, a fáscia transversal torna-se a única barreira contra a herniação direta. O objetivo de uma herniorrafia eficaz não é apenas fechar um defeito, mas reconstruir a dinâmica da parede posterior. A compreensão precisa de quais estruturas estão presentes, quais são deficientes e quais podem ser utilizadas para um reparo sólido e sem tensão é o que diferencia um procedimento bem-sucedido de uma recidiva.
4.0 Pontos-Chave
1. A Complexidade é Real: A anatomia inguinal é intrincada e repleta de controvérsias terminológicas. Um estudo contínuo é necessário.
2. O Transverso do Abdome é Rei: A integridade do músculo transverso do abdome e sua aponeurose é o fator mais crítico na fisiopatologia e prevenção das hérnias inguinais.
3. O Tendão Conjunto é Raro: O “tendão conjunto” clássico é um achado raro (3-5%). O termo “área conjunta” é mais apropriado para descrever as estruturas utilizadas cirurgicamente.
4. A Parede Posterior é a Chave: O sucesso do reparo de uma hérnia inguinal depende fundamentalmente da reconstrução de uma parede posterior forte e sem tensão, utilizando as estruturas anatômicas corretas.
5. Conheça Seus Marcos: O Ligamento de Cooper, o Trato Iliopúbico e o Triângulo de Hesselbach são referências anatômicas indispensáveis para o cirurgião realizar um procedimento seguro e eficaz.
5.0 Conclusões Aplicadas à Prática Clínica
Apesar de séculos de estudo e de incontáveis procedimentos cirúrgicos, a região inguinal permanece um desafio anatômico. As variações individuais e as controvérsias na nomenclatura exigem do cirurgião mais do que a memorização de diagramas; exigem um conhecimento profundo e funcional. Esta compreensão detalhada da anatomia é a ferramenta mais poderosa que possuímos para avaliar defeitos herniários, escolher a técnica de reparo mais adequada e, por fim, garantir resultados cirúrgicos superiores e duradouros para nossos pacientes.
#AnatomiaCirurgica #HerniaInguinal #CirurgiaGeral #ResidenciaCirurgia #AparelhoDigestivo
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Conteúdo Extra
Lista Completa de Epônimos Anatômicos da Região Inguinal
Esta lista abrange as estruturas clássicas nomeadas em homenagem a anatomistas e cirurgiões, fundamentais para a compreensão cirúrgica da região inguiocrural.
1. Ligamentos e Estruturas Fibrosas
Os elementos estruturais que formam as paredes e o assoalho da região.
- Ligamento de Poupart
- Nome Moderno: Ligamento Inguinal.
- Quem foi: François Poupart (cirurgião francês, séc. XVII).
- Descrição: A borda inferior enrolada da aponeurose do músculo oblíquo externo. Estende-se da EIAS ao tubérculo púbico, formando o “assoalho” do canal inguinal.
- Ligamento de Gimbernat
- Nome Moderno: Ligamento Lacunar.
- Quem foi: Antonio de Gimbernat y Arbós (cirurgião espanhol, séc. XVIII).
- Descrição: Extensão posterior e triangular do ligamento de Poupart que se fixa no osso púbico. Forma a borda medial cortante do anel femoral.
- Ligamento de Cooper
- Nome Moderno: Ligamento Pectíneo.
- Quem foi: Astley Cooper (cirurgião inglês, séc. XIX).
- Descrição: Espessamento forte do periósteo (membrana do osso) ao longo do ramo superior do púbis. É o principal ponto de ancoragem óssea para telas em cirurgias complexas.
- Trato de Thomson
- Nome Moderno: Trato Iliopúbico.
- Quem foi: James Thomson (anatomista escocês, séc. XIX).
- Descrição: Espessamento da fáscia transversal profundo e paralelo ao ligamento inguinal. É o divisor profundo entre o canal inguinal (acima) e o canal femoral (abaixo).
- Ligamento de Henle
- Nome Moderno: Expansão lateral da bainha do músculo reto abdominal (frequentemente associado à foice inguinal/tendão conjunto).
- Quem foi: Friedrich Gustav Jakob Henle (anatomista e patologista alemão, séc. XIX).
- Descrição: Uma estrutura aponeurótica na parede posterior do canal inguinal, logo na borda do músculo reto abdominal. Ele forma o limite medial do Trígono de Hesselbach. Sua presença é variável; quando forte, protege contra hérnias diretas; quando ausente ou fraco, predispõe a elas.
- Ligamento de Colles (ou Ligamento Reflexo)
- Nome Moderno: Ligamento Inguinal Reflexo.
- Quem foi: Abraham Colles (cirurgião e anatomista irlandês, séc. XIX).
- Descrição: É uma camada de fibras derivadas da aponeurose do oblíquo externo do lado oposto, que cruzam a linha média e se inserem na crista púbica e na linha pectínea do lado afetado. Ele passa atrás do anel inguinal superficial e na frente do tendão conjunto, reforçando a porção medial do canal inguinal.
2. Fáscias e Camadas
As camadas de cobertura da parede abdominal anterior.
- Fáscia de Scarpa
- Nome Moderno: Lâmina membranácea da tela subcutânea.
- Quem foi: Antonio Scarpa (anatomista italiano, séc. XVIII/XIX).
- Descrição: A camada membranosa mais profunda da gordura abaixo da pele.
- Fáscia de Camper
- Nome Moderno: Lâmina adiposa da tela subcutânea.
- Quem foi: Petrus Camper (anatomista holandês, séc. XVIII).
- Descrição: A camada de gordura superficial e fofa logo abaixo da pele.
- Fáscia de Colles
- Nome Moderno: Fáscia membranácea do períneo.
- Quem foi: Abraham Colles (cirurgião irlandês, séc. XIX).
- Descrição: A continuação da Fáscia de Scarpa na região do períneo e escroto/lábios.
3. Espaços e Áreas Definidas
Marcos geográficos críticos para cirurgia e diagnóstico.
- Trígono de Hesselbach
- Nome Moderno: Trígono Inguinal.
- Quem foi: Franz Kaspar Hesselbach (anatomista alemão, séc. XIX).
- Descrição: A área triangular na parede posterior da virilha onde ocorrem as hérnias diretas. Delimitado pelos vasos epigástricos inferiores, a borda do músculo reto (Ligamento de Henle) e o ligamento inguinal.
- Orifício de Fruchaud
- Nome Moderno: Orifício Miopectíneo.
- Quem foi: Henri Fruchaud (cirurgião francês, séc. XX).
- Descrição: O “grande buraco” conceitual na parede abdominal que engloba todas as potenciais hérnias da virilha (direta, indireta e femoral), que deve ser coberto pela tela.
- Espaço de Bogros
- Nome Moderno: Espaço Retroinguinal (pré-peritoneal lateral).
- Quem foi: Jean-Annet de Bogros (anatomista francês, séc. XIX).
- Descrição: O espaço virtual atrás da fáscia transversal e à frente do peritônio, onde as telas são colocadas nas cirurgias laparoscópicas (TEP/TAPP).
- Espaço de Retzius
- Nome Moderno: Espaço Retropúbico (pré-vesical).
- Quem foi: Anders Retzius (anatomista sueco, séc. XIX).
- Descrição: O espaço atrás do osso púbico e à frente da bexiga, medial ao espaço de Bogros.
4. Linfonodos e Vasos
- Gânglio de Cloquet (ou Rosenmüller)
- Nome Moderno: Linfonodo inguinal profundo proximal.
- Quem foram: Jules Germain Cloquet (francês) e Johann Christian Rosenmüller (alemão).
- Descrição: O linfonodo localizado dentro do canal femoral, que pode simular uma hérnia se estiver inflamado.
- Corona Mortis (Termo clássico, não epônimo de pessoa)
- Tradução: Coroa da Morte.
- Descrição: Uma variação vascular perigosa (conexão entre vasos ilíacos externos e internos) que passa sobre o osso púbico, com risco de hemorragia grave se lesada durante a cirurgia.
Hemorragia Digestiva
Hemorragia Gastrointestinal: Visão do Cirurgião
1.0 Introdução
A hemorragia gastrointestinal (HGI) representa uma das principais emergências médicas e cirúrgicas, demandando diagnóstico rápido e manejo assertivo. Classificamos a HGI com base em sua origem anatômica em relação ao ligamento de Treitz. A Hemorragia Digestiva Alta (HDA), proximal a este ligamento, é a mais comum, com uma incidência, no contexto dos Estados Unidos, de 67 casos por 100.000 habitantes. A Hemorragia Digestiva Baixa (HDB), originada distalmente ao ligamento, apresenta uma incidência de 36 casos por 100.000 habitantes, conforme dados do mesmo país. O manejo eficaz desses quadros exige uma abordagem sistemática e multidisciplinar, na qual o cirurgião ocupa uma posição de destaque, sendo peça-chave na condução dos casos refratários ao tratamento clínico e endoscópico.
2.0 Avaliação e Diagnóstico
2.1 Apresentação Clínica e Avaliação Inicial
A apresentação clínica da HGI varia conforme a localização e a intensidade do sangramento.
- HDA: Os sinais clássicos são a hematêmese (vômito com sangue vivo ou com aspecto de “borra de café”) e a melena (fezes enegrecidas, de odor fétido), que pode manifestar-se com perdas sanguíneas de apenas 50 mL.
- HDB: O principal sinal é a hematoquezia (eliminação de sangue vivo ou marrom nas fezes). É crucial ressaltar que a hematoquezia pode ocorrer em 10-15% dos casos de hemorragia digestiva alta maciça, um sinal de sangramento de grande volume e trânsito acelerado, geralmente associado à instabilidade hemodinâmica.
- Avaliação de Severidade: A anamnese e o exame físico são primordiais para determinar a estabilidade hemodinâmica do paciente. A perda de volemia correlaciona-se diretamente com as alterações nos sinais vitais:
- Perda < 15% (<750 mL): Sinais vitais podem estar normais.
- Perda de 15-30% (750-1500 mL): Taquicardia (FC > 100 bpm) e débito urinário reduzido (≤ 30 mL/h).
- Perda de 30-40% (1500-2000 mL): Hipotensão, taquicardia acentuada (FC > 120 bpm) e confusão mental.
- Perda > 40% (>2000 mL): Hipotensão grave, taquicardia (FC > 140 bpm), taquipneia e letargia, com débito urinário insignificante.
- Exames Laboratoriais: A avaliação laboratorial inicial deve incluir hemograma completo, tipagem sanguínea e provas de coagulação, além de avaliação das funções hepática e renal. Uma relação entre a Ureia e a Creatinina sérica (em inglês, Blood Urea Nitrogen ou BUN, resultando na razão BUN/Creatinina) ≥ 30 é um forte preditor de hemorragia digestiva alta.
2.2 Abordagem Diagnóstica por Localização
- Hemorragia Digestiva Alta (HDA):
- Causas Principais: Doença ulcerosa péptica, varizes esofágicas, esofagite, gastrite, lesão de Dieulafoy, lacerações de Mallory-Weiss e neoplasias.
- Diagnóstico: A endoscopia digestiva alta é a modalidade diagnóstica e terapêutica de eleição, devendo ser realizada preferencialmente nas primeiras 24 horas. É imperativo notar que, na suspeita de sangramento por varizes esofágicas, este intervalo deve ser encurtado para 12 horas. Os achados são estratificados pela Classificação de Forrest, que correlaciona o aspecto da lesão (sangramento arterial ativo [Ia], sangramento babante [Ib], vaso visível não sangrante [IIa], coágulo aderido [IIb]) com o risco de ressangramento, orientando a terapêutica.
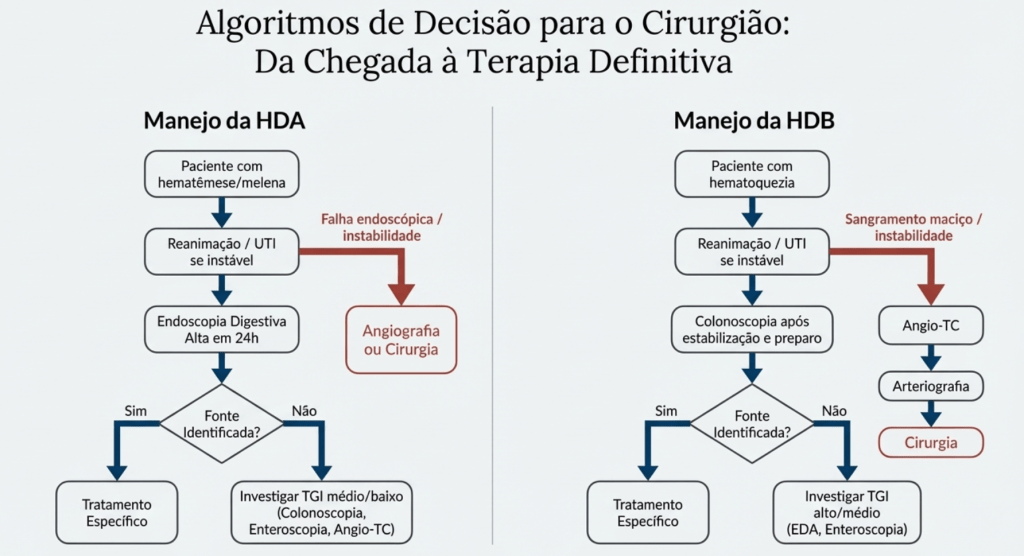
- Hemorragia Digestiva Baixa (HDB):
- Causas Principais: Doença diverticular, angiodisplasia, colites (infecciosa, isquêmica), doença inflamatória intestinal e neoplasias.
- Diagnóstico: Em pacientes estáveis, a colonoscopia é o exame de escolha. Para pacientes instáveis com sangramento ativo e maciço, a angiotomografia computadorizada (Angio-TC) e a arteriografia são fundamentais. A Angio-TC pode detectar sangramentos a uma taxa de 0.3-0.5 mL/min, enquanto a arteriografia requer uma taxa de 0.5-1.0 mL/min, permitindo, contudo, a embolização terapêutica. Em casos de melena com endoscopia alta negativa, a colonoscopia é frequentemente indicada para investigar lesões no cólon direito, que podem apresentar-se de forma atípica.
3.0 Aplicação na Cirurgia Digestiva: O Papel do Cirurgião
A intervenção cirúrgica é, na maioria das vezes, uma terapia de resgate na HGI, reservada para cenários específicos e bem definidos.
3.1 Indicações para Intervenção Cirúrgica
As indicações para uma cirurgia de urgência incluem:
- Falha do tratamento endoscópico ou angiográfico em controlar a hemorragia.
- Instabilidade hemodinâmica persistente, a despeito de ressuscitação volêmica adequada.
- Ressangramento recorrente ou persistente.
- Necessidade de transfusão maciça (para HDB, definida como > 4 unidades de concentrado de hemácias em 24 horas).
- Condições associadas que requerem abordagem cirúrgica, como perfuração ou malignidade.
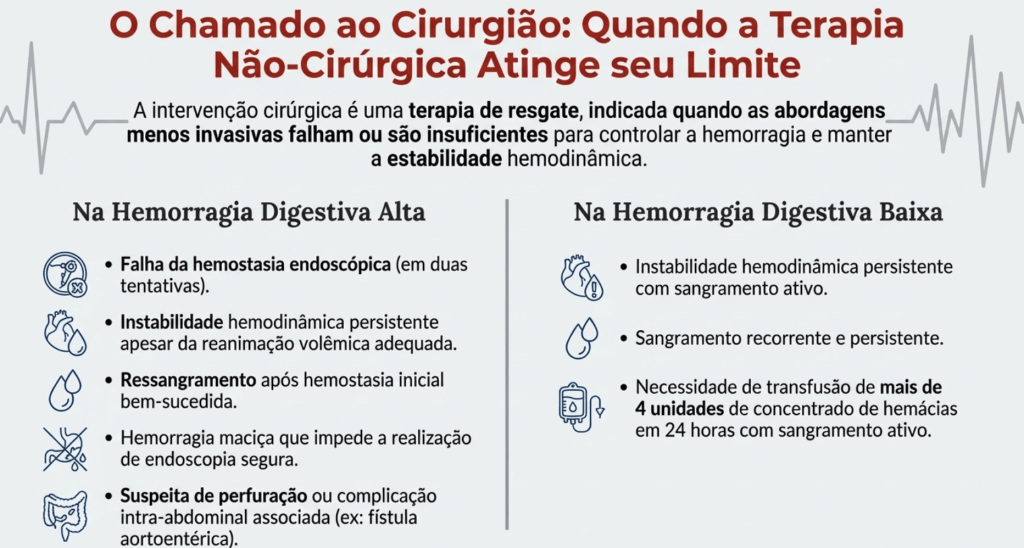
3.2 Estratégias Cirúrgicas na Hemorragia Digestiva Alta
- Úlcera Duodenal: A abordagem cirúrgica clássica para a úlcera péptica duodenal sangrante consiste em duodenotomia anterior, ligadura direta do vaso sangrante (geralmente a artéria gastroduodenal) com pontos em “U, seguida de uma piloroplastia tipo Heineke-Mikulicz. Em pacientes estáveis, a vagotomia troncular pode ser associada para tratar a doença ulcerosa de base.
- Úlcera Gástrica: O tratamento de eleição é a ressecção da úlcera, seja por gastrectomia em cunha ou por uma gastrectomia distal (ex: Billroth I/II). A excisão é imperativa para análise histopatológica, dado que 4-5% das úlceras com aparência benigna podem, na verdade, ser malignas.
- Varizes Esofágicas: A cirurgia é uma terapia de resgate. As opções incluem shunts portossistêmicos (seletivos ou não seletivos) para descompressão portal ou procedimentos de desvascularização (ex: procedimento de Sugiura) em casos selecionados.
- Lesão de Mallory-Weiss: A necessidade de tratamento cirúrgico é rara, consistindo na sutura da laceração esofágica por via laparoscópica ou aberta.
3.3 Estratégias Cirúrgicas na Hemorragia Digestiva Baixa
A localização pré-operatória precisa do sítio de sangramento é o fator mais crítico para o sucesso cirúrgico na HDB.
- Quando o ponto de sangramento é identificado, a ressecção segmentar do cólon é o procedimento de escolha.
- Em pacientes instáveis com sangramento maciço de fonte não localizada, a colectomia subtotal com ileostomia terminal é o procedimento indicado. Esta abordagem está associada a taxas de morbidade de aproximadamente 37% e de mortalidade entre 11% e 33%.
4.0 Pontos-Chave para a Prática Cirúrgica
- A avaliação inicial focada na estabilidade hemodinâmica dita o ritmo da investigação e do tratamento.
- A endoscopia digestiva alta é o pilar diagnóstico e terapêutico na HDA, e a Classificação de Forrest é essencial para guiar a conduta pós-endoscópica.
- A cirurgia na HGI é predominantemente uma terapia de resgate, indicada após falha das modalidades menos invasivas ou em casos de instabilidade hemodinâmica refratária.
- A localização pré-operatória do sítio de sangramento na HDB é fundamental para minimizar a morbimortalidade, sendo a colectomia subtotal reservada para emergências com fonte desconhecida.

5.0 Conclusões
O manejo da hemorragia gastrointestinal é um desafio complexo que exige uma abordagem multidisciplinar e bem coordenada. Embora a cirurgia seja frequentemente uma terapia de resgate, o cirurgião deve ser envolvido precocemente na avaliação de pacientes graves. Um profundo conhecimento das opções diagnósticas e terapêuticas, tanto cirúrgicas quanto não cirúrgicas, é indispensável para garantir a tomada de decisão correta e o melhor desfecho para o paciente.
“A ligadura direta das varizes esofágicas representa a abordagem mais fundamental para controlar uma hemorragia que ameaça a vida.” – Inspirado nos trabalhos de George Crile Jr., 1950.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
#HemorragiaGastrointestinal #CirurgiaDigestiva #CirurgiaGeral #HemorragiaDigestiva #Medicina
Além do Bisturi: A Filosofia Cirúrgica de René Leriche e a Revolução Fisiológica
Na história da medicina, existem cirurgiões famosos por suas mãos ágeis e outros lembrados por suas mentes inquietas. René Leriche (1879-1955) pertence, indubitavelmente, à segunda categoria. Embora fosse um operador exímio, seu verdadeiro bisturi era o intelecto. Autor da obra seminal “La chirurgie, discipline de la connaissance” (A cirurgia, disciplina do conhecimento), Leriche não via a sala de operações apenas como um local de reparo mecânico, mas como um laboratório vivo de fisiologia. Para ele, operar era interrogar a vida. Neste artigo, revisitamos a filosofia deste gigante francês e como ele transformou a cirurgia de um ofício anatômico para uma ciência biológica.
Da Anatomia Estática à Fisiologia Dinâmica
Até o início do século XX, a cirurgia era predominantemente “anatômica”. O cirurgião era visto como um encanador de luxo: removia-se o que estava podre, costurava-se o que estava rasgado, drenava-se o que estava infectado. O foco era a lesão estrutural visível. Leriche desafiou esse paradigma. Ele argumentava que a lesão anatômica era frequentemente o fim da doença, não o começo. A verdadeira patologia residia no distúrbio funcional invisível que precedia a lesão.
“A doença é, antes de tudo, um drama funcional que se desenrola no silêncio dos tecidos.”
Essa visão deu origem ao conceito de Cirurgia Fisiológica. O objetivo não deveria ser apenas a extirpação do órgão doente (uma “confissão de fracasso”, segundo ele), mas a restauração da função normal, muitas vezes através da manipulação do sistema nervoso autônomo e da vascularização.
A Cirurgia como “Vivissecção Terapêutica”
Leriche elevou o status epistemológico da cirurgia. Ele afirmava que o cirurgião possuía um privilégio que o anatomista e o patologista não tinham: o acesso à patologia viva. Enquanto a anatomia patológica estuda as “cinzas do incêndio” (o tecido morto), a cirurgia observa o “fogo” (a doença em evolução). Portanto, a cirurgia deveria ser uma “disciplina do conhecimento”, onde cada intervenção serve para entender a fisiopatologia humana. Para Leriche, um cirurgião que não raciocina fisiologicamente é apenas um técnico manual, fadado à obsolescência.
A Dor como Doença (La Douleur-Maladie)
Talvez a contribuição mais humanística de Leriche tenha sido sua guerra contra a dor. Rompendo com a tradição estoica que via a dor como um mecanismo de defesa útil ou um aviso benéfico, Leriche a classificou como um erro biológico. Ele cunhou o termo “A Dor-Doença”. Na visão dele, a dor crônica não protege; ela destrói. Ela altera a personalidade, esgota as reservas vitais e cria um ciclo vicioso simpático que perpetua o sofrimento. Suas pesquisas sobre a causalgia e o papel do sistema simpático na dor abriram as portas para a moderna medicina da dor e a neuromodulação. Foi neste contexto que ele nos legou sua definição poética e precisa de saúde:
“A saúde é a vida no silêncio dos órgãos.”
O Legado de Leriche na Cirurgia Moderna
Por que ler René Leriche em pleno século XXI? Porque a cirurgia moderna é, em essência, a realização do sonho de Leriche. Quando realizamos uma cirurgia metabólica para tratar diabetes (e não apenas para reduzir o estômago), estamos praticando a cirurgia fisiológica de Leriche. Quando utilizamos bloqueios nervosos ou estimulação medular, estamos seguindo seus passos no controle da dor. Quando buscamos a preservação de órgãos em vez da amputação, honramos sua filosofia. René Leriche nos ensinou que a técnica é indispensável, mas é a fisiologia que deve guiar a mão do cirurgião. O virtuosismo técnico sem base científica é perigoso; a ciência sem técnica é impotente. O cirurgião completo, portanto, é aquele que opera com as mãos, mas corta com a mente.

Gostou desta reflexão histórica? Acompanhe o The Surgeon para mais conteúdos sobre a arte, a ciência e a filosofia da cirurgia.
A Dualidade da Humanização Cirúrgica
Era da Inteligência Artificial e da Robótica: Desafios e Perspectivas
Por Prof. Dr. Ozimo Gama
Coordenador do Curso de Medicina da Universidade Federal do Maranhão
O Cenário Atual e a Necessidade do “Toque Humano”
A prática da cirurgia do aparelho digestivo vive um momento de paradoxo fascinante. Por um lado, testemunhamos avanços tecnológicos sem precedentes, com a cirurgia robótica e a inteligência artificial (IA) redefinindo os limites do possível. Por outro, enfrentamos uma crise silenciosa na relação médico-paciente. No Brasil, segundo dados do DATASUS e do Conselho Federal de Medicina, realizamos milhões de procedimentos cirúrgicos anuais pelo Sistema Único de Saúde (SUS), onde a alta demanda muitas vezes colide com a necessidade de um atendimento individualizado.
A “humanização” não é apenas um conceito abstrato ou uma “soft skill” desejável; é um imperativo clínico. Estudos epidemiológicos demonstram que pacientes que estabelecem uma relação de confiança sólida com seus cirurgiões apresentam melhor adesão ao tratamento pós-operatório, menores índices de litígios médicos e, subjetivamente, uma percepção de dor reduzida.
O desafio contemporâneo, como bem alertava o Prof. Alcino Lázaro da Silva, é evitar que o “fascínio das máquinas e dos botões” transforme o jovem cirurgião em um “sectário ou robô”. Precisamos integrar a tecnologia sem permitir que ela congele nossos sentimentos ou desqualifique a essência da nossa profissão: o cuidado com o ser humano.
Tecnologia, Ontoética e Controvérsias
A Inteligência Artificial e a Despersonalização
A IA chegou para auxiliar na tomada de decisão, predizendo complicações e otimizando fluxos em centros cirúrgicos. No entanto, existe o risco real da “atrofia da empatia”. Quando confiamos excessivamente em algoritmos para o prognóstico, corremos o risco de tratar o paciente como um conjunto de dados biométricos, e não como uma biografia. A tecnologia deve ser uma ferramenta de meio, nunca de fim. O cirurgião que se esconde atrás da tela do computador perde a oportunidade de exercer a “Ontoética” — a ética do ser, o respeito intrínseco à vida humana que transcende a técnica.
Aspectos Médico-Legais e o Consentimento
A humanização tem implicações jurídicas diretas. O Prof. Milton Glezer destaca que o paciente tem o direito de recusar tratamento (salvo risco iminente de morte) e de ter acesso irrestrito ao seu prontuário. No Brasil, a judicialização da medicina tem crescido exponencialmente. Uma parte significativa desses processos não decorre de erro técnico (imperícia), mas de falha na comunicação. O Consentimento Livre e Esclarecido não deve ser apenas um formulário burocrático assinado na admissão. Ele deve ser um processo contínuo de diálogo, onde o cirurgião traduz o “tecniquês” para a realidade do doente, respeitando sua autonomia e dignidade.
Controvérsias Filosóficas
A controvérsia reside na formação médica atual. Os currículos de graduação e residência muitas vezes privilegiam a técnica em detrimento da humanística. Criamos excelentes técnicos capazes de realizar gastrectomias complexas, mas que, por vezes, falham em comunicar um diagnóstico de câncer gástrico com a compaixão necessária. A escola médica deve ensinar que o doente prefere, acima do tecnocrata, o amigo; acima do executor de procedimentos, o médico que orienta e acolhe.
Aplicação Prática na Cirurgia do Aparelho Digestivo
Na nossa especialidade, a humanização possui facetas muito específicas e impactantes:
- Ostomias e Imagem Corporal: Ao indicar uma colostomia definitiva, por exemplo, o cirurgião digestivo não está apenas alterando a anatomia, mas a autoimagem e a vida social do paciente. A abordagem humanizada exige preparar este paciente psicologicamente, envolvendo a equipe multidisciplinar e a família antes mesmo do ato cirúrgico.
- Oncologia Cirúrgica: O diagnóstico de neoplasias do trato gastrointestinal carrega um estigma de mortalidade. A forma como a notícia é dada (protocolo SPIKES, por exemplo) é tão crucial quanto a linfadenectomia realizada.
- Cirurgia Bariátrica: O paciente obeso muitas vezes carrega anos de preconceito, inclusive dentro do sistema de saúde. A humanização aqui significa enxergar a obesidade como doença crônica, despindo-se de julgamentos morais e oferecendo um suporte que vai além da perda de peso.
Pontos-Chave para a Prática Diária
Para o residente e o jovem cirurgião, a humanização se traduz em atos concretos:
- Olho no Olho: A tecnologia (computadores, tablets) não deve ser uma barreira física durante a consulta. Sente-se, olhe para o paciente e escute ativamente antes de examinar.
- Identificação Clara: Como preconizado nas diretrizes hospitalares, apresente-se, diga sua função e certifique-se de que o paciente sabe quem é o responsável pelo seu tratamento (titularidade médica).
- Gestão da Expectativa: Explique riscos e benefícios reais. A frustração do paciente muitas vezes nasce de uma expectativa irrealista não corrigida pelo cirurgião no pré-operatório.
- O “Não” Terapêutico: Saber a hora de não operar (obstinação terapêutica) em casos de carcinomatose ou doenças terminais é, talvez, a maior prova de humanidade e ética cirúrgica.
Perspectivas Futuras
O futuro da Cirurgia do Aparelho Digestivo não será definido apenas pela precisão dos robôs ou pela acurácia dos algoritmos de IA, mas pela nossa capacidade de manter a essência humana em um ambiente cada vez mais digital. A “Ontoética” deve guiar nossas mãos tanto quanto a anatomia.
Precisamos formar cirurgiões “híbridos”: exímios operadores da tecnologia, mas profundos conhecedores da alma humana. Como discutido nos textos bases, o hospital deve buscar trazer esperança, e o médico deve lembrar que, ao tratar um doente, está lidando com uma unidade indivisível de medos, histórias e sentimentos. A tecnologia passa, a máquina obsoleta é trocada, mas o impacto de um atendimento humano perdura na memória do paciente e de seus familiares.
#CirurgiaDigestiva #HumanizaçãoMédica #Bioética #EducaçãoMédica #OncologiaCirurgica
“O único meio de combater a praga da impessoalidade e da frieza na medicina moderna é cultivar as humanidades no médico, pois o segredo do cuidado com o paciente é importar-se com o paciente.” — Adaptado de Francis Peabody (embora clínico, sua máxima é a pedra angular para a humanização cirúrgica moderna).
Gostou? ❔ Nos deixe um comentário ✍️, compartilhe em suas redes sociais e/ou mande sua dúvida pelo 💬 Chat Online em nossa DM do Instagram.
Princípios Fundamentais da Oncologia Cirúrgica Digestiva
Uma Abordagem Contemporânea e Baseada em Evidências
O Cenário Atual do Câncer Digestivo no Brasil
A Cirurgia do Aparelho Digestivo vive um momento de transformação sem precedentes. Não somos mais apenas “técnicos de ressecção”, mas parte integrante de uma complexa engrenagem multidisciplinar. A relevância deste tema é sublinhada pelos dados epidemiológicos alarmantes. Se no passado nos baseávamos em estimativas modestas, hoje a realidade é desafiadora: segundo a Estimativa 2023-2025 do Instituto Nacional de Câncer (INCA), esperam-se 704 mil casos novos de câncer por ano no Brasil.
Destaque-se que as neoplasias do trato gastrointestinal ocupam posições cimeiras. O câncer colorretal figura como o segundo mais incidente em mulheres e homens na maioria das regiões, com cerca de 45 mil novos casos anuais, seguido de perto pelo câncer de estômago (21 mil casos) e esôfago. Estes números não são apenas estatísticas; representam uma demanda crescente por cirurgiões oncológicos altamente qualificados, capazes de compreender não apenas a anatomia, mas a biologia tumoral.
A Biologia como Norte da Técnica Cirúrgica
Fisiopatologia e Disseminação
O entendimento clássico da cirurgia oncológica, herdado dos princípios de William Halsted no final do século XIX, baseava-se na premissa de que o câncer era uma doença puramente local que se disseminava centrifugamente. Embora a radicalidade (ressecção em bloco) permaneça um pilar, hoje compreendemos a doença como sistêmica desde fases precoces em muitos casos.
A disseminação ocorre por três vias principais que o cirurgião deve dominar:
- Linfática: Predominante em carcinomas (ex: adenocarcinoma gástrico e cólon).
- Hematogênica: Preferencial em sarcomas e carcinomas avançados (fígado e pulmões como sítios-alvo).
- Transcelômica (Peritoneal): Comum em neoplasias gástricas T3/T4, ovário e apêndice, exigindo estratégias específicas como a peritoniectomia.
O Princípio da Radicalidade e Margens (R0)
O objetivo primário da cirurgia oncológica curativa é a ressecção R0 (ausência de doença residual macroscópica e microscópica). A cirurgia R1 (doença microscópica residual) ou R2 (macroscópica) impacta drasticamente o prognóstico.
- Ressecção em Bloco: O tumor nunca deve ser violado. A peça deve ser removida envolta por tecido saudável, respeitando as fáscias anatômicas e os pedículos vasculares na sua origem.
- Linfadenectomia: Não serve apenas para estadiamento, mas tem papel terapêutico. No câncer gástrico, por exemplo, a linfadenectomia D2 é o padrão-ouro em centros especializados, associada a menor recidiva locorregional.
Neoadjuvância vs. Adjuvância
A decisão entre operar primeiro (upfront surgery) ou indicar terapia neoadjuvante é um dos grandes debates atuais.
- Vantagens da Neoadjuvância: Tratamento precoce de micrometástases, redução do tumor (downstaging) facilitando a ressecção R0 e teste in vivo da quimiossensibilidade. É o padrão atual para câncer de esôfago localmente avançado e câncer de reto médio/baixo.
- Vantagens da Adjuvância: Baseada no estadiamento patológico preciso (pTNM), evitando tratamento excessivo em estádios precoces.
Aplicação Prática na Cirurgia Digestiva
A prática moderna exige que o cirurgião diferencie dois conceitos cruciais frequentemente confundidos: Ressecabilidade e Operabilidade.
- Ressecabilidade: É uma característica do tumor (relação com estruturas vitais).
- Operabilidade: É uma característica do paciente (reserva funcional, comorbidades, status performance). Um tumor pode ser ressecável, mas o paciente inoperável.
O Papel da Citorredução e HIPEC
Para a carcinomatose peritoneal, historicamente considerada uma condição terminal, houve uma mudança de paradigma. Em neoplasias selecionadas (como pseudomixoma peritoneal, mesotelioma e alguns casos de câncer colorretal), a combinação de Cirurgia de Citorredução (Peritoniectomia) com Quimioterapia Intraperitoneal Hipertérmica (HIPEC) tem oferecido sobrevida em longo prazo, transformando uma doença fatal em uma condição crônica tratável.
Planejamento Multidisciplinar
O cirurgião oncológico não atua isolado. A discussão em Tumor Boards é mandatória. A indicação cirúrgica deve considerar a biologia molecular (ex: status do gene APC em colorretal, superexpressão de HER2 em gástrico) e a resposta a terapias sistêmicas.
Pontos-Chave para a Prática Cirúrgica
- Estadiamento Preciso: Nunca leve um paciente à sala sem um estadiamento completo. A laparoscopia diagnóstica é fundamental em tumores gástricos e pancreáticos para evitar laparotomias desnecessárias em casos de carcinomatose oculta.
- Margens Cirúrgicas: A margem circunferencial (radial) no câncer de reto e a margem proximal no câncer gástrico e esofágico são preditores independentes de sobrevida.
- Manuseio da Peça (“No-touch technique”): Evite a manipulação direta do tumor. A ligadura vascular prévia e a mobilização cuidadosa previnem a embolização tumoral intraoperatória.
- Documentação: O relatório cirúrgico deve detalhar as cadeias linfáticas dissecadas e as estruturas preservadas ou ressecadas, orientando o patologista e o oncologista clínico.
Perspectivas Futuras
A cirurgia digestiva na sua área de atuação oncológica evoluiu de amputações extensas para procedimentos de precisão, muitas vezes minimamente invasivos (laparoscópicos ou robóticos), sem perder a radicalidade oncológica. O futuro aponta para uma integração ainda maior com a biologia molecular e a imunoterapia. O cirurgião do futuro deverá ser, antes de tudo, um oncologista que opera: alguém que entende que o bisturi é apenas uma das armas, e que saber quando não operar é tão vital quanto a técnica operatória refinada.
Como nos ensinou o pai da cirurgia oncológica moderna:
“O cirurgião deve ser o médico do paciente oncológico, e não apenas o técnico que remove o tumor.” — William Stewart Halsted
Hashtags
#CirurgiaDigestiva #OncologiaCirurgica #EducaçãoMédica #ResidenciaCirurgia #CancerDigestivo
Gostou? ❔ Nos deixe um comentário ✍️, compartilhe em suas redes sociais e/ou mande sua dúvida pelo 💬 Chat Online em nossa DM do Instagram.
ASPECTOS MÉDICO-LEGAIS DA LESÃO INADVERTIDA DA VIA BILIAR
- Membro Titular do Colégio Brasileiro de Cirurgiões
- Membro Titular do Colégio Brasileiro de Cirurgia Digestiva
1. Introdução
A lesão inadvertida da via biliar (LVB) é a complicação com maior impacto clínico, emocional e jurídico da colecistectomia. Em muitos países, é uma das principais causas de processos por erro médico em cirurgia geral. Do ponto de vista médico-legal, o ponto central não é a existência da lesão em si, mas a forma como o cirurgião:
- Indicou a cirurgia;
- Conduziu o procedimento (técnica, CVS, bailouts);
- Reconheceu e tratou a lesão;
- Documentou e comunicou o evento ao paciente e à família.
Este texto aborda, em linguagem direta, os principais aspectos médico-legais que o cirurgião geral | cirurgião do aparelho digestivo precisa dominar frente a uma suspeita de lesão iatrogênica da via biliar principal.

2. Lesão de via biliar ≠ erro médico automático
Juridicamente, lesão de via biliar é, em princípio, um evento de risco inerente ao procedimento, sobretudo na colecistectomia laparoscópica, reconhecido em diretrizes nacionais e internacionais.
Em termos de responsabilidade profissional, o que será avaliado é se houve:
- Indicação adequada da cirurgia;
- Técnica compatível com o padrão atual (CVS, uso de bailouts, conversão quando necessário);
- Diligência no reconhecimento precoce da lesão;
- Conduta correta após o dano (referência, reconstrução, suporte);
- Transparência na comunicação.
Ou seja: não é a complicação que gera responsabilidade, e sim a condução inadequada antes, durante ou depois do evento.
3. Consentimento informado
Do ponto de vista pericial, o consentimento é peça-chave:
- A colecistectomia deve ser apresentada como procedimento com:
- Risco de sangramento, infecção, fístula biliar, lesão de via biliar e necessidade de reoperação.
- O termo deve ser:
- Claro, objetivo, datado, assinado pelo paciente (ou responsável) e pela equipe.
- Ideal:
- Anotação no prontuário reforçando que os riscos foram explicados verbalmente.
Em muitos litígios, a ausência de menção à possibilidade de lesão de via biliar no consentimento é usada como argumento de falha na informação, mesmo quando a técnica foi correta.
4. Padrão técnico esperado (CVS, bailouts e conversão)
Peritos costumam avaliar:
- Se houve tentativa documentada de obter o Critical View of Safety;
- Se o cirurgião reconheceu a “vesícula difícil” e utilizou manobras de bailout (subtotal, fundo–primeiro, conversão, abandono);
- Se a insistência em dissecar um triângulo de Calot obliterado foi temerária.
Alguns pontos práticos com peso médico-legal:
- Não obter CVS e mesmo assim clipar e seccionar estruturas é quase sempre visto como conduta imprudente.
- Não converter ou não chamar ajuda em cirurgias claramente difíceis pode ser interpretado como negligência.
- O uso de colangiografia intraoperatória em caso de dúvida anatômica é bem visto pericialmente, mesmo que não obrigatório.
5. Reconhecimento e manejo da lesão intraoperatória
Do ponto de vista jurídico, lesão reconhecida e tratada intraoperatória gera cenário muito mais favorável ao cirurgião do que lesão ignorada e diagnosticada tardiamente com peritonite biliar ou sepse.
Boas práticas com impacto médico-legal:
- Se houver suspeita de lesão maior:
- Registrar no ato operatório que houve dificuldade anatômica e suspeita de dano.
- Se a equipe não tiver expertise em reconstrução, não improvisar; encaminhar para centro de referência.
- Drenos adequados e exames de imagem precoces (TC, colangioRM, CPRE) em pós-operatório duvidoso demonstram diligência.
A omissão em investigar icterícia, febre ou saída de bile por dreno no pós-operatório é frequentemente qualificada como negligência em perícias.
6. Documentação operatória
O relatório cirúrgico é uma das peças centrais em processos médico-legais. Deve conter:
- Indicação da cirurgia (cólica biliar, colecistite aguda, etc.);
- Achados intraoperatórios (inflamação, fibrose, “vesícula difícil”);
- Descrição da técnica:
- Tentativa de obter CVS;
- Uso de colangiografia intraoperatória, quando feita;
- Manobras de bailout, conversão, subtotal, etc.;
- Quaisquer intercorrências (sangramento, suspeita de lesão, necessidade de sutura em via biliar, etc.).
A ausência de descrição detalhada geralmente é interpretada contra o cirurgião, pois abre espaço para a presunção de que padrões técnicos não foram seguidos.
7. Comunicação com o paciente e a família
A forma como o cirurgião comunica a complicação é relevante:
- Negar ou minimizar o evento, ou culpar exclusivamente “o organismo do paciente”, costuma agravar o conflito.
- O recomendado é:
- Explicar com clareza o que ocorreu;
- Deixar claro que a complicação está sendo manejada com todos os recursos disponíveis;
- Documentar o conteúdo da conversa no prontuário.
Transparência e empatia costumam reduzir a judicialização. O oposto também é verdadeiro.
8. Encaminhamento a centros de referência
Outra questão avaliada em perícia é quando e para onde o paciente foi encaminhado:
- Lesões complexas (Strasberg E, perda de segmento biliar, comprometimento vascular) não devem ser reparadas por equipes sem experiência em reconstrução biliodigestiva.
- Reconstruções malsucedidas em série, feitas em hospitais sem expertise, frequentemente são interpretadas como imprudência e imperícia.
O encaminhamento precoce para centro com cirurgião HPB experiente demonstra boa prática e costuma ter peso favorável em eventual demanda judicial.
9. Papel das diretrizes e literatura
Em perícia, é comum a comparação da conduta com:
- Diretrizes societárias (CBCD, WSES, SAGES, EAES etc.);
- Protocolos hospitalares;
- “Estado da arte” à época do procedimento (por exemplo, reconhecimento do CVS como padrão-ouro).
Se o cirurgião seguiu recomendações amplamente aceitas, é difícil sustentar que houve erro grosseiro, mesmo diante de complicação grave.
10. Dano, nexo causal e responsabilidade
Em termos médico-legais, três elementos precisam estar presentes para configurar responsabilidade civil:
- Ato ou omissão culposa (técnica inadequada, falta de diligência, ausência de informação).
- Dano (lesão de via biliar, perda de parte do fígado, invalidez, óbito).
- Nexo causal entre a conduta e o dano.
Exemplo:
– Lesão biliar reconhecida, adequadamente reparada em centro de referência, com boa evolução → pode ser entendida como complicação aceitável.
– Lesão ignorada, sem investigação, evoluindo para sepse e transplante → há forte argumento de falha na assistência.
11. Estratégias de prevenção médico-legal
Em linhas simples:
- Indique bem (indicação precisa e registrada).
- Faça CVS sempre que possível e saiba abandonar a dissecção perigosa.
- Use bailouts (subtotal, fundo–primeiro, conversão) quando necessário; não insista em anatomia impossível.
- Documente tudo (relatório detalhado, fotos/vídeos, evolução diária).
- Investigue sinais de complicação sem demora.
- Encaminhe cedo lesões complexas a centros de referência.
- Comunique com clareza e registre a conversa.
Essas medidas não apenas reduzem o risco de processo, mas principalmente melhoram o cuidado ao paciente, que é o objetivo central.
“O objetivo técnico principal na Colecistectomia, não é a retirada da vesícula biliar, mas proteger a via biliar principal.” Prof. Dr. Ozimo Gama
Hashtags (SEO)
#LesãoDeViaBiliar #ResponsabilidadeMédica #CirurgiaDigestiva #MedicinaLegal #CriticalViewOfSafety
A Doutrina da Visão Crítica de Segurança (CVS) na Colecistectomia Laparoscópica
Fundamentos, Técnica e a Era da Inteligência Artificial
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 11 minutos)
Introdução
A colecistectomia laparoscópica é, indiscutivelmente, uma das intervenções cirúrgicas mais realizadas no planeta. Contudo, apesar de sua consolidação como um procedimento seguro, as lesões iatrogênicas da via biliar principal continuam a assombrar os blocos operatórios, configurando-se como uma das complicações mais temidas, onerosas e medicolegais da cirurgia moderna. Com o advento da laparoscopia no final dos anos 1980, observou-se um pico alarmante na incidência dessas lesões. Em resposta a esta crise global de segurança, o Dr. Steven Strasberg propôs, em 1995, a Visão Crítica de Segurança (CVS – Critical View of Safety). Mais do que uma simples manobra, o CVS transformou-se no dogma central da cirurgia biliar. Este artigo disseca o racional anatômico, a sistematização técnica rigorosa e as aplicações contemporâneas do CVS na prática do cirurgião do aparelho digestivo.
A Patogenia da Lesão e o Racional Anatômico
Para prevenir um erro, é imperativo compreender a sua gênese. A literatura clássica é taxativa: a esmagadora maioria das lesões biliares graves não ocorre por imperícia motora, mas por um erro de percepção visual conhecido como “Misidentification” (identificação errônea). A armadilha mais letal é a técnica da “Visão Infundibular”. Em cenários de inflamação aguda, fibrose ou tração inadequada, o ducto colédoco ou o ducto hepático comum alinham-se paralelamente à vesícula, mimetizando o ducto cístico. O cirurgião se convence de forma ilusória e perigosa de que “tem certeza de estar vendo o cístico”. Essa confiança excessiva, aliada à dissecção apressada, resulta na transecção trágica da via biliar principal. O CVS foi desenhado cirurgicamente para aniquilar esta ilusão de ótica.
Os Três Critérios Obrigatórios do CVS
O CVS não é uma suposição; é um método de prova anatômica objetiva. Para declarar que o CVS foi atingido, todos os três critérios abaixo devem ser cumpridos simultaneamente antes do disparo de qualquer clipe ou grampeador:
- Dissecção Completa do Triângulo Hepatocístico: Toda a gordura e o tecido fibroso devem ser removidos do triângulo formado pelo ducto cístico, ducto hepático comum e borda hepática. A exposição deve ser visualizada nas faces anterior e posterior. Atenção: o ducto hepático comum não precisa (e não deve) ser dissecado ativamente, mas o triângulo deve estar limpo.
- Separação Parcial da Vesícula do Leito Hepático: O terço inferior da vesícula biliar (infundíbulo) deve ser completamente descolado da placa cística (leito hepático). Este passo, muitas vezes negligenciado, é o que garante que as estruturas dissecadas estão efetivamente a entrar na vesícula, e não a passar por ela.
- Apenas Duas Estruturas Adentrando a Vesícula: Exclusivamente um ducto (ducto cístico) e uma artéria (artéria cística) devem ser vistos penetrando a vesícula. Ambos devem estar completamente isolados e identificáveis circunferencialmente (visão de 360 graus).
Robustez, Saídas e a Era Moderna
A eficácia do CVS é incontestável. Em grandes séries publicadas, como a de Yegiyants et al. (3.042 casos) e Avgerinos et al. (998 casos) em que o CVS foi estritamente aplicado, a taxa de lesão biliar grave foi de zero.
Cenários Adversos e Técnicas de Saída (Bail-Out Procedures)
O verdadeiro valor do CVS revela-se na dificuldade. Quando há inflamação severa, colecistite crônica esclerosante ou um Triângulo de Calot “obliterado” (frozen Calot), atingir o CVS torna-se perigoso ou impossível.
Para o cirurgião maduro, a incapacidade de completar o CVS não é um obstáculo a ser forçado, mas um alarme biológico de perigo iminente. Nestes casos, impõe-se a adoção imediata de técnicas de saída:
- Colecistectomia Subtotal (Fenestrada ou Reconstituída).
- Conversão precoce para cirurgia aberta.
- Realização de Colangiografia Intraoperatória.
Documentação Médico-Legal
A diretriz cirúrgica contemporânea exige que o CVS seja documentado. O cirurgião deve registrar uma fotografia ou um breve vídeo intraoperatório que demonstre inequivocamente a exposição anterior e posterior das estruturas isoladas. A inclusão desta prova no prontuário médico eletrônico protege o paciente contra complicações e o cirurgião em contextos litigiosos.
Cirurgia Robótica e Inteligência Artificial (IA)
Os princípios de Strasberg são universais e imutáveis, independentemente do instrumental. Na Cirurgia Robótica, a visão 3D ampliada de altíssima definição e a estabilidade das pinças facilitam o cumprimento escrupuloso dos três critérios. As perspetivas futuras são ainda mais fascinantes: algoritmos de Inteligência Artificial (IA) e visão computacional estão a ser treinados para reconhecer e validar os critérios do CVS em tempo real no monitor cirúrgico, funcionando como um checklist virtual que impede a clipagem até que o software confirme a segurança anatômica.
Pontos-Chave para a Prática Diária
- Prova, não Suposição: O CVS transforma um julgamento subjetivo (“parece o cístico”) numa evidência anatômica irrefutável.
- O Risco da Visão Infundibular: Confundir um infundíbulo dilatado com o ducto cístico é a principal via para a lesão do colédoco.
- Descolar para Comprovar: Não basta limpar o triângulo de Calot; a separação do terço inferior da vesícula do leito hepático (Critério 2) é essencial.
- Pausa Obrigatória: A identificação das duas únicas estruturas deve ser um “momento estático”, validado verbalmente por toda a equipe antes da transecção.
Conclusões Aplicadas
O Critical View of Safety transcendeu a classificação de “técnica cirúrgica” para se consolidar como o padrão-ouro e a obrigação ética universal na colecistectomia laparoscópica. A sua adoção obrigatória nos programas de residência médica aniquila a cultura do achismo visual, substituindo-a pelo rigor científico. Ao reconhecer que o principal inimigo do cirurgião biliar é a sua própria mente (na forma de ilusão de ótica), o CVS fornece a armadura necessária para proteger o doente de morbidades devastadoras. Na cirurgia do aparelho digestivo, a paciência não é apenas uma virtude; é uma técnica de salvamento.A identificação deve ser um momento estático, após completa dissecação, e não um julgamento apressado.”
“A identificação deve ser um momento estático, após completa dissecação, e não um julgamento apressado.” — Dr. Steven Strasberg, cirurgião e idealizador da Visão Crítica de Segurança.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
KYOTO IPMN GUIDELINES 2024
Introdução
A neoplasia mucinoso papilar intraductal do pâncreas (IPMN) representa um dos principais desafios no diagnóstico e manejo das lesões císticas pancreáticas. Com o avanço das técnicas diagnósticas e uma compreensão mais profunda da progressão dessas lesões, o Protocolo de Kyoto 2024 trouxe diretrizes atualizadas e baseadas em evidências para orientar a conduta cirúrgica. Este artigo tem como objetivo esclarecer os principais pontos das novas recomendações, abordando sua aplicação na prática do cirurgião do aparelho digestivo.
Classificação e Critérios de Risco
Os IPMNs são classificados em tipo ducto principal (MD-IPMN), tipo ducto secundário (BD-IPMN) e tipo misto (MT-IPMN). Os novos critérios de risco do Protocolo de Kyoto 2024 incluem:
- Estigmas de alto risco (HRS): icterícia obstrutiva, nódulo mural ≥5 mm, dilatação do ducto pancreático principal ≥10 mm e citologia suspeita ou positiva.
- Características preocupantes (WF): crescimento acelerado (>2,5 mm/ano), cistos >30 mm, nódulos murais <5 mm, espessamento da parede cística, entre outros.
O reconhecimento desses fatores é essencial para a decisão cirúrgica, diferenciando lesões de baixo risco daquelas que podem evoluir para displasia de alto grau ou carcinoma invasivo.
Indicação Cirúrgica
O Protocolo de Kyoto 2024 reforça a necessidade de uma abordagem personalizada, considerando o estado clínico do paciente, as condições anatômicas e a presença de comorbidades. As principais indicações cirúrgicas incluem:
- IPMNs do ducto principal devido ao alto risco de malignização.
- IPMNs do ducto secundário com estigmas de alto risco.
- IPMNs mistos com crescimento progressivo ou sintomatologia associada.
A decisão entre pancreatectomia parcial ou total depende da extensão da lesão e da histologia intraoperatória.
Aplicação na Cirurgia Digestiva
O manejo cirúrgico do IPMN deve seguir princípios oncológicos rigorosos, evitando pancreatectomias excessivas e preservando a função endócrina e exócrina do órgão. Algumas das principais estratégias incluem:
- Ressecção com margens negativas: intraoperatório, a análise histológica por congelação é essencial para guiar a extensão da ressecção.
- Pancreatectomia minimamente invasiva: avanços na laparoscopia e cirurgia robótica permitiram ressecções mais seguras e menos invasivas.
- Monitoramento pós-operatório: mesmo após a ressecção completa, a vigilância é recomendada devido ao risco de neoplasia residual ou carcinoma concomitante.
Estatísticas Relevantes
No Brasil, o câncer de pâncreas representa cerca de 2% de todos os tumores malignos, mas com alta letalidade. Estima-se que cerca de 10-15% dos casos de adenocarcinoma pancreático estejam associados a IPMNs. O aprimoramento das diretrizes pode impactar diretamente na detecção precoce e na sobrevida dos pacientes.
Pontos-chave
- O Protocolo de Kyoto 2024 reformulou a abordagem ao IPMN, priorizando critérios objetivos para indicação cirúrgica.
- O uso de nomogramas e avanços em EUS-FNA ampliaram a precisão diagnóstica.
- Critérios de descontinuidade de vigilância foram estabelecidos para pacientes com IPMNs pequenos e estáveis.
- O risco de PDAC concomitante exige monitoramento a longo prazo mesmo em lesões consideradas indolentes.
Conclusão
O manejo do IPMN requer uma abordagem multidisciplinar e individualizada. As novas diretrizes do Protocolo de Kyoto 2024 promovem um melhor refinamento na seleção de pacientes para cirurgia, minimizando riscos e otimizando resultados. Para o cirurgião digestivo, a compreensão detalhada dessas recomendações é essencial para um tratamento eficaz e baseado em evidências.
“A cirurgia pancreática não é apenas uma questão de técnica, mas de planejamento preciso, trabalho em equipe e respeito à biologia do tumor.” – Markus W. Büchler
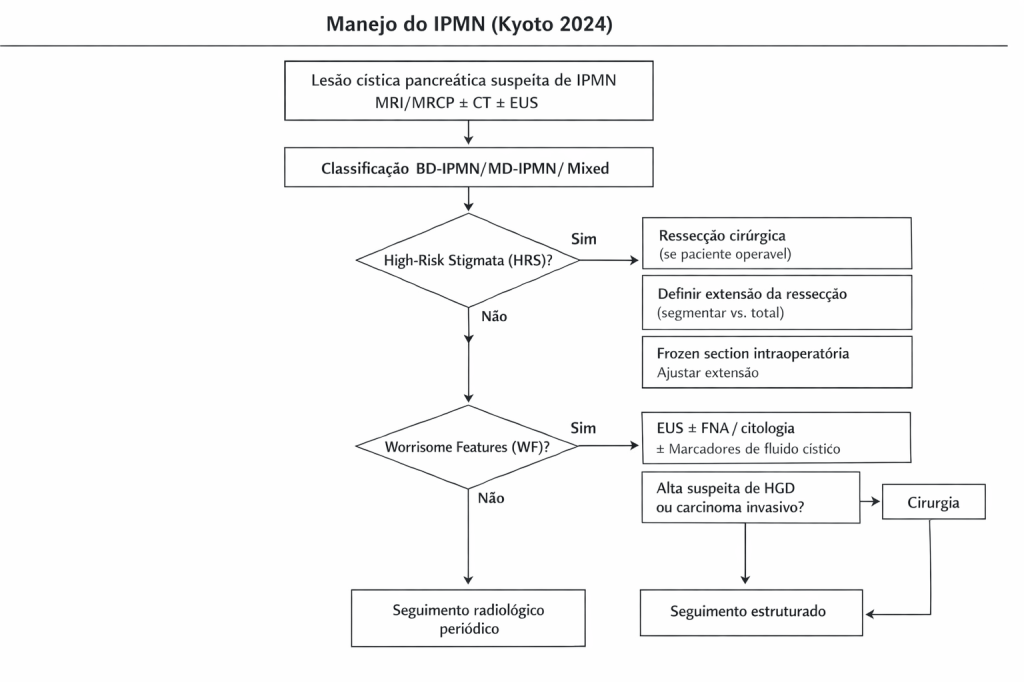
- Estigmas de alto risco (HRS): icterícia obstrutiva, nódulo mural ≥5 mm, dilatação do ducto pancreático principal ≥10 mm e citologia suspeita ou positiva.
- Características preocupantes (WF): crescimento acelerado (>2,5 mm/ano), cistos >30 mm, nódulos murais <5 mm, espessamento da parede cística, entre outros.
Gostou ❔Nos deixe um comentário ✍️, compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Qual a função do Apêndice Vermiforme?
Da Teoria Vestigial ao Protagonismo Imunológico e Microbiológico
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 12 minutos)
Introdução
Durante mais de um século, o apêndice vermiforme foi relegado ao status de um mero resquício evolutivo — um órgão vestigial, desprovido de função e célebre apenas pela sua capacidade de inflamar e exigir intervenção cirúrgica de urgência. No entanto, a medicina baseada em evidências e a compreensão profunda do trato gastrointestinal reescreveram esta narrativa. Longe de ser uma “sobra” anatômica, o apêndice é hoje reconhecido como uma estrutura morfofuncional de extrema relevância, atuando ativamente na imunidade mucosal e na regulação do microbioma intestinal. Para o estudante de medicina, o residente e o cirurgião do aparelho digestivo, compreender a anatomia, a fisiologia e o impacto a longo prazo da ressecção deste pequeno órgão tubular é fundamental para aprimorar o raciocínio clínico e refinar as indicações terapêuticas perante a suspeita de um abdome agudo inflamatório.
A Anatomia Cirúrgica do Apêndice
O conhecimento anatômico do apêndice é o mapa que guia o bisturi (ou o trocarte) na sala de operações.
1. Morfologia e Topografia
O apêndice vermiforme é uma projeção tubular cega que se origina na confluência das tênias colônicas, no ceco. Seu comprimento varia de 5 a 25 cm (média de 10 cm). Sua localização típica é na fossa ilíaca direita, topografada na superfície abdominal pelo ponto de McBurney (terço externo da linha imaginária entre a espinha ilíaca anterossuperior direita e a cicatriz umbilical). Contudo, a ponta do apêndice é como o ponteiro de um relógio, assumindo diversas posições:
- Retrocecal (mais comum – aprox. 65%): Oculto atrás do ceco, frequentemente simulando afecções renais ou dificultando o diagnóstico de peritonite precoce.
- Pélvico (aprox. 30%): Pode irritar a bexiga ou anexos uterinos.
- Subcecal, Pré ou Pós-ileal.
- Nota Cirúrgica: Em casos raros de má rotação intestinal ou situs inversus, o apêndice pode estar localizado no quadrante inferior esquerdo.
2. Vascularização e Inervação
A irrigação provém da artéria apendicular, um ramo terminal da artéria ileocólica (ramo da mesentérica superior), que transita na borda livre do mesoapêndice. Por ser uma artéria terminal, a oclusão da luz apendicular (por um fecalito) gera rápido ingurgitamento, trombose, isquemia e, subsequentemente, necrose e perfuração. A inervação, oriunda do plexo mesentérico superior (T10), explica a evolução clássica da dor na apendicite aguda: inicialmente dor visceral, difusa e periumbilical; que, com a progressão da inflamação para o peritônio parietal (inervação somática), migra e se localiza na fossa ilíaca direita.
A Mudança de Paradigma: Funções Funcionais (Microbioma e Imunidade)
A verdadeira revolução na compreensão do apêndice ocorreu no campo da imunologia e da microbiologia.
O “Refúgio Seguríssimo” (Safe House) do Microbioma
A mucosa apendicular é rica em biofilmes e serve como um autêntico “cofre” para as bactérias comensais (benéficas) do intestino. Durante infecções gastrointestinais severas, que resultam em diarreia profusa e “lavagem” da flora cólica, o apêndice mantém um reservatório seguro destas bactérias. Uma vez cessado o quadro agudo, este reservatório é utilizado para repovoar o cólon, restaurando a homeostase do microbioma de forma acelerada.
O Campo de Treinamento Imunológico
O apêndice é um componente vital do GALT (Gut-Associated Lymphoid Tissue). Ele contém uma densa rede de folículos linfoides e células M especializadas. Estas células capturam antígenos luminais e os apresentam aos linfócitos (Células T e B), orquestrando a resposta imune local (produção de IgA) e sistêmica. O apêndice atua como um órgão linfoide primário no desenvolvimento inicial e como um sentinela imune na vida adulta.
Aplicação na Cirurgia Digestiva e Implicações Clínicas
A apendicectomia continua sendo o procedimento cirúrgico de urgência mais realizado no mundo. Contudo, a ablação deste órgão carrega repercussões que a cirurgia moderna não pode mais ignorar.
1. Implicações da Apendicectomia a Longo Prazo
A remoção da “base de treinamento” imune e do reservatório microbiano altera a fisiologia intestinal. Estudos epidemiológicos recentes sugerem que a apendicectomia pode estar associada a um risco aumentado de desenvolvimento de:
- Síndrome do Intestino Irritável (SII): Devido à disbiose crônica (redução de bactérias protetoras, como o Butyricicoccus).
- Doenças Metabólicas e Autoimunes: Modulações na tolerância imunológica têm sido correlacionadas com maior incidência de Diabetes Mellitus tipo 2 e Lúpus.
- Risco Oncológico: Embora ainda exija mais robustez estatística, algumas coortes sugerem que a perda da vigilância imunológica (redução de células T CD3+ e CD8+ induzidas pelo apêndice) possa ter um papel na carcinogênese colorretal.
2. O Debate Contemporâneo: Cirurgia vs. Antibioticoterapia
Dado o seu papel funcional, extirpar o apêndice profilaticamente ou ao menor sinal de dor já não é consenso absoluto. A literatura recente, notavelmente o estudo CODA publicado no New England Journal of Medicine (NEJM, 2020), demonstrou que a antibioticoterapia exclusiva pode ser uma alternativa segura e eficaz em casos selecionados de apendicite aguda não complicada, evitando a cirurgia e preservando o órgão em uma parcela significativa dos pacientes. Cabe ao cirurgião avaliar criteriosamente a presença de fecalitos (que predizem falha do tratamento clínico) e o risco de ruptura.
Pontos-Chave para a Prática Diária
- Não é Vestigial: O apêndice é um órgão linfoide ativo e um modulador essencial do microbioma e da imunidade mucosal.
- A Anatomia Dita a Clínica: A variação na posição da ponta do apêndice (retrocecal, pélvica) é a principal causa de apresentações clínicas atípicas que atrasam o diagnóstico cirúrgico.
- A Isquemia é Precoce: Por ser irrigado por uma artéria terminal (a. apendicular), a obstrução luminal rapidamente evolui para gangrena e perfuração se não diagnosticada.
- Reservatório Protetor: O apêndice atua como um “safe house” bacteriano, acelerando a recuperação do cólon após infecções entéricas severas.
- Apendicectomia tem Preço Fisiológico: A remoção não é isenta de consequências a longo prazo, predispondo a disbiose, SII e possíveis disfunções imunológicas.
- Tratamento Conservador: O manejo não operatório com antibióticos da apendicite não complicada é uma realidade baseada em evidências que deve constar no arsenal terapêutico do cirurgião moderno.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
A apendicectomia — preferencialmente por via laparoscópica — permanecerá como o esteio do tratamento da apendicite aguda, salvando inúmeras vidas de peritonites letais. No entanto, o cirurgião do aparelho digestivo do século XXI deve abandonar a visão mecanicista e adotar uma perspectiva fisiológica. Considerar o tratamento antimicrobiano exclusivo em casos iniciais e não complicados não é uma heresia cirúrgica, mas sim o reconhecimento do valor morfofuncional do apêndice. Além disso, a vigilância clínica a longo prazo dos pacientes apendicectomizados, monitorando o desenvolvimento de disbiose ou patologias colorretais, deve ser encorajada. Conhecer a fundo a biologia daquilo que operamos é o que separa o mero “operador” do verdadeiro médico cirurgião.
A Anatomia Cirúrgica do Apêndice
O conhecimento anatômico do apêndice é o mapa que guia o bisturi (ou o trocarte) na sala de operações.
1. Morfologia e Topografia
O apêndice vermiforme é uma projeção tubular cega que se origina na confluência das tênias colônicas, no ceco. Seu comprimento varia de 5 a 25 cm (média de 10 cm). Sua localização típica é na fossa ilíaca direita, topografada na superfície abdominal pelo ponto de McBurney (terço externo da linha imaginária entre a espinha ilíaca anterossuperior direita e a cicatriz umbilical). Contudo, a ponta do apêndice é como o ponteiro de um relógio, assumindo diversas posições:
- Retrocecal (mais comum – aprox. 65%): Oculto atrás do ceco, frequentemente simulando afecções renais ou dificultando o diagnóstico de peritonite precoce.
- Pélvico (aprox. 30%): Pode irritar a bexiga ou anexos uterinos.
- Subcecal, Pré ou Pós-ileal.
- Nota Cirúrgica: Em casos raros de má rotação intestinal ou situs inversus, o apêndice pode estar localizado no quadrante inferior esquerdo.
2. Vascularização e Inervação
A irrigação provém da artéria apendicular, um ramo terminal da artéria ileocólica (ramo da mesentérica superior), que transita na borda livre do mesoapêndice. Por ser uma artéria terminal, a oclusão da luz apendicular (por um fecalito) gera rápido ingurgitamento, trombose, isquemia e, subsequentemente, necrose e perfuração. A inervação, oriunda do plexo mesentérico superior (T10), explica a evolução clássica da dor na apendicite aguda: inicialmente dor visceral, difusa e periumbilical; que, com a progressão da inflamação para o peritônio parietal (inervação somática), migra e se localiza na fossa ilíaca direita.
3. Resumo Prático da Anatomia Apendicular
Para uma consulta rápida e direcionada à prática cirúrgica, eis a síntese estrutural do apêndice:
- Forma e Dimensões: Estrutura tubular cega, medindo em média 10 cm de comprimento.
- Base Anatômica: Origina-se invariavelmente na confluência das três tênias colônicas no ceco.
- Posição da Ponta: Mais frequentemente retrocecal (65%) ou pélvica (30%).
- Referência de Superfície: Ponto de McBurney (fossa ilíaca direita).
- Irrigação Sanguínea: Artéria apendicular (artéria terminal; o que favorece isquemia precoce em casos de obstrução).
- Inervação Autonômica: Segmento T10, justificando a dor periumbilical referida na fase inicial da inflamação.
“A medicina é uma arte, não uma ciência exata.” — William Osler. A compreensão contínua das funções do apêndice e a evolução das abordagens terapêuticas refletem a natureza dinâmica da prática médica, onde novas evidências moldam as decisões clínicas e cirúrgicas.
Gostou ❔Nos deixe um comentário ✍️, compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
“Aleijados Biliares”
O Flagelo Silencioso da Lesão do Ducto Biliar na Colecistectomia Laparoscópica
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 8 minutos)

Introdução
No âmbito da cirurgia digestiva, poucas complicações causam tanto temor aos cirurgiões quanto a lesão do ducto biliar (LDB) durante a colecistectomia laparoscópica. Apesar de ser o procedimento padrão-ouro para o tratamento da colelitíase sintomática, esta intervenção carrega um perigo oculto que pode transformar uma operação de rotina num evento devastador, alterando irreversivelmente a vida tanto do doente quanto do cirurgião — criando o que a literatura clássica tragicamente apelida de “aleijados biliares”.
O Paradoxo Laparoscópico e o Impacto Socioeconómico
A colecistectomia laparoscópica, introduzida no final da década de 1980, revolucionou a cirurgia da vesícula biliar, proporcionando recuperações mais rápidas e menor dor pós-operatória. No entanto, trouxe consigo um risco aumentado de LDB em comparação com a abordagem aberta tradicional. Dados de um estudo do Colégio Brasileiro de Cirurgiões relataram uma taxa de LDB de 0,18% em colecistectomias laparoscópicas, um valor ligeiramente inferior à média global que oscila entre 0,3% e 0,7%. Contudo, as consequências da LDB são de uma gravidade extrema. Frequentemente exigem cirurgia reconstrutiva complexa (como a hepaticojejunostomia em Y de Roux) e resultam em significativa morbilidade, mortalidade e custos de saúde astronómicos. Um estudo brasileiro estimou que os casos de LDB conduzem a uma média de 22 dias adicionais de internamento hospitalar e a um aumento de 30 vezes nos custos hospitalares associados.
Pontos-Chave na Prevenção e Gestão da LDB
Para mitigar este flagelo, a abordagem cirúrgica deve assentar em quatro pilares fundamentais:
1. Fatores de Risco
Compreender e antecipar os fatores relacionados com o doente (ex: colecistite aguda, obesidade grave, variações anatómicas) e com o cirurgião (ex: inexperiência, fadiga, interpretação errónea da anatomia ou “ilusão de ótica” cirúrgica) é absolutamente crucial para o planeamento operatório.
2. Estratégias de Prevenção Inegociáveis
- Visão Crítica de Segurança (CVS): Esta técnica de identificação anatómica, defendida pelo Dr. Steven Strasberg, é a pedra basilar na prevenção da LDB. Exige a limpeza do triângulo hepatocístico, a separação do terço inferior da vesícula da placa cística e a visualização de apenas duas estruturas a adentrar a vesícula.
- Colangiografia Intraoperatória (CIO): Embora ainda alvo de algum debate quanto à sua utilização universal, a CIO é uma ferramenta valiosa que pode auxiliar de forma decisiva na identificação da anatomia biliar e no diagnóstico precoce de lesões.
- “Cultura de Segurança”: É imperativo adotar uma mentalidade que priorize a segurança do doente acima da conclusão do procedimento por via laparoscópica a todo o custo. A conversão para cirurgia aberta ou a realização de uma colecistectomia subtotal são sinais de maturidade cirúrgica, e nunca de fracasso.
3. Reconhecimento e Manejo Adequado
O reconhecimento precoce da LDB, preferencialmente no período intraoperatório, é vital. O reencaminhamento atempado e o reparo imediato ou diferido realizado por cirurgiões hepatobiliares experientes e dedicados proporcionam, inequivocamente, os melhores resultados a longo prazo.
4. Formação e Educação Médica Contínua
O treino baseado em simulação e a adoção de protocolos padronizados de segurança devem fazer parte da matriz formativa de qualquer serviço, ajudando a reduzir de forma drástica as taxas de LDB, especialmente entre os médicos internos (residentes) de cirurgia geral e digestiva.
Conclusões Aplicadas
Como cirurgiões digestivos, devemos permanecer em vigilância constante contra a ameaça da lesão do ducto biliar. Ao aderirmos de forma obstinada às técnicas cirúrgicas adequadas, mantendo um elevado índice de suspeição e fomentando uma cultura de segurança inabalável, podemos minimizar esta complicação potencialmente devastadora. A jornada para o “zero LDB” está em andamento, exigindo educação contínua, autorreflexão e um compromisso diário com a excelência na nossa prática.
“O desafio da cirurgia é a mão do cirurgião curar um doente pela precisão na estrutura e propósito.” – Joseph E. Murray, cirurgião plástico, pioneiro dos transplantes e Prémio Nobel da Medicina.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe nas suas redes sociais e|ou mande a sua dúvida pelo 💬 Chat On-line na nossa DM do Instagram.
Visão Crítica de Segurança
A Visão Crítica de Segurança na Colecistectomia Laparoscópica: O Padrão-Ouro na Prevenção de Lesões da Via Biliar
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 9 minutos)
Introdução
A colecistectomia laparoscópica é, indiscutivelmente, um dos procedimentos cirúrgicos mais realizados no mundo. No Brasil, dados do Departamento de Informática do SUS (DATASUS) revelam que mais de 200.000 colecistectomias são realizadas anualmente apenas no sistema público de saúde. Apesar da padronização técnica e da vasta experiência acumulada nas últimas três décadas, a lesão iatrogênica da via biliar principal (VBP) permanece como uma das complicações mais devastadoras da cirurgia digestiva contemporânea. Com uma incidência que varia de 0,3% a 0,5% na era laparoscópica (uma taxa superior à antiga era da cirurgia aberta), a lesão biliar acarreta morbidade severa, mortalidade não negligenciável e um imenso custo médico-legal. Para o estudante de medicina, o residente de cirurgia geral e o cirurgião do aparelho digestivo, a mitigação desse risco não se baseia na sorte, mas na adesão obstinada a uma filosofia de identificação anatômica: a Visão Crítica de Segurança (CVS – Critical View of Safety).
A Anatomia da Prevenção
Introduzida em 1995 pelo Dr. Steven Strasberg, a Visão Crítica de Segurança não é um método de dissecção per se, mas sim um método rigoroso de identificação de alvos. A grande armadilha da cirurgia biliar é a ilusão de ótica: a tração inadequada ou a inflamação severa podem fazer com que o ducto colédoco ou o ducto hepático comum sejam mimetizados e confundidos com o ducto cístico. Para declarar que a Visão Crítica de Segurança foi alcançada, três critérios obrigatórios e simultâneos devem ser rigorosamente preenchidos antes da aplicação de qualquer clipe cirúrgico ou energia:
- Limpeza do Triângulo Hepatocístico: O triângulo hepatocístico (delimitado pelo ducto cístico, ducto hepático comum e a borda inferior do fígado) deve ser completamente limpo de tecido adiposo e fibroso. Ressalta-se que a dissecção ocorre no triângulo hepatocístico, e não apenas no Triângulo de Calot clásico.
- Exposição da Placa Cística (Leito Hepático): O terço inferior (infundíbulo) da vesícula biliar deve ser completamente dissecado e separado do leito hepático (placa cística). Esta manobra comprova que as estruturas dissecadas estão, de fato, indo em direção exclusiva à vesícula.
- Apenas Duas Estruturas Adentrando a Vesícula: Somente o ducto cístico e a artéria cística devem ser vistos penetrando a vesícula biliar. Nenhuma outra estrutura tubular deve estar presente no campo dissecado.
Aplicação na Cirurgia Digestiva: Estratégias e Armadilhas
Alcançar a CVS exige técnica padronizada e conhecimento das armadilhas anatômicas e inflamatórias:
- Dinâmica de Tração: A tração dita a anatomia. O fundo da vesícula deve ser tracionado em direção cefálica (em direção ao ombro direito), enquanto o infundíbulo deve ser tracionado lateralmente e para baixo. Esta “tração em duas vias” abre o ângulo entre o ducto cístico e o colédoco, evitando a perigosa distorção anatômica (o alinhamento do ducto cístico paralelo ao colédoco).
- Dissecção Começando pelo Infundíbulo: A dissecção deve iniciar na transição entre o infundíbulo e o ducto cístico, mantendo-se sempre rente à parede da vesícula. Afastar-se da vesícula em direção ao hilo hepático é o caminho mais curto para o desastre.
- O Momento de Parar (Bailout Procedures): Em casos de colecistite aguda severa, síndrome de Mirizzi ou fibrose intensa (vesícula escleroatrófica), alcançar a CVS pode ser impossível ou excessivamente perigoso. O cirurgião maduro reconhece este limite. Nestes cenários, a conversão para cirurgia aberta ou a realização de uma colecistectomia subtotal (fenestrada ou reconstituída) são atitudes de extrema sabedoria cirúrgica, não de fracasso.
Pontos-Chave para a Prática Diária
- Pausa Estratégica (Time-Out): Antes de aplicar os clipes, o cirurgião e o primeiro assistente devem verbalizar e confirmar visualmente, de forma independente, que os três critérios da CVS foram atingidos (frente e verso da vesícula).
- Documentação Fotográfica: Registrar a CVS (fotografia ou vídeo) antes da clipagem é uma excelente prática de gestão de risco e proteção jurídica, documentando a adesão aos padrões de segurança (Lex Artis).
- Colangiografia Intraoperatória (CIO): A CVS e a CIO não são excludentes, mas complementares. Se a anatomia permanecer confusa mesmo após a dissecção, a CIO ou a ultrassonografia intraoperatória devem ser realizadas para mapear a árvore biliar.
Conclusões Aplicadas
A excelência na cirurgia do aparelho digestivo não é definida pela velocidade com que um procedimento é concluído, mas pela consistência da segurança entregue ao paciente. A adoção universal e compulsória da Visão Crítica de Segurança transformou o que outrora era um dogma anatômico flexível em uma diretriz irrevogável. Para o jovem cirurgião, introjetar a filosofia da CVS significa compreender que, frente à inflamação biliar, a humildade e a paciência são os instrumentos mais afiados da bandeja cirúrgica. A prevenção da lesão biliar é, e sempre será, a marca do verdadeiro mestre.
“A Visão Crítica de Segurança não é apenas uma técnica de dissecção, mas sim um método definitivo de identificação de alvos. Na cirurgia biliar, nós não presumimos a anatomia; nós a provamos inequivocamente antes de cortar.” — Adaptado dos ensinamentos de Dr. Steven Strasberg, cirurgião que conceituou a Visão Crítica de Segurança em 1995.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.


Colecistectomia Subtotal
Uma Abordagem Segura para Situações Complexas
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 9 minutos)
Introdução
A colecistectomia laparoscópica é o procedimento padrão-ouro para o tratamento da litíase biliar sintomática. No entanto, o cirurgião do aparelho digestivo que atua nas emergências brasileiras frequentemente se depara com o “abdome hostil”. Dados do Ministério da Saúde demonstram que uma parcela expressiva das internações cirúrgicas de urgência no SUS deve-se a quadros de colecistite aguda grave, muitas vezes com evolução de vários dias, resultando em intensa inflamação, fibrose e distorção anatômica do hilo hepático. Quando o Triângulo de Calot se torna um bloco fibrótico impenetrável — o chamado frozen Calot —, a insistência em realizar uma colecistectomia total clássica aumenta exponencialmente o risco de lesão iatrogênica da via biliar principal e de vasos hepáticos. Neste cenário crítico, a Colecistectomia Subtotal (CS) ressurge não como um sinal de fracasso ou imperícia, mas como uma manobra tática de extrema sabedoria cirúrgica (bailout procedure) para garantir a segurança e a vida do paciente.
Indicações e a Classificação da Técnica
A indicação primária para a colecistectomia subtotal é a impossibilidade de se alcançar com segurança a Visão Crítica de Segurança (CVS) de Strasberg. Isso ocorre classicamente em casos de colecistite aguda gangrenosa, colecistite xantogranulomatosa, cirrose hepática com hipertensão portal (risco de sangramento incontrolável no leito hepático) e na Síndrome de Mirizzi.
Historicamente, a cirurgia subtotal pode ser dividida em duas abordagens principais, conforme a intenção do cirurgião em relação ao remanescente infundibular:
- Colecistectomia Subtotal Reconstituída: A parede anterior da vesícula é ressecada e o remanescente infundibular é suturado (fechado), criando uma “neo-vesícula”. Embora reduza o risco de fístula biliar pós-operatória, esta técnica carrega um risco maior de recorrência de cálculos e colecistite no coto residual a longo prazo.
- Colecistectomia Subtotal Fenestrada: O infundíbulo é deixado aberto. O cirurgião remove todos os cálculos, fulgura a mucosa da parede posterior (que permanece aderida ao fígado para evitar sangramento) e pode ou não tentar ocluir o orifício do ducto cístico por dentro. Um dreno de demora é mandatoriamente posicionado. A vantagem é a menor taxa de recorrência de sintomas, embora a fístula biliar (geralmente autolimitada) seja uma ocorrência comum e esperada.
Aplicação na Cirurgia Digestiva: Aspectos Técnicos
A execução de uma colecistectomia subtotal segura exige padronização técnica:
- Incisão da Vesícula: Após a constatação do risco no hilo, a vesícula deve ser incisada no fundo ou no corpo, longe das estruturas nobres. O conteúdo purulento e a bile devem ser aspirados.
- Remoção dos Cálculos: É imperativo retirar todos os cálculos, com atenção especial àqueles impactados na bolsa de Hartmann, utilizando pinças extratoras ou lavagem exaustiva. Um cálculo residual fatalmente perpetuará o processo inflamatório ou causará fístula crônica.
- Tratamento da Mucosa Remanescente: A parede posterior da vesícula, deixada aderida ao leito hepático, possui mucosa secretora. Esta deve ser ablacionada utilizando eletrocautério de argônio ou cautério monopolar potente para destruir o epitélio e reduzir a secreção.
- Manejo do Orifício Cístico: Tentar identificar o óstio do ducto cístico por visão intraluminal e fechá-lo com sutura em bolsa ou em “Z” (fio absorvível) é desejável. Se não for possível identificá-lo com clareza devido à inflamação, não se deve realizar suturas “às cegas”. Instala-se um dreno tubular de sistema fechado próximo à abertura fenestrada e encerra-se o procedimento.
Pontos-Chave para a Prática Diária
- Maturidade Cirúrgica: Converter para via aberta ou optar pela colecistectomia subtotal são decisões que refletem o respeito do cirurgião pela anatomia. O princípio de Hipócrates, Primum non nocere (Primeiro, não fazer mal), deve guiar o raciocínio no centro cirúrgico.
- Consentimento Informado: Em pacientes com alto risco preditivo para frozen Calot, a possibilidade de uma cirurgia subtotal deve ser discutida no pré-operatório.
- Pós-Operatório e CPRE: Em casos de colecistectomia fenestrada com fístula biliar de alto débito ou persistente por mais de 2 a 3 semanas, a realização de uma Colangiopancreatografia Retrógrada Endoscópica (CPRE) para papilotomia e/ou passagem de stent biliar resolve a fístula na esmagadora maioria dos casos, reduzindo a pressão no ducto e facilitando o fechamento do coto.
Conclusões Aplicadas
A Colecistectomia Subtotal é uma ferramenta indispensável no arsenal do cirurgião do aparelho digestivo. Em meio à “tempestade perfeita” da inflamação biliar severa, ela atua como um porto seguro, prevenindo o dano catastrófico às vias biliares e aos vasos hepáticos. Compreender as nuances entre as técnicas fenestrada e reconstituída permite individualizar o tratamento conforme os achados intraoperatórios. Cabe aos preceptores das residências médicas desmistificarem a cirurgia subtotal, ensinando aos cirurgiões em formação que, na complexidade do abdome hostil, a preservação da integridade estrutural do paciente vale muito mais do que a ressecção anatômica completa do órgão.
“A grandeza de um cirurgião não se mede apenas pela excelência com que realiza uma ressecção completa, mas fundamentalmente pelo discernimento e pela humildade de saber o momento exato de parar.” — William J. Mayo, um dos fundadores da Mayo Clinic, cujos ensinamentos perpetuam o valor da prudência na prática cirúrgica.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Colecistectomia Segura: Plano R4U
O Imperativo do Sulco de Rouvière e a Visão Crítica de Segurança
Autor: Prof. Dr. Ozimo Gama
Afiliação: Membro Titular do Colégio Brasileiro de Cirurgiões
Membro Titular do Colégio Brasileiro de Cirurgia Digestiva
Introdução
A colecistectomia laparoscópica (CL) permanece como um dos procedimentos cirúrgicos mais executados globalmente. No entanto, sua ubiquidade não mitiga riscos inerentes; a variação anatômica dos ductos biliares, combinada à identificação visual incorreta, continua a precipitar complicações graves, notadamente as lesões iatrogênicas das vias biliares[1]. Neste cenário, a segurança do paciente transcende a destreza manual, residindo na identificação rigorosa de marcos anatômicos imutáveis. Entre estes, o sulco de Rouvière (SR) emerge não apenas como detalhe morfológico, mas como farol essencial para a orientação cirúrgica segura[2].
A Nomenclatura e a Realidade Anatômica
A precisão cirúrgica exige precisão anatômica. Na literatura, o SR é referenciado sob diversas nomenclaturas, incluindo “incisura dextra de Gans”[7] e, originalmente por Henri Rouvière, como “le sillon du processus caudé”[5]. Embora textos clássicos apresentem dados inconsistentes, estudos contemporâneos demonstram a presença do SR em até 80% dos fígados[3,6]. Tal prevalência torna o reconhecimento deste marco uma competência obrigatória. A relevância topográfica do SR é crítica, estabelecendo um divisor de águas anatômico: o ducto e a artéria cística localizam-se anterossuperiormente ao sulco, enquanto o ducto biliar comum (CBD) reside abaixo do seu nível. Evidências sugerem que dissecções iniciadas ventralmente ao SR reduzem significativamente a incidência de lesões ao CBD[2]. Ademais, o marco é instrumental para a execução segura de ressecções hepáticas segmentares[4].
A Integração com a Visão Crítica de Segurança (CVS)
A técnica da Critical View of Safety (CVS), preconizada por Strasberg, é o padrão ouro para minimizar riscos de lesão biliar[1]. Contudo, a aplicação da CVS deve ser ancorada em marcos confiáveis. Variações da árvore biliar extra-hepática afetam até um terço dos pacientes[3], mas o SR tende a manter-se no mesmo plano do ducto hepático comum e do CBD, facilitando a orientação tridimensional. A identificação do SR deve ser o passo preliminar que habilita a construção segura da CVS, mormente em casos de anatomia distorcida por inflamação.
Estratégias de Contingência: A Linha R4U
Em casos onde o SR está obscurecido por fibrose ou aderências, a segurança não pode ser comprometida. A linha R4U — estendendo-se da fissura umbilical para a direita do hilo — apresenta-se como alternativa viável para delimitar um plano seguro de dissecção[2]. Todavia, a utilização eficaz da linha R4U exige profundo conhecimento da anatomia hepática e treinamento contínuo em técnicas de segurança.
Conclusão
A prevenção de lesões na CL exige uma sistematização que transcende a técnica básica. A identificação rotineira do Sulco de Rouvière e a adesão estrita à CVS são imperativos éticos e técnicos. Ao integrar o conhecimento anatômico clássico com estratégias modernas, elevamos o padrão de cuidado. Como nos lembra a sabedoria cirúrgica secular:
“O cirurgião que ignora a anatomia esculpe o corpo humano como um cego esculpe a madeira.” — Guy de Chauliac (1300–1368), Chirurgia Magna.
Referências Bibliográficas
Referências
- Strasberg, S. M., et al. “The Critical View of Safety in Laparoscopic Cholecystectomy.”
- Hugh, T. B. “Anatomical Landmarks for Safe Laparoscopic Cholecystectomy.”
- Zubair, M., et al. “Anatomical Variations in the Extrahepatic Biliary Tree.”
- Couinaud, C. “Segmental Anatomy of the Liver.”
- Rouvière, H. “Le sillon du processus caudé.”
- Reynaud, C., Coucoravas, G., Giuly, J., et al. “Incisura Dextra de Gans.”
- Hugh, T. B. “Minimal Common Bile Duct Injury During Laparoscopic Cholecystectomy.”
- Gans, H. “Incisura Dextra in Classic Anatomical Literature.”
O Legado do Dr. William Stewart Halsted
Pioneiro da Cirurgia Moderna
A história da medicina é marcada por avanços revolucionários que transformaram a prática clínica, o ensino e os cuidados aos pacientes. Entre os nomes que se destacam neste cenário, o do cirurgião norte-americano William Stewart Halsted (1852–1922) é, sem dúvidas, um dos mais influentes. Halsted não apenas elevou os padrões da cirurgia, mas também criou um modelo de treinamento que se tornou a base para a formação de cirurgiões em todo o mundo, com aplicações diretas no tratamento das doenças do aparelho digestivo.
O Início de uma Jornada Brilhante
Nascido em Nova York, Halsted iniciou sua formação acadêmica com forte ênfase em anatomia e fisiologia, que mais tarde se tornariam a base de suas contribuições à medicina. Após se formar na College of Physicians and Surgeons, em 1877, ele ampliou seus horizontes ao estudar em centros de excelência europeus, como Viena e Hamburgo, onde foi influenciado por cirurgiões renomados como Theodor Billroth e Johannes von Mikulicz.
Contribuições ao Tratamento Cirúrgico do Aparelho Digestivo
Entre os muitos campos em que Halsted deixou sua marca, destaca-se a cirurgia do aparelho digestivo. Seu estudo experimental sobre suturas intestinais, realizado no início de sua carreira em Baltimore, estabeleceu as bases para anastomoses seguras e eficazes. Ele demonstrou que a submucosa é a camada crítica para sustentação das suturas, um conceito que permanece fundamental até hoje. Outro marco foi seu pioneirismo em ressecções gastrointestinais e controle de sangramentos intra-abdominais. Sua abordagem técnica, caracterizada por dissecação cuidadosa e manuseio gentil dos tecidos, minimizou complicações como infecção e deiscências, ampliando significativamente as chances de sucesso em cirurgias de alta complexidade.
O Modelo Halstediano de Treinamento Cirúrgico
Um dos legados mais duradouros de Halsted foi seu modelo de residência médica, implementado no Hospital Johns Hopkins. Ele estabeleceu um sistema hierárquico com responsabilidades graduais, permitindo que residentes desenvolvessem habilidades progressivamente. Esse método não apenas garantiu um treinamento mais completo, mas também formou líderes que perpetuaram suas ideias. Para a cirurgia do aparelho digestivo, essa abordagem foi crucial. O treinamento intensivo em anatomia, fisiopatologia e técnicas operatórias sofisticadas possibilitou avanços significativos no manejo de doenças como cânceres gastrointestinais, doenças inflamatórias intestinais e patologias biliares.
Avanços e a Influência no Ensino Moderno
Embora o modelo Halstediano tenha sido modificado ao longo das décadas, seus princípios básicos continuam sendo a espinha dorsal da educação cirúrgica. Programas atuais incorporam avanços tecnológicos, como cirurgia robótica e simulações, mas a ética da responsabilidade progressiva e a atenção aos detalhes, promovida por Halsted, permanecem inalteradas.

Reflexão Final
O legado de William Stewart Halsted é inestimável. Suas contribuições estabeleceram os alicerces da cirurgia moderna, com implicações diretas na melhora do cuidado ao paciente e na educação médica. Para estudantes e residentes, entender sua história é compreender as origens de muitas práticas e conceitos que hoje são considerados padrão na formação e prática cirúrgica.
“A grandeza de um cirurgião não reside apenas em suas habilidades técnicas, mas na sua dedicação contínua em aprimorar a arte de curar.” – William Stewart Halsted.
Gostou ❔ Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#CirurgiaDigestiva #EducaçãoMédica #HistóriaDaCirurgia #ResidênciaMédica #WilliamHalsted
Michelangelo Buonarroti
5 Segredos de Anatomia Escondidos na Capela Sistina: A Neuroanatomia Clandestina de Michelangelo
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 10 minutos)
Onde a Fé e o Bisturi se Encontram
Na formação médica contemporânea, o estudo da anatomia topográfica num laboratório de dissecação é o rito de passagem fundamental para qualquer cirurgião. No Brasil, apesar dos desafios atuais na captação de cadáveres para estudo nas faculdades de medicina, a dissecação continua a ser a base insubstituível da técnica cirúrgica. Contudo, no século XVI, o estudo do corpo humano além da superfície era um tabu severo, vigiado de perto pelas leis civis e canónicas. Michelangelo Buonarroti, celebrado mundialmente pela sua terribilità — aquela força emocional e técnica avassaladora —, viveu um paradoxo perigoso. O artista profundamente religioso era também um anatomista clandestino. Desafiando os dogmas de sua época, ele dedicou inúmeras noites à dissecação de cadáveres, buscando nos tendões, fáscias e vísceras a geometria da perfeição biológica. O que a humanidade demorou 500 anos para perceber é que Michelangelo não utilizou este conhecimento apenas para conferir realismo hipertrófico às suas figuras; ele codificou verdadeiras lições de neuroanatomia diretamente no teto da Capela Sistina. O santuário do conclave papal guarda um mapa do intelecto humano, sugerindo que a verdadeira centelha divina reside na intrincada arquitetura do sistema nervoso central. Abaixo, dissecamos os 5 segredos anatómicos ocultos nesta obra-prima.
A Anatomia Oculta nos Afrescos
1. O Cérebro como a “Faísca Divina” em A Criação de Adão
Em 1990, o médico norte-americano Frank Meshberger publicou uma descoberta no prestigiado Journal of the American Medical Association (JAMA) que alterou o curso da história da arte e da medicina. Ele demonstrou que a figura de Deus, envolta num manto avermelhado e cercada por anjos, compõe um corte sagital milimetricamente exato de um cérebro humano. A genialidade reside nos detalhes: o contorno inferior do manto segue com precisão o sulco lateral (Fissura de Sylvius). O braço estendido do Criador atravessa exatamente o giro do cíngulo. Um “anjo” posicionado inferiormente desenha o trajeto da artéria basilar, enquanto o pé bifurcado de um querubim representa a glândula pituitária (hipófise). Para Michelangelo, o que Adão recebe no toque não é apenas o fôlego biológico, mas o intelletto — a razão suprema.
2. O Tronco Encefálico no Pescoço de Deus
A análise de A Criação de Adão revela o cérebro macroscópico, mas o painel central A Separação da Luz das Trevas aprofunda-se em estruturas neurais complexas. Em 2010, os investigadores Ian Suk e Rafael Tamargo, neurocirurgiões da Universidade Johns Hopkins, identificaram um detalhe audacioso. O pescoço de Deus exibe uma anatomia irregular que foge à hipertrofia muscular renascentista padrão. Utilizando um escorço dramático (técnica de perspetiva que encurta a figura), Michelangelo camuflou uma visão ventral do tronco encefálico humano. Estão lá, representados com rigor de atlas cirúrgico, o bulbo, a ponte e a estrutura em forma de “Y” característica dos nervos óticos e do quiasma ótico.
3. Arquitetura Neural: Ventrículos e o Corpo Caloso
A investigação ganhou novos contornos em 2015, quando Ciurea et al. identificaram como o mestre utilizou a técnica do chiaroscuro (luz e sombra) aplicando o princípio da Gestalt para ocultar formas. Na mesma cena da Separação da Luz das Trevas, os olhos treinados de um neuroanatomista conseguem completar as figuras:
- Área A: O quarto ventrículo perfeitamente delineado.
- Área B: A ponte de Varólio, formada pela curvatura da coxa direita da divindade, exibindo a oliva pontina e o sulco colateral anterior.
- Área C: O manto superior que emula uma imagem espelhada do corpo caloso (a via de comunicação entre os hemisférios cerebrais). A inversão da imagem serviu para manter o fluxo estético sem perder a mensagem anatómica.
4. O Anatomista Clandestino de Santo Spirito
Para que um artista atingisse tal nível de detalhe no século XVI — superando as obras de Galeno (que se baseavam em dissecações de macacos e porcos) —, a observação clínica superficial não bastaria. Aos 18 anos, Michelangelo firmou um acordo secreto com o prior da Igreja de Santo Spirito, em Florença. Em troca da escultura de um crucifixo de madeira, o prior permitia-lhe dissecar cadáveres humanos no hospital da igreja durante a madrugada. armado com um bisturi primitivo, ele antecipou descobertas que a medicina oficial, com Andreas Vesalius, só documentaria décadas mais tarde.
5. Uma Mensagem de Protesto e Subversão (A Costela Oculta)
O anatomista era também um livre-pensador influenciado pelo Neoplatonismo florentino. O investigador Deivis Campos (2019) identificou uma “costela extra” no lado esquerdo do torso de Adão. Ao invés de pintar uma costela a ser removida para a criação de Eva (como ditava o dogma), Michelangelo pintou uma costela extra e oculta. Esta representação anatómica subversiva sugere que as essências feminina e masculina coexistem na natureza humana original, uma alusão ao misticismo da Cabala e um protesto velado contra a interpretação literal das escrituras.
Pontos-Chave para a Formação Médica
- A Observação é a Base da Medicina: O génio de Michelangelo prova que a capacidade de observar minuciosamente a anatomia é o que separa o conhecimento superficial da verdadeira maestria.
- Integração Arte e Ciência: As estruturas neurais (fissura de Sylvius, tronco encefálico, quiasma ótico) pintadas no século XVI mostram que a medicina e a arte nasceram da mesma curiosidade intrínseca sobre o milagre da vida.
- O Cérebro como Sede da Consciência: Ao colocar o sistema nervoso central no epicentro do ato da Criação, Michelangelo antecipou em séculos a premissa da neurociência moderna: somos o nosso cérebro.
Conclusões Aplicadas à Prática do Cirurgião
Para o cirurgião do aparelho digestivo, ou de qualquer outra especialidade, a história de Michelangelo traz uma lição de humildade e reverência. Quando entramos no centro cirúrgico e realizamos uma incisão, não estamos apenas a manipular tecidos e órgãos; estamos a interagir com a mais sublime e complexa arquitetura do universo conhecido. Se o maior segredo do Renascimento — o mapeamento do nosso intelecto na morada do papado — permaneceu oculto por cinco séculos à vista de todos, devemos questionar-nos diariamente: o que mais estamos a falhar em enxergar nos nossos doentes devido à pressa ou à desatenção clínica? A medicina de excelência exige o olhar crítico do cientista e a sensibilidade meticulosa do artista.
“Onde o espírito não conduz a mão do artista, não há arte. E onde o conhecimento da anatomia não conduz a mão do médico, não há cura. A estrutura do corpo humano é a obra-prima inquestionável do Criador.” — Adaptado dos pensamentos do Renascimento Médico.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Aula de Anatomia do Dr Nicolaes Tulp (1632)
O valor da obra “A Aula de Anatomia do Dr. Nicolaes Tulp” é incalculável, pois ela pertence ao acervo do Mauritshuis, em Haia, na Holanda, e é considerada uma das mais importantes e valiosas obras do museu. Além disso, a pintura é uma das mais famosas obras de Rembrandt e uma das mais importantes do período Barroco holandês. Por isso, é considerada uma obra-prima da arte ocidental e tem um valor histórico, artístico e cultural inestimável. Embora não haja um valor monetário exato para a pintura, pode-se dizer que é uma das obras mais valiosas e procuradas do mundo da arte, tanto pelo seu significado histórico quanto pela sua qualidade artística.
“A Aula de Anatomia do Dr. Nicolaes Tulp” é uma pintura a óleo sobre tela, criada por Rembrandt van Rijn em 1632. A obra mede 169,5 cm x 216,5 cm e está atualmente exposta no Mauritshuis, em Haia, na Holanda. A composição da pintura apresenta um grupo de homens em torno de uma mesa de dissecação, liderados pelo médico Nicolaes Tulp, que está realizando uma demonstração de anatomia. O corpo sendo dissecado é o de um criminoso enforcado chamado Aris Kindt. A composição apresenta uma disposição simétrica e organizada das figuras em torno da mesa, com Tulp no centro da imagem.
A luz na pintura é focada no corpo sendo dissecado, destacando-o em relação ao fundo escuro da sala. A técnica de chiaroscuro usada por Rembrandt acentua o realismo e o drama da cena. As figuras são pintadas em tons de marrom, cinza e preto, com destaques de branco. A obra apresenta detalhes precisos e realistas da anatomia do corpo, bem como das ferramentas médicas utilizadas na dissecação. O corpo do criminoso apresenta uma ferida na cabeça e uma perna amputada, o que sugere que ele pode ter sido executado por um crime violento.
No canto inferior direito da pintura, há um livro aberto com o título “Spiegel der Konst” (“Espelho da Arte”), um tratado de anatomia escrito por Adriaan van de Spiegel e utilizada pelos médicos da época. Em geral, a “Aula de Anatomia do Dr. Nicolaes Tulp” é uma obra-prima devido à sua técnica precisa e detalhada, bem como à sua habilidade em transmitir um senso de realismo e drama. A pintura é considerada uma das obras mais importantes do período Barroco holandês e é frequentemente citada como um exemplo do estilo de pintura de Rembrandt.
A seguir estão algumas das características artísticas e estéticas da obra:
- Composição: A pintura apresenta uma composição equilibrada e organizada, com as figuras dos membros da guilda cirúrgica em torno da mesa de dissecação centralizada.
- Luz e Sombra: Rembrandt usa uma técnica conhecida como chiaroscuro, ou contraste entre luz e sombra, para dar profundidade e dimensão à cena. A luz focaliza no cadáver e no médico principal, destacando-os do fundo escuro.
- Realismo: A pintura é altamente realista, mostrando detalhes precisos das ferramentas cirúrgicas, do cadáver e das expressões dos personagens.
- Cores: O uso limitado de cores em tons de marrom e cinza dá à pintura uma atmosfera austera e solene.
- Simbolismo: A pintura inclui vários elementos simbólicos, como a presença de uma coruja, que representa sabedoria, e a posição da mão do cadáver, que simboliza a morte.
- Técnica: A pintura foi executada com uma técnica de pincelada solta e fluida, que enfatiza a textura e a superfície da pintura.
Em geral, a “Aula de Anatomia do Dr. Nicolaes Tulp” é considerada uma obra-prima devido à sua habilidade técnica e sua capacidade de transmitir um senso de realismo e drama. A pintura é considerada uma das obras mais importantes do período Barroco holandês e é frequentemente citada como um exemplo do estilo de pintura de Rembrandt.
Visão Crítica de Segurança (Colecistectomia)
A colecistectomia laparoscópica (CL) é o padrão-ouro para tratamento de cálculos biliares. No entanto, o risco de lesão do ducto biliar (BDI) continua a ser preocupação significativa, uma vez que CL ainda tem taxa de BDI maior do que a via laparotômica, apesar de muitos esforços propostos para aumentar sua segurança. A Visão Crítica da Segurança (CVS) proposta por Strasberg é a técnica para a identificação dos elementos críticos do triângulo de Calot durante a CL. Esta técnica foi adotada em vários programas de ensino e com a proposta de reduzir o risco de lesão acidental da via biliar (LAVB) e o uso da adequado da CVS está associado a menores taxas de LAVB. O objetivo deste #Webinar é abordar a Anatomia Cirúrgica Fundamental para a realização de uma Colecistectomia Laparoscópica.
Aderências Pós-Operatórias
Do Manejo Conservador à Decisão Cirúrgica
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 10 minutos)
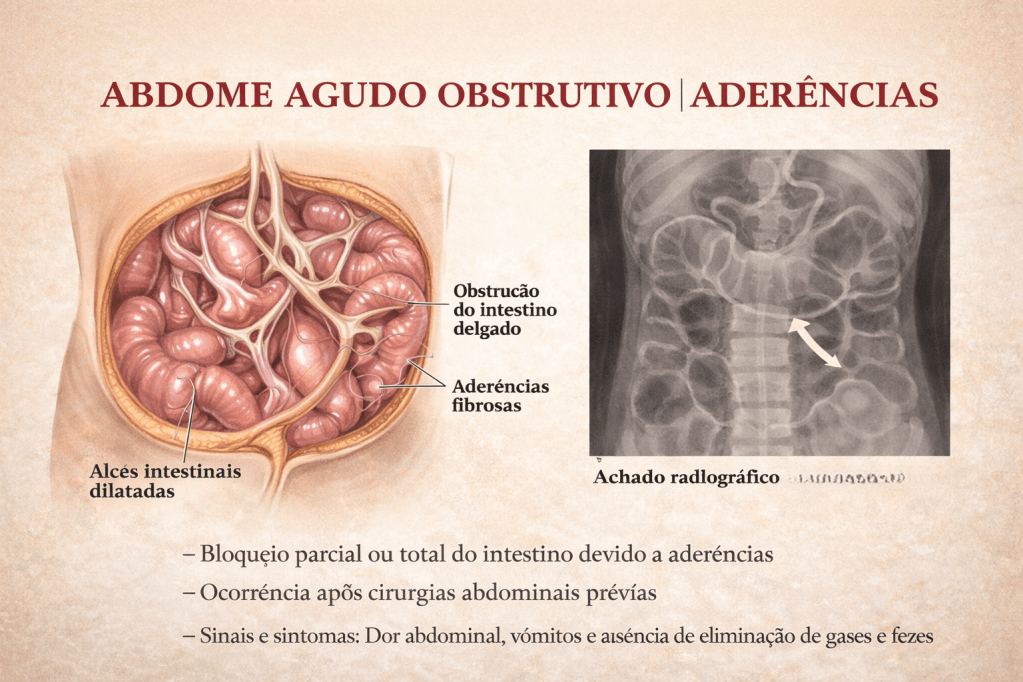
Introdução
A obstrução intestinal é um dos cenários mais desafiadores e frequentes no pronto-socorro cirúrgico. Historicamente, o abdome agudo obstrutivo impunha o dilema imediato da exploração cirúrgica. Hoje, compreendemos que a etiologia dita o compasso da intervenção. Entre todas as causas de obstrução do intestino delgado, as aderências pós-operatórias (bridas) assumem o protagonismo absoluto. Para o estudante de medicina, o residente e o cirurgião do aparelho digestivo, dominar o manejo da obstrução por bridas é essencial. O desafio não reside apenas na técnica operatória da enterólise, mas sim no raciocínio clínico aguçado para responder à pergunta fundamental: quando persistir no tratamento conservador e quando a indicação cirúrgica se torna imperativa?
Cenário Brasileiro
A formação de aderências peritoniais é uma resposta fisiológica quase universal ao trauma cirúrgico (isquemia, manipulação, coágulos), ocorrendo em até 90% dos pacientes submetidos a laparotomias. Contudo, em uma parcela significativa, essa cicatrização aberrante leva à obstrução mecânica. Na prática da cirurgia geral no Brasil, a obstrução por bridas responde por cerca de 60% a 75% das admissões por obstrução do intestino delgado. Dados do Sistema Único de Saúde (DataSUS) indicam que milhares de laparotomias exploradoras são realizadas anualmente no país devido a quadros obstrutivos agudos, gerando elevado custo financeiro e considerável morbimortalidade, além de reinternações frequentes.
Fisiopatologia e Diagnóstico
O peritônio, quando lesado, inicia uma cascata inflamatória rica em fibrina. Em condições normais, a fibrinólise degrada essa matriz em poucos dias. O desequilíbrio nesse sistema — com falha na fibrinólise peritonia — resulta na organização da fibrina em tecido conjuntivo vascularizado: a aderência.
A Tríade Diagnóstica
O diagnóstico é eminentemente clínico e radiológico:
- Clínica: Dor abdominal em cólica, distensão, vômitos (fecaloides em fases tardias) e parada de eliminação de flatus e fezes.
- Laboratório: Hemograma, eletrólitos, lactato e gasometria são cruciais para rastrear sinais de isquemia ou necrose (leucocitose importante, acidose metabólica).
- Imagem: A Tomografia Computadorizada (TC) de abdome com contraste venoso substituiu o raio-X simples como padrão-ouro. A TC identifica o ponto de transição (zona de calibres distintos), o grau de obstrução, a presença de sofrimento de alça (espessamento parietal, pneumatose, gás no sistema porta) e descarta outras etiologias (hérnias internas, neoplasias).
Estratégias de Tratamento
O manejo da obstrução por bridas sofreu uma evolução paradigmática, distanciando-se de intervenções intempestivas em favor de protocolos baseados em evidências.
1. Tratamento Conservador (Não Operatório)
Na ausência de sinais de isquemia intestinal, perfuração ou peritonite localizada, a conduta inicial deve ser conservadora:
- Jejum (NPO) e descompressão com Sonda Nasogástrica (SNG).
- Ressuscitação volêmica vigorosa e correção de distúrbios hidroeletrolíticos.
- Protocolo com Contraste Hidrossolúvel: A administração de contraste hiperosmolar (ex: Gastrografin) via SNG não possui apenas valor diagnóstico (avaliar se o contraste atinge o cólon em 24h), mas também efeito terapêutico. A hiperosmolaridade atrai líquido para a luz intestinal, reduzindo o edema da parede e estimulando o peristaltismo, resolvendo o quadro obstrutivo em uma parcela significativa dos casos.
2. Tratamento Cirúrgico: O Timing Ideal
A falha do tratamento conservador (geralmente avaliada após 48 a 72 horas) ou o surgimento de sinais de alarme (taquicardia, febre, irritação peritoneal, acidose) indicam cirurgia de urgência.
- Laparotomia vs. Laparoscopia: A via aberta continua sendo o padrão em pacientes com múltiplas cirurgias prévias ou grande distensão abdominal. A abordagem laparoscópica é excelente em mãos experientes, mas reserva-se a casos selecionados (ex: suspeita de brida única, distensão moderada), exigindo extrema cautela na introdução do primeiro trocarte (técnica aberta de Hasson) para evitar enterotomias iatrogênicas.
- O Ato Cirúrgico: A lise de aderências deve ser restrita ao necessário para resolver a obstrução. Múltiplas enterólises desnecessárias aumentam o risco de lesões e a formação de novas bridas. Em caso de necrose, a ressecção do segmento isquêmico com anastomose primária ou estomia (a depender da estabilidade hemodinâmica) é imperativa.
Pontos-Chave para a Prática Diária
- Suspeição de Isquemia: Dor refratária a analgésicos, taquicardia inexplicada e acidose metabólica são gritos de socorro de uma alça intestinal isquêmica. O tratamento conservador é contraindicado.
- O Valor da TC: A tomografia não apenas confirma o diagnóstico, mas é o farol que guia a decisão entre a enfermaria e o centro cirúrgico.
- Prevenção Primária: O uso de barreiras antiaderentes ainda carece de evidências universais robustas, mas a técnica cirúrgica apurada, manipulação tecidual delicada e controle rigoroso da hemostasia continuam sendo a melhor profilaxia.
Conclusões Aplicadas
O tratamento da obstrução intestinal por bridas é a quintessência do bom senso cirúrgico. O cirurgião moderno deve possuir a paciência de um clínico para conduzir o tratamento conservador respaldado pelo contraste hidrossolúvel e, simultaneamente, a assertividade de um intervencionista para indicar a sala de cirurgia ao primeiro sinal de estrangulamento.Compreender que “operar a radiografia” é um erro crasso e que a reavaliação clínica seriada (de preferência pelo mesmo examinador) é a bússola do tratamento, molda o profissional de excelência que minimiza ressecções intestinais desnecessárias e reduz a morbidade pós-operatória.
“Na obstrução intestinal aguda, não deixe o sol se pôr ou nascer sobre o paciente sem uma decisão. Mas lembre-se: a cirurgia sem indicação precipita o desastre que buscava evitar.” — Aforismo clássico derivado dos ensinamentos de Sir Zachary Cope, pioneiro no estudo e diagnóstico do abdome agudo.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Vascularização da Árvore Biliar
O Fio da Navalha na Prevenção da Isquemia e Estenose
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 11 minutos)
Introdução
No campo minado que é a cirurgia hepatobiliar, existe um princípio fisiológico que não admite margem para erro: enquanto o parênquima hepático é um órgão privilegiado, nutrido por um duplo suprimento sanguíneo (arterial e venoso portal), a árvore biliar é alimentada exclusivamente pelo sistema arterial. Para o estudante de medicina e o residente de cirurgia, a compreensão desta premissa muda drasticamente a forma como o bisturi e o cautério são manuseados em torno do hilo hepático. A esqueletização excessiva de um ducto biliar não é um sinal de dissecção meticulosa, mas sim a antessala anatómica de uma complicação catastrófica: a isquemia, seguida de necrose e estenose biliar. Neste artigo, dissecaremos a anatomia vascular da árvore biliar, as armadilhas do ducto cístico e os fundamentos anatómicos da cirurgia oncológica da vesícula.
1. A Vesícula Biliar: Topografia e Peculiaridades Histológicas
A vesícula biliar repousa no equador que divide o fígado direito do esquerdo — uma linha imaginária conhecida como Linha de Cantlie (ou linha de Rex-Cantlie), que cursa entre os segmentos IVb e V em direção à veia cava inferior posteriormente.
A vesícula é maioritariamente peritonizada, exceto na sua face posterior, que assenta diretamente na placa cística. No entanto, o seu verdadeiro “Calcanhar de Aquiles” reside na sua histologia: a vesícula biliar não possui muscularis mucosae, não possui submucosa e apresenta uma camada muscular descontínua.
- Implicação Cirúrgica Oncológica: Estas especificidades anatómicas removem as barreiras naturais contra a progressão tumoral, facilitando a invasão direta do cancro da vesícula biliar para o parênquima hepático. É por este motivo que o tratamento cirúrgico curativo exige uma Colecistectomia Radical (que inclui a ressecção em cunha dos segmentos hepáticos IVb e V) sempre que o estadiamento tumoral (T) for superior ou igual a T1b.
2. O Labirinto Anatómico do Ducto Cístico e da Via Biliar Principal
A partir do infundíbulo cónico da vesícula, o ducto cístico estende-se como o limite inferior do triângulo hepatocístico em direção ao hilo, unindo-se ao ducto hepático comum (DHC) para formar o ducto colédoco (VBP). Contudo, na via biliar, a variação anatómica é a regra, não a exceção. O ducto cístico pode correr paralelamente ao DHC, espiralar posteriormente a este e inserir-se na sua face medial. Mais perigoso ainda é quando o cístico se insere no Ducto Setorial Posterior Direito (RPD), uma variação que ocorre em cerca de 4% dos fígados. Esta configuração é notoriamente perigosa, expondo o RPD a um risco altíssimo de secção inadvertida durante uma colecistectomia de rotina. Distalmente, o colédoco entra na cabeça do pâncreas e une-se ao ducto pancreático (Wirsung) para formar a ampola hepatopancreática, controlada pelo Esfíncter de Oddi.
- O Canal Comum Longo: Quando a junção entre o colédoco e o ducto pancreático ocorre de forma anómala (antes do complexo esfincteriano), ocorre o refluxo de enzimas pancreáticas ativadas para a árvore biliar. Este trauma químico crónico é o principal fator de risco para a formação de cistoss do colédoco e para o desenvolvimento de Colangiocarcinoma.
3. O “Tendão de Aquiles”: A Vascularização Arterial da Via Biliar
Como mencionado, a árvore biliar depende de um fluxo arterial ininterrupto. O suprimento segue um padrão de perfusão que ascende e descende ao longo dos ductos:
- O Suprimento Distal (Ascendente): O ducto colédoco recebe a sua irrigação inferior a partir de arteríolas emparelhadas provenientes da Artéria Gastroduodenal (GDA) e da Artéria Pancreatoduodenal Superior Posterior (PSPDA). Esta última representa o suprimento arterial mais importante e constante para o colédoco distal.
- O Suprimento Proximal (Descendente): Proximamente, o colédoco é alimentado por arteríolas originadas da artéria hepática direita (AHD).
- As Artérias Marginais: Estes vasos superiores e inferiores anastomosam-se para formar as artérias marginais, que correm paralelamente ao longo do ducto colédoco, situando-se tipicamente nas posições das 3 e 9 horas (lateral e medialmente). Desnudar (esqueletizar) o colédoco deste suprimento arterial para criar uma anastomose ou durante uma linfadenectomia não regrada acarreta um risco altíssimo de isquemia e estenose cicatricial a longo prazo.
4. O Plexo Epicoledociano Hilar e as Variações Arteriais
No interior do hilo hepático, uma rica rede de capilares liga as artérias hepáticas direita e esquerda. Este leito vascular, denominado Plexo Epicoledociano Hilar, fornece uma circulação colateral crítica que pode manter o suprimento arterial para um lado do fígado caso o vaso ipsilateral seja lesado. A preservação deste plexo e do suprimento sanguíneo arterial para o fígado remanescente é absolutamente crucial na criação de uma anastomose biliodigestiva (hepaticojejunostomia). A isquemia hilar resulta na temível colangiopatia isquémica e no desenvolvimento de abcessos hepáticos intratáveis.
O Papel das Variações Arteriais no Colangiocarcinoma Hilar
Na cirurgia do colangiocarcinoma hilar (Tumor de Klatskin), a complexidade aumenta devido às variações arteriais. A artéria hepática direita cruza posteriormente ao ducto hepático na maioria dos casos, mas em 25% cruza anteriormente. Mais relevante ainda é a presença de uma Artéria Hepática Direita Substituída (ou Acessória), com origem na Artéria Mesentérica Superior (AMS). Ao contrário da anatomia clássica, este vaso cursa lateralmente ao ducto colédoco (e não medialmente), estando extremamente vulnerável à iatrogenia se o cirurgião não o identificar durante a dissecção do ligamento hepatoduodenal. Combinações destas variações com a localização exata do tumor ditarão se uma lesão hilar é ressecável ou irresecável.
Pontos-Chave para a Prática Diária
- A Regra das 3 e 9 Horas: Lembre-se sempre de que o suprimento axial do colédoco viaja nos seus flancos laterais. Evite dissecções circunferenciais extensas da via biliar principal.
- Histologia e Neoplasias: A ausência de submucosa na vesícula biliar dita a necessidade de cirurgia hepática radical (ressecção em cunha do leito) em tumores T1b ou superiores.
- Inserções Anómalas do Cístico: A inserção num ducto setorial direito (RPD) é uma armadilha clássica. A Visão Crítica de Segurança (CVS) e a colangiografia são as únicas formas de evitar a transecção de um ducto principal aberrante.
- O Perigo do Canal Comum: A junção biliopancreática anómala exige vigilância ou tratamento cirúrgico devido ao elevado risco de colangiocarcinoma derivado da inflamação enzimática crónica.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
O respeito pela árvore biliar transcende a mera identificação do tubo que transporta a bílis; exige uma veneração profunda pela sua microvascularização. O cirurgião que descasca a via biliar como se tratasse de um cabo elétrico condena o seu doente a um futuro de estenoses isquémicas, colangites de repetição e reintervenções de extrema complexidade. O domínio da variabilidade anatómica vascular (como as artérias substituídas da AMS) e o conhecimento tático do plexo epicoledociano não são meros detalhes de rodapé dos livros de anatomia; são a linha que separa o triunfo cirúrgico oncológico da catástrofe iatrogénica irreparável.
“A anatomia biliar não segue regras absolutas, apenas tendências. Operar no hilo hepático assumindo a normalidade é o primeiro passo para o desastre. O cirurgião deve dissecar com a expectativa constante da variação.” — Aforismo clássico da cirurgia hepatobiliar.
Gostou ❔Deixe-nos um comentário ✍️, partilhe nas suas redes sociais e|ou envie a sua dúvida pelo 💬 Chat On-line na nossa DM do Instagram.
Anatomia Cirúrgica Hepática
O Mapa Fundamental para Ressecções e Transplantes
Autor: Prof. Dr. Ozimo Gama
Categoria: Cirurgia Hepatobiliar / Anatomia Aplicada / Transplante Hepático Tempo de Leitura: 12 minutos
“Um bom conhecimento da anatomia do fígado é um pré-requisito para a cirurgia moderna do fígado.” — H. Bismuth
Introdução
O fígado, o maior órgão sólido do corpo humano (representando 2-3% do peso corporal), é uma estrutura de complexidade arquitetônica fascinante. Para o cirurgião geral, e imperativamente para o cirurgião hepatobiliar, o domínio da anatomia hepática transcende a memorização de nomes; trata-se de compreender as relações tridimensionais que ditam a segurança de uma hepatectomia e o sucesso de um transplante. Neste artigo, dissecaremos a anatomia hepática sob uma ótica cirúrgica, indo além da morfologia externa para explorar a segmentação funcional e as nuances vasculares vitais para a prática operatória de excelência.
1. Meios de Fixação e Mobilização Cirúrgica
O fígado é envolto pela cápsula de Glisson e peritônio, exceto na “área nua” diafragmática e no hilo. Seus ligamentos não são apenas estruturas de sustentação, mas marcos anatômicos cruciais para a mobilização segura do órgão:
-
Ligamentos Coronários e Triangulares: A mobilização destes permite a exposição da veia cava inferior (VCI) e das veias hepáticas.
-
Ligamento Venoso (Arantius): Remanescente do ducto venoso fetal. Sua dissecção é uma manobra chave. Ao isolá-lo, o cirurgião ganha acesso ao tronco das veias hepáticas esquerda e média, facilitando o controle vascular em hepatectomias esquerdas ou transplantes.
-
Ligamento Hepatocaval (Makuuchi): Uma estrutura fibrosa (por vezes contendo parênquima) que fixa o lobo caudado à veia cava. Sua divisão cuidadosa é obrigatória para expor a veia hepática direita e para a mobilização completa do lobo direito em transplantes intervivos.
2. A Revolução de Couinaud
A anatomia clássica, que dividia o fígado em lobos direito, esquerdo, quadrado e caudado baseada apenas em marcos externos (como o ligamento falciforme), é insuficiente para a cirurgia moderna. A verdadeira divisão funcional segue a Linha de Cantlie, um plano imaginário que vai do leito da vesícula biliar à veia cava inferior. Esta linha divide o fígado em metades funcionalmente independentes (Direita e Esquerda), cada uma com sua própria irrigação arterial, portal e drenagem biliar.
Adotamos a Segmentação de Couinaud (1954), que organiza o fígado em 8 segmentos baseados na distribuição das veias hepáticas e pedículos portais:
-
Fígado Direito (Setores Anterior e Posterior): Segmentos V, VIII (Anterior) e VI, VII (Posterior).
-
Fígado Esquerdo: Segmentos II, III (Lateral) e IV (Medial).
-
Lobo Caudado (Segmento I): Uma entidade autônoma. Localizado dorsalmente, recebe sangue de ambos os ramos portais (direito e esquerdo) e drena diretamente na VCI através de veias curtas. Esta drenagem direta confere ao caudado uma “proteção” relativa em casos de Síndrome de Budd-Chiari, onde ele frequentemente se hipertrofia.
3. O Hilo Hepático e a Tríade Portal
A dissecção do hilo exige precisão milimétrica, especialmente em transplantes com doador vivo (LDLT). As estruturas da tríade portal seguem uma organização anteroposterior constante que guia o cirurgião:
-
Ducto Biliar: Mais ventral (anterior) e lateral.
-
Artéria Hepática: Medial e na camada intermédia.
-
Veia Porta: A estrutura mais dorsal (posterior).
Variações Vasculares Importantes
-
Artéria Hepática: A anatomia “clássica” (artéria hepática comum saindo do tronco celíaco) está presente em apenas 60% dos casos. Variações críticas incluem a Artéria Hepática Direita Substituída (da Mesentérica Superior), que passa posterior à veia porta, e a Artéria Hepática Esquerda Substituída (da Gástrica Esquerda). O não reconhecimento pode levar à necrose do enxerto ou isquemia biliar.
-
Veia Porta: Variações na bifurcação, como a ausência do tronco principal da veia porta direita (trifurcação), exigem reconstruções complexas em transplantes.
4. Drenagem Venosa: O Escoamento
As três veias hepáticas principais (Direita, Média e Esquerda) correm nas fissuras intersegmentares:
-
Veia Hepática Direita (RHV): Drena o setor posterior. É a maior veia.
-
Veia Hepática Média (MHV): Corre na fissura principal (Linha de Cantlie). Fundamental para a drenagem dos segmentos V e VIII. Em transplantes de lobo direito, a gestão dos tributários da MHV é crítica para evitar congestão do enxerto.
-
Veias Acessórias: Cerca de metade da população possui veias hepáticas acessórias inferiores (drenando os segmentos VI e VII diretamente na cava). Se calibrosas (>5mm), devem ser reimplantadas para garantir a função do enxerto.
5. A Via Biliar e sua Vascularização: O “Tendão de Aquiles”
A anatomia biliar é a mais variável e propensa a complicações.
-
Irrigação Biliar: Diferente do parênquima, os ductos biliares extra-hepáticos são irrigados exclusivamente por um plexo arterial peribiliar (artérias das 3h e 9h), derivado principalmente da artéria hepática direita e retroduodenal.
-
Pérola Cirúrgica: Durante a captação do fígado, a dissecção excessiva do ducto biliar pode desvascularizá-lo, levando a estenoses isquêmicas tardias. Preservar a bainha peribiliar e o tecido hilar é mandatório.
6. A Vesícula Biliar e o Triângulo de Calot
Embora a colecistectomia seja um procedimento comum, ela exige respeito absoluto à anatomia. O Triângulo de Calot (delimitado pelo ducto cístico, ducto hepático comum e borda hepática) é a zona de segurança. A artéria cística deve ser identificada aqui. Variações, como um ducto cístico curto ou inserção no ducto direito, ou uma artéria hepática direita tortuosa (“Hump”) invadindo o triângulo, são armadilhas para o cirurgião desatento.
Conclusão
A cirurgia hepática evoluiu de ressecções em cunha não anatômicas para segmentectomias precisas e transplantes de doadores vivos. Essa evolução foi sustentada por um aprofundamento do conhecimento anatômico. Para o cirurgião em formação, o estudo exaustivo destas estruturas, suas variações e suas relações vasculares não é apenas acadêmico — é a base ética para oferecer segurança e cura aos pacientes portadores de doenças hepatobiliares.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags: #AnatomiaHepatica #CirurgiaDoFigado #TransplanteHepatico #Couinaud #CirurgiaHPB
Tratamento Cirúrgico da Hemorragia digestiva alta por varizes esofágicas | Hipertensão Porta
Introdução
A hipertensão portal é uma das principais complicações das doenças hepáticas crônicas e representa um dos maiores desafios da cirurgia do aparelho digestivo. Define-se classicamente como um aumento do gradiente de pressão portossistêmico acima de 5 mmHg, sendo clinicamente significativo quando ultrapassa 10–12 mmHg, nível a partir do qual surgem varizes gastroesofágicas e risco de hemorragia digestiva alta.
A cirrose hepática responde por cerca de 90% dos casos de hipertensão portal no mundo, sendo também a principal etiologia no Brasil. Estima-se que aproximadamente 50–60% dos pacientes cirróticos desenvolvem varizes esofágicas, e cerca de 30% destes apresentarão episódio de sangramento varicoso ao longo da vida.
Apesar dos avanços na terapia endoscópica e farmacológica, o tratamento cirúrgico da hipertensão portal permanece uma ferramenta essencial em casos selecionados, particularmente quando ocorre falha terapêutica ou quando há indicações específicas relacionadas à etiologia e à função hepática do paciente.
Neste artigo de educação médica continuada revisaremos os principais aspectos do tratamento cirúrgico da hipertensão portal, com foco em indicações, resultados comparativos entre técnicas e implicações na prática atual da cirurgia digestiva.
ARTIGO DE REVISÃO – HIPERTENSÃO PORTAL
Fisiopatologia da Hipertensão Portal
A hipertensão portal resulta do aumento da resistência ao fluxo portal associado ou não ao aumento do fluxo sanguíneo esplâncnico. Os mecanismos principais incluem:
- Aumento da resistência intra-hepática
- fibrose e distorção arquitetural na cirrose
- compressão sinusoidal
- disfunção endotelial hepática
- Aumento do fluxo portal
- vasodilatação esplâncnica mediada por óxido nítrico
- Formação de circulação colateral portossistêmica
- desenvolvimento de varizes esofagogástricas
- shunts espontâneos
As principais manifestações clínicas incluem:
- hemorragia digestiva alta por varizes
- ascite
- encefalopatia hepática
- hiperesplenismo
O tratamento cirúrgico visa reduzir a pressão portal ou interromper o fluxo varicoso, prevenindo novos episódios hemorrágicos.
Indicações do Tratamento Cirúrgico
Com o advento da ligadura elástica endoscópica, da terapia farmacológica vasoativa e do TIPS, as indicações cirúrgicas tornaram-se mais restritas. Atualmente, as principais indicações incluem:
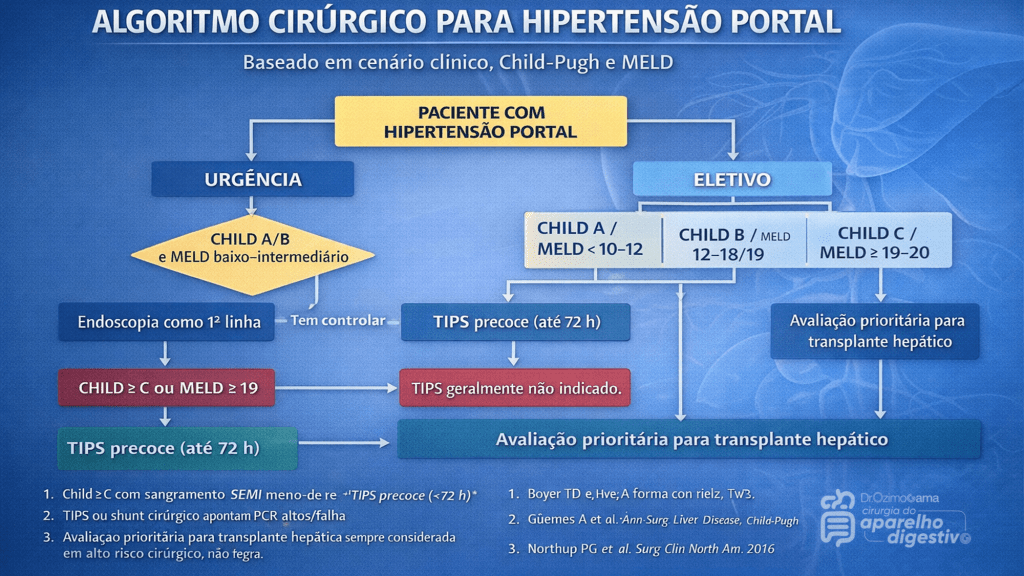
A indicação cirúrgica atual exige a aplicação rigorosa de escores prognósticos, notadamente o Child-Pugh e o MELD. Pacientes Child-Pugh A (MELD < 10 a 15) possuem baixo risco cirúrgico, sendo candidatos ideais para cirurgias eletivas, incluindo shunts e desvascularização. Por outro lado, pacientes descompensados (Child-Pugh C ou MELD > 19-20) apresentam alto risco de mortalidade pós-operatória, inclusive pós-TIPS, sendo o transplante hepático a via mandatória. O grande desafio recai sobre os pacientes limítrofes (Child-Pugh B ou MELD 15-19). Neste estrato de risco intermediário, shunts cirúrgicos tendem a oferecer maior sobrevida a longo prazo para aqueles com função hepática estável, enquanto o TIPS demonstra maior benefício na sobrevida de pacientes com ascite refratária ou sangramento agudo.
AULA: TRATAMENTO CIRÚRGICO DA HIPERTENSÃO PORTAL
Na prática contemporânea da cirurgia hepatobiliar, o manejo da hipertensão portal é multidisciplinar, envolvendo:
- hepatologistas
- endoscopistas
- radiologistas intervencionistas
- cirurgiões digestivos
O algoritmo terapêutico atual pode ser resumido da seguinte forma:
- Primeira linha
- terapia farmacológica
- ligadura elástica endoscópica
- Falha terapêutica
- TIPS
- Pacientes selecionados
- shunt cirúrgico
- desvascularização
- Doença hepática avançada
- transplante hepático
O cirurgião digestivo continua desempenhando papel fundamental, sobretudo em centros terciários e unidades de referência hepatobiliar.

Pontos-chave para o Cirurgião Digestivo
- A hipertensão portal clinicamente significativa ocorre com gradiente >10–12 mmHg
- O sangramento varicoso continua sendo a complicação mais grave
- TIPS é hoje a principal estratégia de resgate após falha endoscópica
- Shunts cirúrgicos permanecem relevantes em pacientes selecionados
- A desvascularização gastroesofágica ainda possui papel importante na esquistossomose
- Transplante hepático é o único tratamento curativo da hipertensão portal associada à cirrose
Conclusão
Embora os avanços na radiologia intervencionista e na endoscopia tenham modificado profundamente o manejo da hipertensão portal, o tratamento cirúrgico permanece indispensável em situações específicas. A seleção adequada do paciente, baseada em função hepática, etiologia da hipertensão portal e recursos disponíveis, continua sendo o fator mais importante para bons resultados. Para o cirurgião digestivo moderno, compreender as diferentes estratégias — desde shunts portossistêmicos até o transplante hepático — é essencial para oferecer um tratamento individualizado e seguro.
PROF. DR. OZIMO GAMA
Gastroenterologia Cirúrgica
“O transplante de fígado e as complexas derivações portais nos ensinaram que não há limites absolutos na cirurgia, apenas fronteiras do conhecimento que aguardam para ser ultrapassadas com dedicação e ciência.” — Thomas Starzl
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
GOSSIPIBOMA
O Inimigo Oculto no Bloco Operatório e o Desafio Médico-Legal na Cirurgia Digestiva
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 11 minutos)
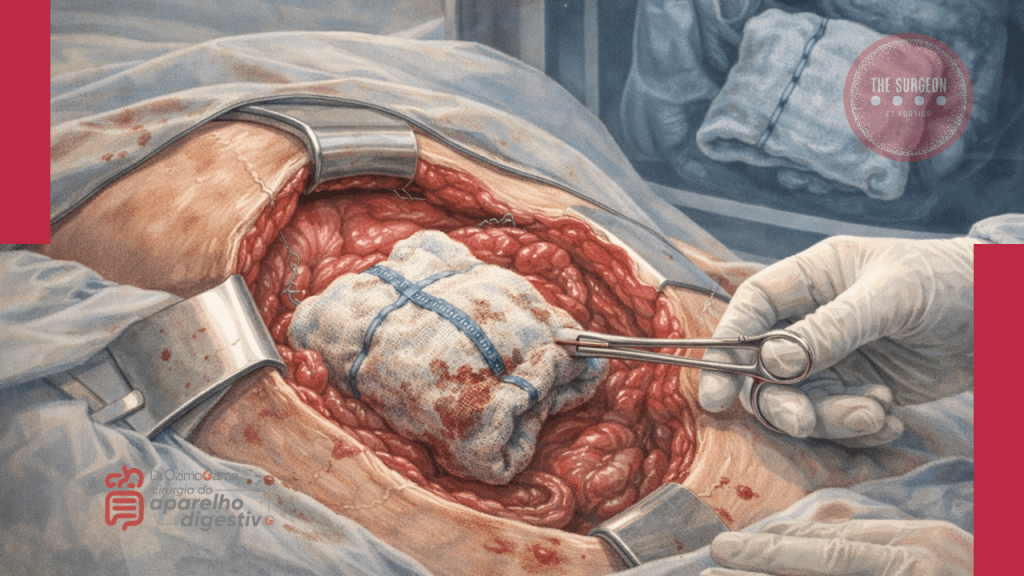
Introdução
No vasto e complexo universo da cirurgia do aparelho digestivo, poucos eventos adversos geram tanta perplexidade clínica e devastação médico-legal quanto o “gossipiboma”. O termo deriva do latim Gossypium (algodão) e do swahili boma (esconderijo), designando uma matriz de matéria têxtil envolvida por uma reação de corpo estranho. Também apelidado de “textiloma”, o seu primeiro caso foi descrito por Wilson em 1884. Embora gazes e compressas sejam as ferramentas mais básicas de qualquer laparotomia, o seu esquecimento no interior da cavidade abdominal transforma um material de hemostase num tumor iatrogénico. A incidência real dos gossipibomas é subnotificada — primariamente devido ao estigma e às pesadas implicações legais da sua deteção —, mas representa uma falha catastrófica nos protocolos de segurança do bloco operatório. Para o cirurgião e para toda a equipa, compreender a fisiopatologia, os fatores de risco e, sobretudo, os métodos de prevenção desta entidade é um dever ético inegociável.
Epidemiologia e Fatores de Risco
Estima-se que a retenção de material têxtil ocorra numa frequência de 1 a cada 1.000 a 1.500 operações intra-abdominais. A cavidade abdominal e pélvica é, de longe, o “esconderijo” mais comum devido à sua vasta anatomia e aos recessos profundos.
O gossipiboma não é um mero fruto do acaso; ele prospera no caos. A literatura científica identifica fatores predisponentes cruciais:
- Cirurgia de Emergência: A incidência é nove vezes maior nestes cenários.
- Mudança de Tática Intraoperatória: Alterações não planeadas no decorrer da intervenção elevam o risco em quatro vezes.
- Fatores do Doente e do Ambiente: Doentes com obesidade mórbida, perdas hemáticas maciças que exigem tamponamento rápido, tempo operatório prolongado e, criticamente, a troca de turnos do pessoal médico e de enfermagem (instrumentistas e circulantes) durante o ato cirúrgico.
Fisiopatologia e Evolução Clínica
O relógio biológico do gossipiboma é imprevisível. O tempo entre a operação primária e as manifestações clínicas pode variar de meros 10 dias a várias décadas. A patologia manifesta-se essencialmente através de duas reações orgânicas distintas:
- Resposta Assética Fibrinosa (Crónica): O material têxtil, se permanecer estéril, induz a produção de fibrina, originando aderências e o encapsulamento do corpo estranho (granuloma). O doente pode permanecer completamente assintomático durante anos, ou apresentar queixas inespecíficas e uma massa abdominal palpável que mimetiza uma neoplasia.
- Resposta Exsudativa (Aguda): Ocorre uma infeção secundária severa, culminando na formação de abcessos e fístulas. O material retido tenta encontrar uma via de exteriorização, podendo fistulizar para órgãos internos (estômago, intestino, cólon, bexiga) ou formar uma fístula externa na parede abdominal. Nestes casos, o doente apresenta um quadro florido: dor abdominal, náuseas, vómitos, febre, sépsis, hemorragia digestiva crómica ou síndrome de má absorção.
Diagnóstico, Tratamento e Prognóstico
A ausência de sintomas precoces ou a sua inespecificidade tornam o diagnóstico um autêntico desafio. O cirurgião deve manter um elevado índice de suspeição perante qualquer massa abdominal num doente com história de laparotomia prévia.
- O Padrão-Ouro Diagnóstico: A Tomografia Computorizada (TC) de abdómen é o exame de eleição. A imagem clássica revela uma lesão cística de aspeto “espongiforme” (padrão em miolo de pão), uma cápsula hiperdensa em camadas concêntricas e, ocasionalmente, calcificações murais. A presença de gás no interior da lesão sem evidência de perfuração intestinal é altamente sugestiva.
- Tratamento: A remoção cirúrgica (seja por via laparoscópica em casos altamente selecionados ou laparotomia) é o único tratamento curativo.
- Prognóstico: A excisão atempada é vital para evitar complicações que elevam a taxa de mortalidade para valores inaceitáveis de 11% a 35%. Se a retenção for crónica, a severidade das aderências pode exigir ressecções intestinais extensas e complexas.
Implicações Médico-Legais e Procedimentos Preventivos
O gossipiboma é indiscutivelmente uma falha grave na prestação de cuidados de saúde (malpractice). Do ponto de vista médico-legal, a responsabilidade é frequentemente partilhada entre o cirurgião principal — o “capitão do navio” — e a equipa de enfermagem responsável pela contagem.
A abordagem definitiva é, e sempre será, a Prevenção. A adoção de protocolos rígidos no bloco operatório salva vidas e carreiras:
- Contagem Meticulosa Universal: São mandatárias quatro contagens rigorosas do material cirúrgico: na montagem da mesa, imediatamente antes da incisão, no início do encerramento da aponevrose e durante a síntese da pele.
- Material Radiopaco: O uso exclusivo de compressas e gazes equipadas com filamentos radiopacos é obrigatório.
- Exploração Ativa: Autores como Dhillon e Park reforçam a necessidade primária da exploração manual e visual dos quatro quadrantes abdominais pelo cirurgião no final do procedimento, independentemente de uma contagem de compressas declarada “correta”.
- Conduta Perante Falha na Contagem: Se a contagem final for divergente, a síntese da cavidade não deve ser concluída até que o material seja localizado (a menos que haja instabilidade hemodinâmica crítica). A realização de uma radiografia intraoperatória imediata é mandatária.
Conclusões Aplicadas
O gossipiboma não é uma complicação inerente e aceitável do ato cirúrgico; é uma falha de sistema e de liderança. O aumento aparente da sua incidência exige que os métodos, a comunicação e a disciplina no interior do bloco operatório sejam revistos e aperfeiçoados. Para os jovens cirurgiões e residentes, a mensagem é clara: a cirurgia de excelência não termina na anastomose perfeita, mas sim na verificação obsessiva e no respeito incondicional pelos protocolos de segurança. A verdadeira destreza cirúrgica repousa na humildade de nunca presumir que a cavidade está vazia sem antes a inspecionar exaustivamente.
“A confiança é um sentimento nobre, mas no bloco operatório, a dupla verificação é a única garantia de segurança. Um erro de omissão pode ensombrar o mais brilhante dos procedimentos cirúrgicos.” — Aforismo da Segurança do Doente Cirúrgico.
Gostou ❔Deixe-nos um comentário ✍️ , partilhe nas suas redes sociais e|ou envie a sua dúvida pelo 💬 Chat On-line na nossa DM do Instagram.
10 Princípios da interação PACIENTE – CIRURGIÃO
Comunicação, Ética e Segurança na Prática Cirúrgica
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 11 minutos)
Introdução
Quando a perspectiva de uma intervenção cirúrgica se impõe — seja para a ressecção de uma neoplasia gástrica, a correção de uma hérnia complexa ou o tratamento metabólico da obesidade —, o medo, a apreensão e a sensação de perda de controle são reações viscerais e universais do ser humano. A visão da dor, o fantasma das complicações e a entrega do próprio corpo ao bisturi de outrem geram uma ansiedade que a mais avançada tecnologia robótica não é capaz de aplacar. No Brasil, onde realizamos milhões de procedimentos cirúrgicos anualmente pelo Sistema Único de Saúde (SUS) e pela Saúde Suplementar, estatísticas dos Conselhos Regionais de Medicina (CRMs) revelam um dado alarmante: mais de 70% das denúncias e processos ético-profissionais por suposto “erro médico” não nascem de falhas técnicas grosseiras, mas da quebra, deterioração ou inexistência de uma relação médico-paciente sólida e transparente. Para o estudante de medicina e o residente de cirurgia, compreender que a destreza manual deve ser precedida pela empatia relacional é o primeiro passo para a maestria.
Os 10 Princípios da Prática Cirúrgica Ética
Para enfrentar os desafios do perioperatório de forma eficaz e blindar a relação terapêutica contra ruídos e frustrações, estruturamos os 10 princípios fundamentais que regem a interação entre o cirurgião e o paciente:
1. Construção da Confiança Mútua
A cirurgia não é um ato comercial; é um pacto de confiança. O cirurgião deve dedicar tempo qualitativo na consulta, evitando o modelo impessoal e apressado (“medicina de linha de montagem”). Um relacionamento humanizado evita que insucessos terapêuticos se transformem em acusações injustas.
2. Clareza e Transparência na Informação
O consentimento deve ser genuinamente esclarecido, não apenas assinado. É imperativo banir o jargão técnico excessivo. Traduzir a fisiopatologia e o plano cirúrgico para uma linguagem acessível reduz o medo do desconhecido e prepara o paciente e seus familiares para o desdobramento natural do pós-operatório.
3. Alinhamento de Expectativas Realistas
Muitas frustrações cirúrgicas nascem do hiato entre a expectativa do paciente e a realidade biológica. É vital discutir os limites da medicina. Prometer “cura absoluta” ou “risco zero” é uma falácia ética.
4. Avaliação Abrangente de Riscos
O Risco Cirúrgico transcende a avaliação cardiológica (Escore de Goldman ou Lee). A avaliação pré-operatória moderna exige uma visão holística: o estado nutricional, a fragilidade (especialmente em idosos), a sarcopenia e, crucialmente, a saúde mental do paciente devem ser exaustivamente investigados.
5. O Papel Estratégico do Anestesiologista
O ato cirúrgico é indissociável do ato anestésico. A escolha da técnica anestésica (bloqueios, anestesia geral, monitorização multimodal) é uma decisão compartilhada. O cirurgião deve fomentar o encontro pré-operatório entre o paciente e a equipe de anestesiologia para dirimir receios e garantir as melhores práticas.
6. Preparação para Mudanças de Rota (O Imprevisto)
O paciente deve entrar no centro cirúrgico ciente de que a tática operatória pode ser alterada. O consentimento para uma laparoscopia deve invariavelmente incluir a possibilidade de conversão para via aberta. Surpresas intraoperatórias (como invasões tumorais insuspeitas) alteram o prognóstico, o tempo de internação e as necessidades de reabilitação.
7. Documentação Exaustiva e Irretocável
O prontuário médico é a testemunha ocular do cuidado. Detalhes das consultas preliminares, opções terapêuticas recusadas pelo paciente e as orientações fornecidas devem estar meticulosamente registrados. Como já abordamos em nosso artigo sobre o método S.O.A.P., documentação é proteção mútua.
8. Descrição Cirúrgica e Rastreabilidade
A descrição do ato operatório deve ser um relato literário da técnica executada. Além disso, a gestão de peças cirúrgicas (envio para exame anatomopatológico) exige rigor logístico. A falha na identificação ou a perda de uma biópsia é uma tragédia diagnóstica inaceitável.
9. Pós-Operatório: Presença e Cuidado Contínuo
O ato cirúrgico não termina no fechamento da pele. O acompanhamento pós-operatório (na UTI, na enfermaria e no ambulatório) exige a presença física e atenciosa do cirurgião principal. Delegar todo o pós-operatório a terceiros é uma das maiores fontes de ressentimento por parte dos pacientes.
10. Atenção ao Estado Emocional
A instabilidade emocional predispõe a uma resposta inflamatória exacerbada e a uma percepção amplificada da dor. Pacientes com ansiedade severa ou depressão pré-existente exigem suporte psicológico ou psiquiátrico adjuvante para garantir resiliência durante a convalescença.
Aplicação na Cirurgia Digestiva
Na cirurgia do aparelho digestivo, estes princípios encontram aplicação diária e visceral:
- Na Cirurgia Bariátrica: O alinhamento de expectativas (Princípio 3) é o alicerce do sucesso. O paciente deve compreender que o bisturi altera a anatomia (Restrição/Incretinas), mas não opera a mente. O reganho de peso é uma possibilidade real se não houver adesão multidisciplinar (Princípio 10).
- Na Cirurgia Oncológica: Informar um paciente sobre a possível necessidade de um estoma (colostomia ou ileostomia) definitivo ou temporário (Princípio 6) exige tato excepcional (Princípio 2). Esconder essa possibilidade para “evitar o sofrimento prévio” destrói a confiança se o paciente acordar com uma bolsa coletora no abdome.
- Na Cirurgia Biliar e Pancreática: Complicações temidas, como a fístula biliar ou pancreática, devem ser discutidas com transparência empática. Quando a complicação ocorre, a presença diária e incansável do cirurgião à beira do leito (Princípio 9) é o que diferencia o abandono do amparo.
Pontos-Chave para a Prática Diária
- Comunicação é Procedimento: Trate a conversa com o paciente e a família com o mesmo rigor técnico que você trata a dissecção de um hilo hepático.
- A Verdade Suportável: Nunca minta, mas adeque a entrega da informação à capacidade de absorção do paciente naquele momento.
- Consentimento Individualizado: Termos de consentimento (TCLE) padronizados e genéricos não possuem força legal. O TCLE deve espelhar as peculiaridades anatômicas e biológicas do paciente específico.
Conclusões Aplicadas
A ética na cirurgia moderna vai imensuravelmente além da destreza técnica, dos nós bem atados e da ausência de complicações infecciosas. Trata-se do respeito à autonomia daquele que se submete à lâmina. A prática cirúrgica de excelência exige que sejamos peritos em fisiologia e mestres em humanidade. O cirurgião do aparelho digestivo que domina estes 10 princípios navega pelas tempestades de uma fístula anastomótica não como um réu diante de um juiz (o paciente), mas como um comandante ao lado de seu companheiro de naufrágio, trabalhando juntos para alcançar a margem segura da cura.
“O bom cirurgião opera com a mão; o cirurgião brilhante opera com o cérebro; mas o cirurgião extraordinário opera com o coração. O bisturi corta tecidos, mas é a compaixão que cicatriza as feridas da alma.” — Adaptado dos princípios humanitários de Sir William Osler, pai da medicina moderna.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Como funciona o GRAMPEADOR INTESTINAL ?
A Busca pela Segurança e Eficiência na Cirurgia Moderna
Introdução O objetivo primordial de qualquer cirurgião, ao iniciar uma intervenção, é garantir que o procedimento seja seguro e eficiente. A “regra de ouro” da cirurgia moderna permanece clara: o ato operatório deve ser o mais breve possível, gerando o menor trauma tecidual e restaurando a função do órgão. O resultado esperado é sempre a minimização das intercorrências no pós-operatório. Embora a cirurgia atual atinja esses objetivos de forma bastante satisfatória, as complicações relacionadas às suturas e à cicatrização ainda são desafios presentes na rotina hospitalar.
A Evolução Histórica e os Desafios da Cicatrização A confiabilidade das suturas gastrointestinais, por exemplo, é uma conquista relativamente recente. Foi apenas no final do século XIX que a compreensão dos princípios básicos da cicatrização tecidual permitiu avanços significativos nesta área. Sabemos hoje que o sucesso do reparo tecidual não depende apenas da técnica empregada, mas é uma equação complexa que envolve o paciente e a área operada. Diversos fatores podem retardar ou prejudicar drasticamente a cicatrização, entre eles:
-
Isquemia (falta de suprimento sanguíneo);
-
Edema (inchaço excessivo);
-
Infecção local ou sistêmica;
-
Desnutrição do paciente.
O Fator Humano e o Surgimento da Tecnologia Existe uma variável crítica na cirurgia: a habilidade manual. Naturalmente, há uma variação na destreza e na técnica entre diferentes cirurgiões. Foi justamente essa disparidade que motivou o desenvolvimento de novos dispositivos cirúrgicos. O objetivo da inovação tecnológica na cirurgia é superar as diferenças individuais, funcionando como um equalizador. Ao utilizar dispositivos que padronizam etapas críticas (como as suturas mecânicas), permite-se que técnicas complexas sejam executadas adequadamente, independente de quem opera.
Conclusão Para que a medicina avance, uma técnica não pode depender apenas do talento de poucos. Ela deve ser reproduzível de forma confiável pelo maior número possível de cirurgiões. Somente através dessa padronização e do auxílio tecnológico é que os resultados cirúrgicos podem ser amplamente adotados, reconhecidos como eficazes e, acima de tudo, seguros para o paciente.
Prontuário Médico
Evolução Cirúrgica S.O.A.P.
A Engenharia do Prontuário Médico, Ética, LGPD e Defesa Profissional
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 12 minutos)

Introdução
O prontuário médico transcende a simples formalidade administrativa; ele é o repositório sagrado do segredo médico, o espelho da qualidade assistencial e a testemunha silenciosa de cada decisão clínica tomada na beira do leito. No ambiente de alta complexidade da cirurgia do aparelho digestivo, onde o limiar entre a recuperação fisiológica e a complicação catastrófica é estreito, a evolução médica diária exige uma precisão quase matemática. A prática de preencher o prontuário é uma obrigação legal e uma responsabilidade intransferível do médico assistente. Em hospitais de ensino — o berço da formação cirúrgica —, acadêmicos de medicina e médicos residentes (especializandos) realizam as anotações sob a estrita supervisão, correção e responsabilidade solidária de seus preceptores ou médicos do staff. É uma prática antiética, ilegal e frontalmente condenável delegar o preenchimento da evolução clínica a qualquer profissional que não seja um médico habilitado perante o Conselho Regional de Medicina (CRM) ou um acadêmico em treinamento devidamente supervisionado. Historicamente e na atualidade, o prontuário médico corretamente preenchido tem sido a principal, e muitas vezes a única, peça de defesa do cirurgião em casos de denúncias por suposto mau atendimento, imperícia, imprudência ou negligência. Quando a polícia, o Poder Judiciário ou as Câmaras Técnicas do CRM são acionados, o prontuário é o primeiro documento requisitado. Se a sua técnica cirúrgica no bloco operatório for irretocável, mas a sua evolução na enfermaria for omissa, perante a lei, o cuidado não existiu.
Aspectos Históricos e a Gênese do Modelo S.O.A.P.
Até meados do século XX, os prontuários médicos eram estruturados de forma cronológica e narrativa, assemelhando-se a um diário confuso, onde informações vitais perdiam-se num mar de textos desorganizados. A revolução ocorreu na década de 1960, quando o Dr. Lawrence L. Weed publicou o artigo seminal “Medical records that guide and teach” (N Engl J Med; 1968). Weed propôs uma inversão de paradigma: o Problem-Oriented Medical Record (Prontuário Médico Orientado por Problemas). No Brasil, este modelo foi amplamente adotado e adaptado sob a sigla POPE (Prontuário Orientado por Problemas e Evidências), destacando a necessidade de fundamentar cada passo clínico em evidências científicas sólidas. A espinha dorsal deste modelo é a nota de evolução estruturada no formato S.O.A.P., que divide o raciocínio médico em quatro quadrantes fundamentais: Subjetivo, Objetivo, Avaliação e Plano. Esta sistematização traz objetividade, clareza, facilidade de auditoria e, principalmente, permite que qualquer membro da equipe multidisciplinar (enfermagem, fisioterapia, nutrição) compreenda imediatamente o estado clínico e as metas terapêuticas do paciente cirúrgico.
A Estrutura do S.O.A.P. Cirúrgico
Na rotina da enfermaria de cirurgia digestiva, a evolução deve seguir um rigor técnico absoluto. O cabeçalho deve, obrigatoriamente, conter a identificação completa do paciente (Nome, Idade, Registro Hospitalar), a Enfermaria/Leito, o Diagnóstico Principal, o Nome da Cirurgia Realizada, o Dia de Pós-Operatório (ex: PO2 de Gastrectomia Total) e o Horário exato do atendimento.
Abaixo, detalhamos como cada componente da sigla S.O.A.P. deve ser preenchido sob a ótica cirúrgica:
1. “S” – Dados Subjetivos (A Voz do Paciente)
Compreende as queixas do paciente, sua percepção sobre a evolução e informações fornecidas por acompanhantes. Em cirurgia, não basta escrever “passou bem”. É imperativo interrogar ativamente sobre:
- Dor: Utilizar escalas validadas (ex: Escala Visual Analógica – EVA de 0 a 10). A dor é em cólica? É contínua? Piora à mobilização?
- Trato Gastrointestinal: Houve náuseas ou episódios de êmese? Houve eliminação de flatos (sinal crucial de retorno do trânsito intestinal)? Houve evacuação? Como foi a aceitação da dieta oferecida?
- Mobilização: O paciente deambulou? Conseguiu sentar na poltrona? (Dados vitais para a profilaxia de trombose venosa profunda e atelectasia).
- Exemplo: “Paciente refere dor incisional leve (EVA 2/10), com boa aceitação de dieta líquida. Nega náuseas. Refere eliminação de flatos durante a madrugada. Deambulou no corredor hoje cedo.”
2. “O” – Dados Objetivos (A Visão do Cirurgião)
Inclui os dados vitais irrefutáveis, o exame físico focado e os resultados de exames complementares laboratoriais ou de imagem. Este é o terreno da evidência mensurável.
- Sinais Vitais: Frequência Cardíaca (FC), Pressão Arterial (PA), Frequência Respiratória (FR), Temperatura (T) e Saturação de O2. A taquicardia inexplicada no pós-operatório de uma anastomose intestinal é o primeiro grito de socorro de uma fístula, antes mesmo da febre ou da dor peritonítica.
- Exame Físico Específico: * Abdome: Globoso? Flácido? Ruídos hidroaéreos presentes? Dor à palpação (diferenciar dor incisional de irritação peritoneal)?
- Ferida Operatória (FO): Limpa e seca? Hiperemiada? Presença de secreção (serosa, purulenta, hemática)?
- Drenos: Tipo de dreno (ex: Jackson-Pratt, Blake, Penrose). Qual o aspecto do débito (seroso, sero-hemático, bilioso, entérico, fecaloide)? Qual o volume em 24 horas?
- Estomas: Colostomia/Ileostomia com mucosa rósea (vitalidade)? Edemaciada? Isquêmica? Estoma funcionante (presença de fezes na bolsa)?
- Exemplo: “PA: 120×70 mmHg; FC: 88 bpm; FR: 16 irpm; T: 36,8ºC. Abdome: flácido, RHA+, indolor à palpação profunda. FO: sem hiperemia, curativo limpo. Dreno de Blake em FIE: débito de 30ml sero-hemático em 24h. Labs (05/10): Hb 11.2, Leucócitos 8.500 (sem desvio), PCR 12 (em queda).”
3. “A” – Avaliação (O Raciocínio Clínico)
A Avaliação é a síntese. É o momento em que o cirurgião processa os dados Subjetivos e Objetivos para emitir o seu juízo de valor sobre o estado do paciente. Não é a repetição dos diagnósticos da internação, mas a avaliação do momento atual.
- O paciente está evoluindo conforme o esperado para o dia de pós-operatório?
- Há suspeita de complicações (íleo paralítico prolongado, infecção de sítio cirúrgico, fístula anastomótica, sangramento, pneumonia)?
- Exemplo: “Paciente no 2º PO de Colectomia Direita Videolaparoscópica por Adenocarcinoma. Evolução clínica e laboratorial amplamente favorável. Trânsito intestinal restabelecido. Sem sinais de complicações infecciosas ou hemorrágicas no momento.”
4. “P” – Plano (A Conduta e o Futuro)
O Plano define as ações imediatas e de médio prazo. É a conduta terapêutica e diagnóstica fundamentada na avaliação recém-feita.
- Terapêutica: Progressão ou regressão de dieta? Transição de analgesia venosa para via oral? Suspensão de fluidos intravenosos? Descalonamento ou suspensão de antibioticoterapia profilática/terapêutica?
- Procedimentos: Retirada de dreno? Troca de curativo? Retirada de Sonda Vesical de Demora (SVD)?
- Diagnóstico: Solicitação de novos exames laboratoriais ou tomografia de abdome (se suspeita de complicação)?
- Educação/Alta: Orientações ao paciente e preparo para alta hospitalar.
- Exemplo: “1. Progredir para dieta pastosa; 2. Suspender hidratação venosa e manter acesso salinizado; 3. Trocar analgesia para via oral; 4. Retirar dreno de Blake hoje; 5. Programar alta hospitalar para amanhã, caso mantenha tolerância à dieta.”
Aspectos Éticos, Legais e Atualizações Normativas
A prática médica contemporânea exige que a evolução cirúrgica esteja blindada contra vulnerabilidades legais. A doutrina da “medicina de defesa” tem dado lugar à Prevenção Jurídica Ativa, onde o prontuário é o escudo. Segundo o Código de Ética Médica (Resolução CFM nº 2.217/2018), em seu Capítulo X, é vedado ao médico negar acesso ao prontuário ao paciente, bem como é infração ética grave deixar de elaborar prontuário legível para cada paciente.
O Código Penal e a Falsidade Ideológica
As anotações devem refletir a estrita verdade temporal e clínica. O Artigo 299 do Código Penal Brasileiro é taxativo quanto ao crime de falsidade ideológica: “Omitir, em documento público ou particular, declaração que dele devia constar, ou nele inserir ou fazer inserir declaração falsa ou diversa da que devia ser escrita…”. A pena varia de 1 a 5 anos de reclusão. Evoluções “clonadas” (o infame “copiar e colar” do dia anterior no prontuário eletrônico sem verificar o paciente) que não relatam a mudança do estado clínico (ex: o paciente apresentou febre à noite, mas a evolução matinal diz “afebril” por cópia da véspera) podem caracterizar este crime, além de negligência médica. No papel, rasuras anulam o valor probatório; deve-se usar a expressão “digo” ou “em tempo” para retificações.
O Prontuário Eletrônico do Paciente (PEP) e a Certificação Digital
A Resolução CFM nº 1.638/2002 tornou obrigatória a legibilidade do prontuário em papel (o fim definitivo da “letra de médico” ilegível). Contudo, a grande revolução normativa reside no Prontuário Eletrônico. De acordo com a Resolução CFM nº 1.821/2007 (e suas atualizações, como a Resolução 2.299/2021), para que um documento médico eletrônico tenha validade legal e elimine a necessidade do papel, ele deve utilizar sistema de segurança com Nível de Garantia de Segurança 2 (NGS2), que exige a Assinatura Digital com certificado ICP-Brasil (Infraestrutura de Chaves Públicas Brasileira). Sem o token ou certificado digital em nuvem assinado pelo médico, a evolução digitada não tem presunção de veracidade jurídica plena. A senha do sistema do hospital não substitui a assinatura digital. A prática de fornecer seu login e token para que o residente ou interno assine por você é falta ética gravíssima, equiparada à quebra de sigilo e falsidade ideológica.
A Lei Geral de Proteção de Dados (LGPD – Lei 13.709/2018)
O prontuário cirúrgico contém dados sensíveis (informações sobre saúde). A implementação da LGPD obriga as instituições e os médicos a garantirem o acesso restrito a essas informações. A evolução clínica SOAP não pode ser fotografada pelo celular do médico e enviada em grupos de mensagens (como WhatsApp) sem a desidentificação completa do paciente ou consentimento expresso. Vazamentos de dados contidos no prontuário geram pesadas multas pela Autoridade Nacional de Proteção de Dados (ANPD) e processos civis por dano moral.
Pontos-Chave para a Prática Diária do Residente
- Tempo é Documento: A data e a hora do atendimento são cruciais. A evolução médica reflete o paciente naquele minuto exato. A cronologia dos eventos salva ou condena o cirurgião em uma sindicância.
- O Perigo do Copiar/Colar: No prontuário eletrônico, o recurso de copiar a evolução do dia anterior induz ao erro, perpetuando dados vitais antigos ou ignorando exames recentes. Cada dia exige uma avaliação autêntica e original.
- Assinatura e Carimbo: No papel, carimbo e assinatura legível com CRM. No eletrônico, Assinatura Digital (ICP-Brasil). A validação de quem prescreve ou evolui é intransferível.
- Comunicação Multidisciplinar: A evolução SOAP não é escrita apenas para o juiz ou para o CRM; ela é lida pelo enfermeiro que administrará o antibiótico, pelo fisioterapeuta que mobilizará o paciente e pelo nutrólogo que ajustará a dieta. Clareza é respeito pela equipe e segurança para o doente.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
A evolução cirúrgica é a radiografia do intelecto do médico. O método S.O.A.P. obriga o cirurgião do aparelho digestivo a estruturar seu pensamento científico de maneira cartesiana, garantindo que nenhum dreno, ostomia ou sintoma de alarme passe despercebido na enfermaria. Em uma era dominada pela alta tecnologia robótica e laparoscópica no centro cirúrgico, é na beira do leito e na frente da tela do Prontuário Eletrônico que o pós-operatório é vencido. Compreender as legislações vigentes, a obrigatoriedade da certificação digital e a rigidez da LGPD protege o patrimônio e a carreira do profissional, permitindo que ele exerça a arte da cirurgia com paz de espírito, sabendo que sua conduta está não apenas eticamente correta, mas juridicamente blindada.
“O prontuário não é apenas um registro de doenças, mas sim o livro de memórias de uma batalha travada em conjunto pelo médico e pelo paciente. Uma palavra mal escrita ou omitida pode ser tão letal quanto um bisturi mal empunhado na sala de operações.” — Aforismo da Educação Médica Cirúrgica.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
O RELATO CIRÚRGICO
A Arte e a Ciência da Documentação no Bloco Operatório
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 10 minutos)

Introdução
Na prática da cirurgia do aparelho digestivo, existe um aforismo não escrito, mas implacável: a cirurgia não termina quando o último ponto é dado na pele, mas sim quando o relato cirúrgico é assinado. O relato (ou descrição) cirúrgico é o documento médico-legal mais importante do perioperatório. Ele é o testemunho definitivo e detalhado de tudo o que ocorreu dentro das portas cerradas do centro cirúrgico. Infelizmente, é comum observarmos descrições feitas de forma apressada, “oficiosa” ou sumariíssima. O uso de frases genéricas como “cirurgia realizada pela técnica habitual” deve ser criticado com veemência e banido da nossa prática. Tais descrições padronizadas omitidas não apenas empobrecem a ciência cirúrgica, perdendo valiosos detalhes para consultas e pesquisas, mas também representam um verdadeiro suicídio jurídico em caso de litígio. O ato cirúrgico exige uma dissertação minuciosa e fiel à realidade biológica e técnica enfrentada.
A Anatomia de um Relato Perfeito
A elaboração da descrição cirúrgica não deve ser um fardo burocrático, mas um exercício de reflexão. Pela sua importância, este relatório pode e deve ser redigido em um momento de calma, propício à clareza mental e ao zelo pela legibilidade. Para garantir a eficácia documental, científica e legal, o relato cirúrgico deve obrigatoriamente conter a seguinte estrutura:
1. Cabeçalho e Identificação Exaustiva
- Identificação do Paciente: Nome completo, idade, número de prontuário (registro hospitalar) e leito.
- Equipe Cirúrgica: Nome do cirurgião principal, 1º e 2º auxiliares, instrumentador(a) e equipe de anestesiologia. A omissão de membros da equipe é uma falha ética grave.
- Procedimento e Diagnóstico: Nome técnico claro e completo da cirurgia proposta e da cirurgia efetivamente realizada. Registro da condição patológica que motivou a intervenção, bem como afecções concomitantes encontradas.
- Cronometria: Hora exata do início da incisão e hora do término da operação (fechamento cutâneo).
2. O Cenário e o Acesso
O relato deve descrever como o paciente foi preparado:
- Posição e Preparo: Posição do paciente na mesa (ex: decúbito dorsal, posição de Lloyd-Davies), uso de coxins de proteção (vital para evitar alegações de lesões de nervos periféricos), e os produtos utilizados para a antissepsia da pele.
- Via de Acesso: Descrição detalhada da incisão (ex: mediana supraumbilical, incisão de Mercedes) ou do posicionamento exato dos trocartes na cirurgia laparoscópica/robótica.
3. A Dissertação Técnica (O Ato em Si)
É aqui que a “técnica habitual” deve dar lugar à precisão milimétrica:
- Achados e Aspecto da Afecção: Descrever o grau de inflamação, fibrose, disseminação tumoral, presença de ascite ou aderências. O que os seus olhos viram ao abrir a cavidade?
- Tática e Técnica Operatória: Descrever o passo a passo. Como os ligamentos foram seccionados? Onde a artéria foi ligada? Houve uso de eletrocautério (monopolar/bipolar) ou energia ultrassônica?
- Fios e Suturas: Especificar os tipos de fios (ex: Polidioxanona 3-0, Polipropileno 1), o tipo de sutura (contínua, separada, invaginante) e o uso de grampeadores mecânicos (marca e cor da carga).
Aplicação na Cirurgia Digestiva: Prevenção e Rastreabilidade
No contexto das operações do aparelho digestivo, frequentemente lidamos com ressecções de órgãos, anastomoses e potencial de contaminação.
- Exames Transoperatórios: Relatar a realização de Colangiografia Intraoperatória (descrevendo seus achados: “ausência de falhas de enchimento, passagem livre de contraste para o duodeno”) ou de ultrassonografia intraoperatória.
- Gestão de Peças e Biópsias: Deve constar explicitamente o envio de peças cirúrgicas, linfonodos ou secreções colhidas para exame histopatológico e/ou cultura.
- Controle de Gaze e Instrumental: É mandatório registrar que a equipe de enfermagem (circulante/instrumentador) realizou e confirmou a contagem dupla de todas as compressas, gazes e instrumentais antes do fechamento da cavidade. Isso isenta a equipe nos tristes casos de corpos estranhos retidos (gossipiboma).
- Intercorrências e Acidentes: Qualquer lesão inadvertida (ex: lesão esplênica ao tracionar o estômago), sangramentos acima do esperado ou instabilidade hemodinâmica devem ser relatados com transparência, bem como as medidas táticas adotadas para a sua resolução.
Pontos-Chave para a Prática Diária
- Fuja do “Control C + Control V”: O relato padrão pré-descrito é injustificável em qualquer caso. Cada ser humano possui uma anatomia única; cada cirurgia é um evento singular.
- Medicina Legal e Traumas: Em lesões por arma branca ou de fogo, o relato deve descrever rigorosamente os trajetos internos. Projéteis ou objetos extraídos devem ser descritos, rotulados e entregues à autoridade policial/instituto médico-legal com protocolo de recebimento assinado.
- Desenhos Esquemáticos: Sempre que possível ou quando o sistema do prontuário permitir, a inclusão de esquemas anatómicos desenhados pelo cirurgião eleva imensamente o valor elucidativo do documento.
Conclusões Aplicadas
A descrição cirúrgica bem executada é um pilar da credibilidade profissional do cirurgião. É ela que justifica a complexidade do ato perante o faturamento hospitalar e os planos de saúde. É ela que orienta o oncologista sobre o estadiamento patológico. E, acima de tudo, é ela o escudo protetor da equipe em caso de demandas judiciais ou sindicâncias ético-profissionais. Criticar as descrições sumárias e incentivar a literatura cirúrgica detalhada nos prontuários é um dever de todos os preceptores de residência médica. Um relato rico e minucioso reflete não apenas o rigor técnico, mas o respeito sagrado do cirurgião pela história daquele paciente.
“Ex nihilo nihil fit.” (Do nada, nada surge). — Princípio filosófico. Na cirurgia moderna, aquilo que não foi detalhadamente escrito, juridicamente e cientificamente, nunca aconteceu.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Prevenção e Rastreamento do Câncer Colorretal
O Papel Proativo do Cirurgião na Interrupção da Sequência Adenoma-Carcinoma
Autor: Prof. Dr. Ozimo Gama (Tempo de Leitura: 9 minutos)
Introdução
O Câncer Colorretal (CCR) representa um dos maiores paradoxos da oncologia moderna: é uma das neoplasias mais letais e prevalentes no mundo, e, simultaneamente, uma das mais preveníveis. Para o cirurgião do aparelho digestivo, compreender a biologia tumoral e os protocolos de rastreamento (screening) é tão fundamental quanto dominar a técnica de uma retossigmoidectomia com excisão total do mesorreto (TME). A prevenção do CCR não se restringe a orientações dietéticas; ela é um ato intervencionista. Ao compreender e atuar na fisiopatologia da doença, o médico em formação — seja o estudante de medicina ou o residente de cirurgia — assume o protagonismo na redução da morbimortalidade associada a esta patologia.
O Cenário Brasileiro
A relevância do CCR no Brasil exige atenção redobrada. Segundo as estimativas do Instituto Nacional de Câncer (INCA) para o triênio 2023-2025, são esperados cerca de 45.630 novos casos anuais no país. Atualmente, o CCR ocupa a segunda posição entre os cânceres mais incidentes tanto em homens quanto em mulheres (excluindo os tumores de pele não melanoma). As regiões Sul e Sudeste concentram as maiores taxas, refletindo a íntima relação da doença com a urbanização, sedentarismo e ocidentalização da dieta (alto consumo de carne vermelha processada e baixo teor de fibras).
A Janela de Oportunidade Biológica
A pedra angular da prevenção do CCR é a teoria genética da sequência adenoma-carcinoma, descrita classicamente por Vogelstein. Sabemos que mais de 90% dos carcinomas colorretais esporádicos surgem de lesões benignas precursoras (pólipos adenomatosos ou lesões serrilhadas). Esse processo de acúmulo de mutações genéticas (como APC, KRAS, TP53) é lento. Estima-se que a transição de um adenoma inicial para um adenocarcinoma invasivo leve de 10 a 15 anos. Esta progressão insidiosa cria uma “janela de oportunidade” excepcional para a intervenção médica: a detecção e ressecção das lesões precursoras antes que a malignidade se instale.
Fatores de Risco e Prevenção Primária
A prevenção primária foca em evitar o surgimento dos pólipos. Envolve a mitigação de fatores de risco modificáveis:
- Dietéticos: Redução do consumo de carnes processadas e vermelhas; aumento da ingestão de fibras, cálcio e vitamina D.
- Estilo de vida: Combate ao tabagismo, ao etilismo excessivo e à obesidade (o tecido adiposo visceral é um órgão endócrino ativo que promove um estado pró-inflamatório crônico).
Aplicação na Cirurgia Digestiva: O Rastreamento (Prevenção Secundária)
Para o cirurgião endoscopista, a colonoscopia é a arma definitiva. Diferente de outros métodos de rastreio (como a mamografia ou o PSA, que são puramente diagnósticos), a colonoscopia é diagnóstica e terapêutica.
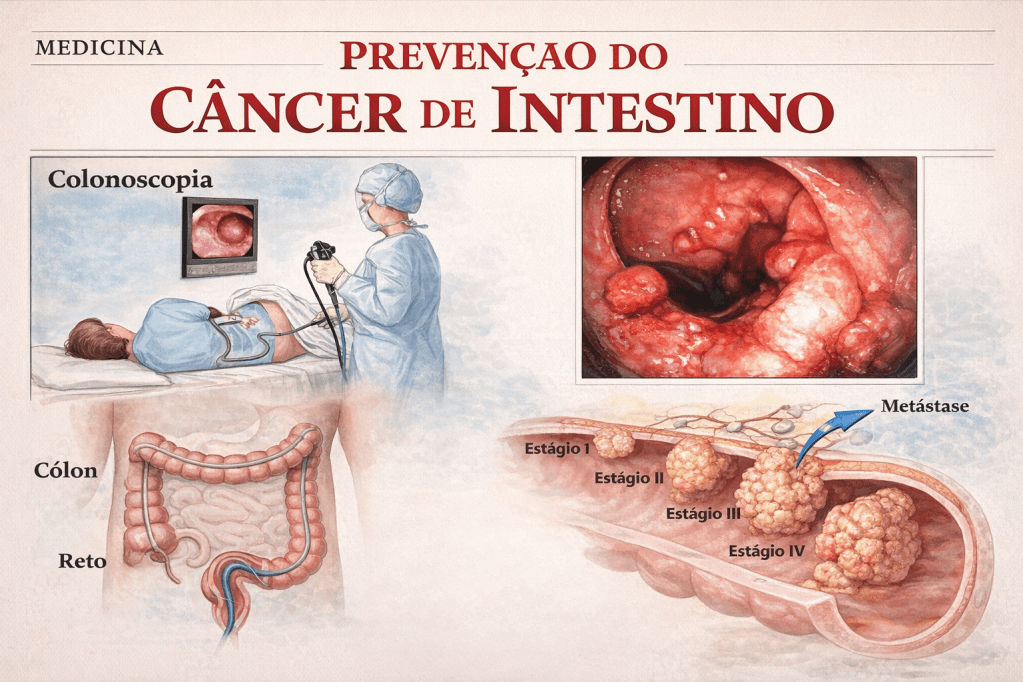
Protocolos de Rastreamento (Screening)
As diretrizes globais sofreram mudanças recentes devido ao aumento alarmante da incidência de CCR em adultos jovens (abaixo dos 50 anos).
- Risco Habitual (População Geral): A Sociedade Americana de Câncer (ACS) e a Força-Tarefa de Serviços Preventivos dos EUA (USPSTF) passaram a recomendar o início do rastreamento aos 45 anos (e não mais aos 50). No Brasil, sociedades médicas (como o CBCD e a SOBED) já endossam essa antecipação. O rastreio pode ser feito através de Colonoscopia (a cada 10 anos) ou Pesquisa de Sangue Oculto nas Fezes (FIT) anualmente, reservando a colonoscopia para os casos positivos.
- Risco Aumentado (Histórico Familiar): Pacientes com parente de 1º grau com CCR ou adenoma avançado devem iniciar o rastreio aos 40 anos, ou 10 anos antes da idade de diagnóstico do familiar mais jovem (o que ocorrer primeiro).
- Alto Risco (Síndromes Hereditárias e DII):
- PAF (Polipose Adenomatosa Familiar): Rastreio inicia aos 10-12 anos de idade com retossigmoidoscopia. A colectomia profilática é a regra.
- Síndrome de Lynch (HNPCC): Colonoscopia anual ou bienal a partir dos 20-25 anos.
- Doenças Inflamatórias Intestinais (Retocolite Ulcerativa e Crohn): Rastreio intensivo com biópsias seriadas após 8 anos de doença ativa devido ao risco de displasia secundária à inflamação crônica.
Pontos-Chave para a Prática Diária
- Idade de Início: Atualize-se sobre a mudança paradigmática do início do rastreamento para os 45 anos na população de risco habitual.
- Polipectomia é Prevenção: A remoção endoscópica de um adenoma tubular (polipectomia, mucosectomia ou ESD) não é apenas um procedimento diagnóstico; é um ato cirúrgico profilático que salva vidas.
- História Clínica: A anamnese detalhada sobre o histórico oncológico familiar é o teste genético mais barato e eficaz à disposição do médico. Nunca negligencie a construção do heredograma.
Conclusões Aplicadas
A cirurgia oncológica colorretal atingiu patamares de excelência técnica com a laparoscopia e a cirurgia robótica. No entanto, o triunfo definitivo do cirurgião do aparelho digestivo não reside na ressecção de grandes massas tumorais, mas sim na sua prevenção. A atuação ativa do especialista na conscientização dos pacientes, na solicitação rigorosa de exames de rastreio nos prazos adequados e na execução meticulosa de colonoscopias profiláticas é o que verdadeiramente altera a curva epidemiológica desta doença devastadora no Brasil e no mundo.
“As nações ocidentais estão cavando suas próprias sepulturas com os próprios dentes. (…) Se você tem um chão inundado por uma torneira aberta, de nada adianta passar um esfregão sem antes fechar a torneira.” — Denis Parsons Burkitt, renomado cirurgião e pesquisador, sobre a importância da dieta e da prevenção nas doenças do trato gastrointestinal.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.