Biópsia do Adenocarcinoma de Pâncreas
Com a crescente adoção da quimioterapia neoadjuvante como estratégia pré-operatória, a confirmação histológica tornou-se obrigatória antes do início do tratamento sistêmico. Este artigo compara os principais métodos de biópsia — EUS-FNB, EUS-FNA, biópsia percutânea guiada por TC e biópsia líquida — em termos de acurácia diagnóstica, taxa de complicações, risco de semeadura tumoral e capacidade de fornecer material para análise molecular.
Boa Leitura !
Avanços da Oncologia Clínica nos Tumores do Aparelho Digestivo
Resumo
Os últimos dez anos representaram uma ruptura no tratamento sistêmico dos tumores gastrointestinais. O estabelecimento da quimioterapia tripla perioperatória (FLOT), o papel da imunoterapia adjuvante pós-ressecção trimodal no esôfago (CheckMate-577), a total neoadjuvância no reto (RAPIDO, PRODIGE 23), a introdução do mFOLFIRINOX adjuvante no pâncreas (PRODIGE 24), e o bloqueio de PD-L1 nas vias biliares (TOPAZ-1, KEYNOTE-966) transformaram fundamentalmente o cenário perioperatório. Esta revisão organiza esses marcos por topografia e tipo histológico, com destaque para os estudos que modificaram diretriz.
Boa Leitura !
Manejo Clínico-Cirúrgico das Fístulas Digestivas Pós-Operatórias
Uma Abordagem Estratégica Baseada em Evidências
Autor: Prof. Dr. Ozimo Gama
Categoria: Cirurgia Geral / Emergências Cirúrgicas / Terapia Intensiva / Cirurgia Digestiva
Tempo de Leitura: 15 minutos
Introdução
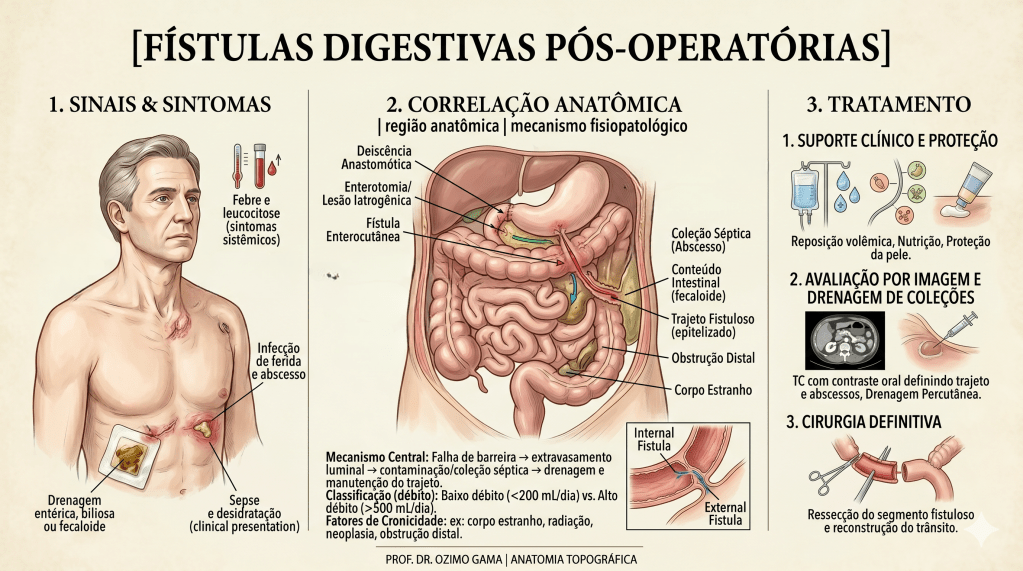
As fístulas digestivas pós-operatórias representam uma das complicações mais temidas e desafiadoras no teatro de operações da cirurgia do aparelho digestivo. Definidas como comunicações anormais entre o lúmen intestinal e o meio externo (fístulas enterocutâneas) ou outros órgãos, elas sinalizam a falência de uma anastomose ou sutura. Historicamente, essa condição era acompanhada por taxas de mortalidade proibitivas. O paradigma do tratamento mudou radicalmente após o trabalho clássico de Chapman et al. (1964), que demonstrou que a desnutrição era o principal determinante de óbito nestes pacientes, e não apenas a falha técnica em si. Antes dessa viragem, a indicação cirúrgica precoce para “fechar o buraco” resultava frequentemente em desastres, devido ao precário estado geral e à inflamação tecidual intensa. Este artigo propõe uma sistematização tática do manejo das fístulas, integrando o suporte metabólico à precisão diagnóstica e à decisão cirúrgica parcimoniosa.
Classificação e Fases do Manejo
A fístula não é um evento isolado, mas um processo dinâmico que exige do cirurgião uma “consciência situacional” aguçada. A classificação baseia-se no débito (volume em 24h): as de Alto Débito (> 500 ml/dia) são as mais críticas, pois provocam distúrbios hidroeletrolíticos e desnutrição acelerada.
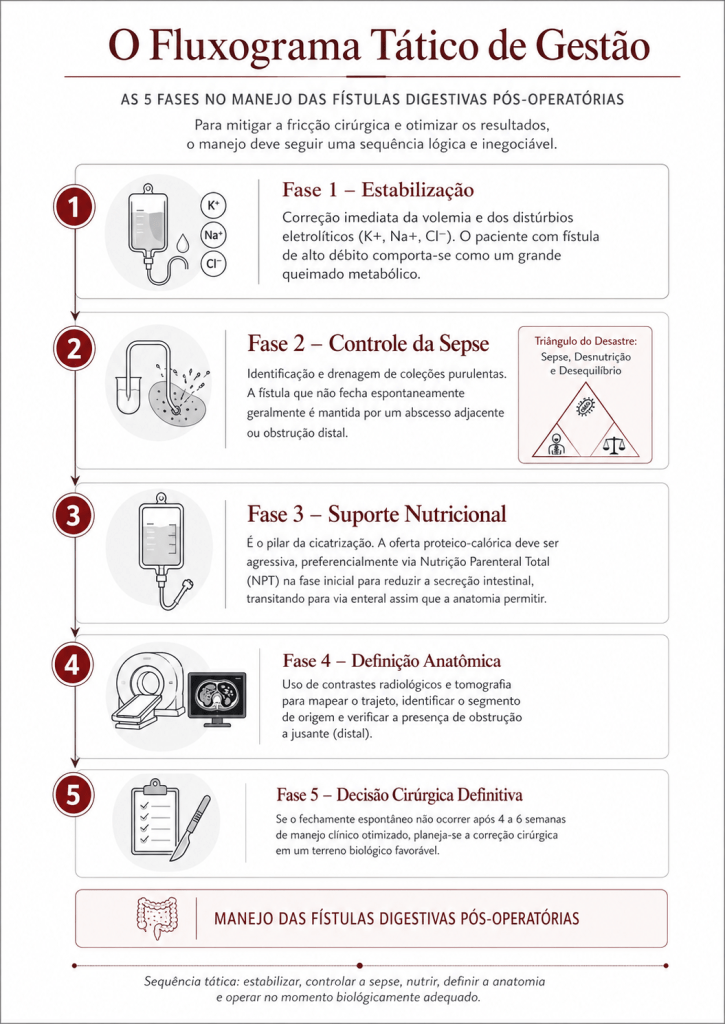
O Fluxograma Tático de Gestão (As 5 Fases)
Para mitigar a fricção cirúrgica e otimizar os resultados, o manejo deve seguir uma sequência lógica e inegociável:
- Fase 1 – Estabilização: Correção imediata da volemia e dos distúrbios eletrolíticos (K+, Na+, Cl-). O paciente com fístula de alto débito comporta-se como um grande queimado metabólico.
- Fase 2 – Controle da Sepse: Identificação e drenagem de coleções purulentas. A fístula que não fecha espontaneamente geralmente é mantida por um abcesso adjacente ou obstrução distal (O Triângulo de Desastre: Sepse, Desnutrição e Desequilíbrio).
- Fase 3 – Suporte Nutricional: É o pilar da cicatrização. A oferta proteico-calórica deve ser agressiva, preferencialmente via Nutrição Parenteral Total (NPT) na fase inicial para reduzir a secreção intestinal, transitando para via enteral assim que a anatomia permitir.
- Fase 4 – Definição Anatômica: Uso de contrastes radiológicos e tomografia para mapear o trajeto, identificar o segmento de origem e verificar a presença de obstrução a jusante (distal).
- Fase 5 – Decisão Cirúrgica Definitiva: Se o fechamento espontâneo não ocorrer após 4 a 6 semanas de manejo clínico otimizado, planeia-se a correção cirúrgica em um “terreno” biológico favorável.
Avaliação Diária dos Dispositivos e da Fístula: Sinais de Alerta
A vigilância diária na enfermaria é a nossa inteligência de campo. O cirurgião deve avaliar os dispositivos com rigor metodológico:
- Efluente da Fístula: Avaliar volume, cor e odor. O aparecimento de bile ou conteúdo gástrico num dreno antes purulento indica uma nova comunicação.
- Proteção da Pele: O suco entérico e pancreático é extremamente cáustico. O uso de bolsas coletoras e pastas de barreira (estomaterapia) é essencial para evitar a evisceração por digestão da parede abdominal.
- Sinais de Alerta (Red Flags):
- Mudança súbita no volume: Parada abrupta de drenagem associada a dor e febre sugere obstrução do trajeto e formação de abcesso.
- Hemorragia “Sentinela”: Sangue vivo no trajeto da fístula pode indicar erosão de vasos mesentéricos pelas enzimas, prenunciando uma hemorragia maciça.
Aplicação na Cirurgia Digestiva: Contexto Brasileiro
No Brasil, autores renomados como Campos, Rasslan e Safatle estabeleceram que o tratamento operatório das fístulas deve ser uma manobra de exceção planejada. Dados brasileiros reforçam que a mortalidade, embora reduzida para patamares de 10% a 20% em centros de excelência, ainda é elevada quando há atraso no suporte nutricional ou controle inadequado da infecção. Em procedimentos como a duodenopancreatectomia (Whipple), a fístula pancreática exige uma tática específica de desvio e proteção vascular, muitas vezes utilizando a somatostatina ou seus análogos para reduzir o débito exócrino e permitir a granulação do leito.
Pontos-Chave
- Paciência Estratégica: Não opere precocemente uma fístula em fase inflamatória (fase de “fricção” máxima). Aguarde a estabilização metabólica.
- Nutrição é Cicatrização: Sem proteínas, não há fechamento. O manejo nutricional é a “munição” do paciente.
- Controle de Sepsis: A fístula não é a vilã; a coleção não drenada é que mata o paciente.
- Anatomia é Destino: Identifique obstruções distais. Uma fístula nunca fechará se houver um obstáculo à frente.
Conclusões Aplicadas à Prática
O manejo das fístulas digestivas pós-operatórias é a prova máxima da resiliência e competência de uma equipe de cirurgia digestiva. Ele exige a fusão entre o conhecimento anatómico profundo e uma disciplina tática inabalável na condução do suporte clínico. O cirurgião que compreende que “operar menos” na fase aguda é, por vezes, a manobra mais heróica, protege a vida do doente. A missão é transformar uma catástrofe pós-operatória numa jornada de reabilitação, onde o bisturi é reservado para o momento da reconstrução definitiva, num organismo capaz de sustentar a cura. Como afirma a literatura clássica, nas fístulas, o cirurgião deve ter a mão de ferro no suporte clínico e a mão de veludo na indicação operatória.
“A fístula digestiva testa a paciência do cirurgião, a resiliência do paciente e a qualidade de todo o sistema de suporte hospitalar.” — Sérgio Rasslan, mestre da cirurgia de urgência e trauma brasileira.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#FistulaDigestiva #CirurgiaDigestiva #ManejoCirurgico #SegurancaDoPaciente #EducacaoMedica
Dieta no Pós-Operatório de Cirurgia Digestiva
Guia Estratégico e Alimentos Proibidos para a Recuperação Tática
Autor: Prof. Dr. Ozimo Gama
Categoria: Cuidados Perioperatórios / Nutrição Clínica / Cirurgia do Aparelho Digestivo
Tempo de Leitura: 14 minutos
Introdução
O sucesso de uma intervenção cirúrgica no aparelho digestivo não se encerra na última sutura ou no grampeamento da anastomose. A fase subsequente, o pós-operatório, exige uma “logística de suprimentos” impecável: a dieta. Historicamente, a conduta cirúrgica era pautada pelo dogma do repouso intestinal absoluto — o infame “nada por via oral” até o retorno dos ruídos hidroaéreos ou a eliminação de flatos. Contudo, a ciência cirúrgica moderna, impulsionada por protocolos como o ERAS (Enhanced Recovery After Surgery) e o brasileiro Projeto ACERTO, promoveu uma quebra de paradigma. Sabemos hoje que a realimentação precoce é uma “manobra tática” essencial para reduzir a resposta endócrino-metabólica ao trauma (REMIT), preservar a barreira mucosa intestinal e acelerar a alta hospitalar. Para o residente e o estudante de medicina, orientar a dieta é prescrever o combustível para a cicatrização e a retomada da “superioridade tática” do organismo do paciente.
Desenvolvimento: A Progressão Fisiológica e o Ciclo de Tolerância
A reintrodução alimentar deve ser vista como uma missão por fases, onde cada etapa é validada pela tolerância do paciente (aplicando o ciclo OODA: Observar a aceitação, Orientar a progressão, Decidir a consistência e Agir na prescrição).
- Fase de Líquidos Claros (Hidratação Tática): Inicia-se nas primeiras 6 a 24 horas. O foco é o teste de motilidade. Inclui água, chais e caldos coados.
- Fase de Líquidos Completos (Aporte Proteico): Introdução de suplementos hiperproteicos para combater a sarcopenia.
- Dieta Pastosa/Branda (Transição de Fluxo): Purês e cozidos de fácil mastigação. É o “reconhecimento do terreno”.
- Dieta Regular (Retorno à Base): Retomada da alimentação sólida, focada em proteínas de alto valor biológico.
Alimentos Proibidos: O que evitar para proteger o “Terreno” em cicatrização
Na estratégia de recuperação, existem “fatores hostis” que podem sabotar a cicatrização das anastomoses ou provocar distensão abdominal, comprometendo a integridade tática da cirurgia. Entender a relação entre a Semente (o procedimento) e o Terreno (o organismo do paciente) é fundamental para o sucesso. Abaixo, listamos os alimentos que devem ser estritamente evitados ou suspensos conforme a fase:
1. Bebidas Gaseificadas (Refrigerantes e Água com Gás)
O dióxido de carbono provoca distensão súbita do lúmen gástrico e intestinal. Em cirurgias com anastomoses recentes, o aumento da pressão intraluminal atua como um estresse mecânico indesejado, podendo agravar o desconforto e retardar o retorno do peristaltismo.
2. Alimentos de Alta Fermentação (FODMAPs e Leguminosas)
Feijão, repolho, brócolis, couve-flor e cebola crua são indutores de gases. A fermentação excessiva no pós-operatório imediato causa cólicas e distensão, dificultando a deambulação e a mecânica respiratória do paciente.
3. Frituras e Gorduras Saturadas
Alimentos gordurosos exigem uma carga biliar e pancreática elevada para a digestão. Em colecistectomias, onde o fluxo biliar é contínuo e sem reservatório, a gordura pode provocar diarreia osmótica e dispepsia severa. Além disso, retardam o esvaziamento gástrico, aumentando o risco de náuseas.
4. Carboidratos Simples e Doces Concentrados
Especialmente críticos em pacientes gastrectomizados. Açúcares refinados, mel e doces de massa podem desencadear a Síndrome de Dumping, caracterizada por tontura, taquicardia e diarreia explosiva devido ao rápido deslocamento osmótico de fluidos para o intestino.
5. Condimentos Irritantes (Pimentas e Molhos Industrializados)
A capsaicina e conservantes químicos agridem a mucosa gastrointestinal em fase de remodelação. A inflamação química da mucosa pode mascarar sinais de alerta e causar desconforto desnecessário.
6. Álcool e Embutidos
O álcool é um agente hepatotóxico e desidratante que interfere na síntese proteica necessária para a cicatrização. Embutidos (salsicha, presunto, salame) contêm níveis elevados de sódio e nitritos, que promovem retenção hídrica e edema de anastomoses.
Aplicação na Cirurgia Digestiva: Especificidades por Procedimento
A tática alimentar deve ser personalizada conforme o “teatro de operações” anatômico:
- Gastrectomias: Fracionamento extremo (6 a 8 refeições). Proibição absoluta: Ingerir líquidos durante as refeições sólidas. Isso acelera o esvaziamento e precipita o Dumping.
- Colecistectomias: Foco em dieta hipogordurosa por pelo menos 15 a 30 dias até a adaptação do esfíncter de Oddi ao fluxo biliar direto.
- Ressecções de Cólon: Evitar fibras insolúveis brutas (cascas de frutas, sementes) nos primeiros dias para não sobrecarregar a área de sutura com volume fecal endurecido.
Pontos-Chave para a Orientação do Paciente
- Mastigação Exaustiva: A digestão mecânica na boca é a primeira linha de defesa contra a sobrecarga das anastomoses.
- Fracionamento: Comer pouco e muitas vezes é o segredo para manter o metabolismo ativo sem gerar distensão.
- Hidratação: Água e chás devem ser consumidos em pequenos goles ao longo do dia, longe das refeições principais.
- Sinais de Alerta: Vômitos, soluços persistentes ou dor abdominal súbita indicam que a progressão da dieta deve ser interrompida (“pausa tática”).
Conclusões Aplicadas
A dieta no pós-operatório de cirurgia digestiva não é um detalhe acessório, mas uma intervenção cirúrgica de caráter biológico. Como cirurgiões e professores, nosso dever é educar o paciente para que ele se torne um aliado tático na sua própria recuperação. Saber o que não comer é tão vital quanto saber o que comer. Ao eliminarmos os alimentos proibidos, estamos blindando o organismo contra complicações mecânicas e funcionais, permitindo que o processo natural de cicatrização ocorra em um ambiente de baixa pressão e inflamação controlada. No “campo de batalha” da recuperação, a disciplina alimentar é a nossa estratégia de elite para garantir uma vitória duradoura contra a doença.
“Que o teu alimento seja o teu único remédio.” — Hipócrates, o pai da medicina. Na cirurgia moderna, a sabedoria reside em saber que a restrição alimentar tática é o caminho mais curto para a liberdade nutricional plena.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#DietaPosOperatória #CirurgiaDigestiva #AlimentosProibidos #ProjetoACERTO #SegurancaDoPaciente
Manobras Cirúrgicas Avançadas no Trauma Abdominal
A Arte da Exposição e o Controle do Caos
Autor: Prof. Dr. Ozimo Gama
Categoria: Cirurgia do Trauma / Técnica Cirúrgica / Anatomia Aplicada
Tempo de Leitura: 18 minutos
Introdução
No “teatro de operações” do trauma abdominal grave, o cirurgião enfrenta o maior de todos os inimigos: o tempo. Quando a cavidade é aberta em uma laparotomia de emergência, a “névoa da guerra” — composta por sangue, coágulos e contaminação entérica — obscurece as lesões vitais. Como ensinam Hirshberg e Mattox no clássico Top Knife, “se você não consegue ver a lesão, você não consegue pará-la”. A cirurgia do trauma não é o lugar para dissecções anatômicas delicadas de livro-texto; é o domínio da exposição tática. O domínio das manobras de rotação visceral e mobilização de órgãos sólidos é o que separa o cirurgião hesitante do estrategista capaz de resgatar um paciente da tríade letal (acidose, hipotermia e coagulopatia). Este artigo aprofunda-se nas manobras fundamentais para o controle de danos e tratamento definitivo dos traumas de órgãos específicos.
Manobras de Exposição e Acesso Vascular
Antes de tratar um órgão específico, o cirurgião deve dominar as grandes manobras de rotação, que permitem o acesso ao retroperitônio e aos grandes vasos.
1. Manobra de Mattox (Rotação Visceral Medial Esquerda)
É a “chave mestra” para o acesso à aorta abdominal suprarrenal e aos vasos renais esquerdos.
- Técnica: Inicia-se com a mobilização do cólon esquerdo (linha de Toldt), estendendo a incisão superiormente, atrás do baço e da cauda do pâncreas. Todo o bloco visceral (cólon, rim, pâncreas e baço) é rotacionado medialmente para a direita.
- Aplicação: Essencial para o controle de sangramentos aórticos próximos ao hiato diafragmático ou lesões da artéria mesentérica superior na sua origem.
2. Manobra de Cattell-Braasch (Rotação Visceral Medial Direita)
Permite a visualização completa do retroperitônio infra e parapancreático.
- Técnica: Realiza-se a mobilização do cólon direito e da base do mesentério do intestino delgado até o ligamento de Treitz. O bloco é rotacionado para a esquerda e para cima.
- Aplicação: Exposição da veia cava inferior (VCI) em toda a sua extensão infra-hepática, dos vasos renais direitos e da aorta infrarrenal.
Manobras Específicas por Órgão
1. Fígado: O Gigante da Hemorragia
O trauma hepático é a principal causa de morte por hemorragia intra-abdominal. As manobras visam o controle do influxo e efluxo sanguíneo.
- Manobra de Pringle: Consiste na oclusão do ligamento hepatoduodenal (veia porta, artéria hepática e via biliar). Se o sangramento persistir após o Pringle, a fonte é provavelmente o efluxo (veias hepáticas ou VCI retro-hepática).
- Mobilização Hepática: Secção dos ligamentos falciforme, coronários e triangulares. Isso permite “trazer o fígado para a linha média”, essencial para suturas em lesões posteriores.
- Packing (Tamponamento): A manobra de controle de danos mais eficaz. Envolve o uso de compressas (“The Big Five”) colocadas entre o fígado e a parede abdominal/diafragma, criando compressão direta sobre a lesão.
2. Baço: Preservação vs. Sacrifício
No trauma esplênico, a decisão é binária: salvar ou retirar.
- Mobilização Esplênica: Através da secção do ligamento esplenorenal. O baço é trazido para a ferida cirúrgica, permitindo a inspeção do hilo e da cauda do pâncreas.
- Técnica: Em pacientes instáveis, a esplenectomia rápida é a conduta tática correta. Suturas esplênicas (esplenorrafias) são reservadas para pacientes estáveis e lesões capsulares simples.
3. Complexo Duodeno-Pâncreas
Devido à sua localização retroperitoneal profunda, as lesões aqui são frequentemente ocultas.
- Manobra de Kocher: Abertura da fáscia de coalescência lateral ao duodeno, permitindo a mobilização da segunda porção do duodeno e da cabeça do pâncreas para a linha média.
- Exposição do Corpo/Cauda: Realizada através da abertura do ligamento gastrocólico (acesso à transcavidade dos epíplons).
A Mentalidade de Controle de Danos
Na prática do cirurgião do aparelho digestivo brasileiro, a aplicação dessas manobras deve seguir a lógica da Cirurgia de Controle de Danos (DCS). No trauma, a técnica deve ser “rápida e suja” (quick and dirty), focada na fisiologia e não na anatomia estética. Por exemplo, em uma lesão pancreática grave com sangramento ativo, a manobra de Kocher extensiva é vital para identificar se há envolvimento da VCI ou da aorta. Se houver contaminação entérica maciça por lesão duodenal, o uso de grampeadores para “fechar as pontas” e realizar o packing é superior a tentativas de reconstruções complexas que consomem tempo e levam à exaustão metabólica.
Pontos-Chave para a Estratégia Operacional
- Exposição Antecipada: Não espere o paciente chocar para realizar uma manobra de Mattox ou Cattell-Braasch. Se há hematoma retroperitoneal em expansão, a manobra deve ser imediata.
- Regra do Pringle: Sempre tente o Pringle primeiro em hemorragias hepáticas; é um teste diagnóstico e terapêutico simultâneo.
- Mobilização Ampla: No trauma, “incisões grandes curam grandes cirurgiões”. Não tente operar através de pequenos acessos; a xifopúbica é a via de regra.
- O Packing é uma Manobra Ativa: O tamponamento deve ser firme e direcionado. Mal executado, ele apenas esconde o sangramento; bem executado, ele salva vidas.
- Respeito aos Grandes Vasos: No retroperitônio, cada milímetro de dissecção exige consciência situacional absoluta das variações anatômicas.
Conclusões Aplicadas à Prática
As manobras cirúrgicas no trauma são ferramentas de Estratégia Operacional. Elas permitem que o cirurgião converta um ambiente de caos absoluto em um cenário de controle relativo. Como Professor de Anatomia, reitero que a técnica manual é inútil sem o mapa mental da anatomia cirúrgica. Dominar a rotação visceral medial e as táticas de tamponamento hepático não é um luxo acadêmico, mas a base da sobrevivência no trauma. Na cirurgia digestiva de urgência, a simplicidade e a rapidez nas manobras de exposição são as maiores virtudes que um cirurgião pode possuir. Lembre-se: no trauma, o cirurgião é o estrategista que decide quando lutar por um órgão e quando recuar para salvar a vida.
“Na cirurgia do politrauma as coisas simples funcionam. Técnicas complexas e manobras sofisticadas permitem belas ilustrações, mas muitas vezes não permitem salvar a vida do paciente.” — Asher Hirshberg e Kenneth Mattox.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#ManobrasCirurgicas #TraumaAbdominal #CirurgiaDeTrauma #TopKnife #AnatomiaCirurgica
Drenos, Sondas e Acessos Vasculares
Sentinelas e Interfaces no Pós-Operatório
Autor: Prof. Dr. Ozimo Gama
Categoria: Cuidados Perioperatórios / Técnica Cirúrgica / Cirurgia do Aparelho Digestivo
Tempo de Leitura: 11 minutos
Introdução
Na prática da cirurgia digestiva de alta complexidade, o cuidado de drenos, sondas e acessos vasculares representa a interface física entre o planejamento tático executado no bloco operatório e a fisiologia do paciente na enfermaria ou UTI. Frequentemente negligenciados, esses dispositivos são, na verdade, sentinelas críticas que fornecem dados em tempo real sobre a homeostase e a integridade das anastomoses. Contudo, vivemos uma mudança de paradigma. Protocolos modernos de aceleração da recuperação, como o ERAS e o brasileiro Projeto ACERTO, têm demonstrado que o uso sistemático e dogmático desses dispositivos pode, em muitos casos, retardar a deambulação e aumentar as taxas de infecção. O cirurgião contemporâneo deve equilibrar a necessidade de monitorização com a premissa de “menos é mais”. Este artigo revisa os fundamentos, as indicações precisas e o manejo desses dispositivos sob uma ótica estratégica e baseada em evidências.
A Trindade da Monitorização e Suporte
A sistematização dos dispositivos cirúrgicos permite uma abordagem organizada para a vigilância do paciente operado.
1. Drenos Cirúrgicos: O “Relator” da Cavidade
O dreno não substitui uma hemostasia rigorosa nem uma anastomose bem feita, mas funciona como um sistema de alerta precoce.
- Drenos de Escoamento (Látex/Penrose): Utilizam a capilaridade. Indicados para coleções superficiais ou espaços contaminados onde se deseja uma comunicação aberta.
- Drenos de Sucção Fechada (Jackson-Pratt/Blake): Operam por pressão negativa. São os preferidos em grandes dissecções (como linfadenectomias D2 ou ressecções pancreáticas), pois permitem a quantificação exata do débito e reduzem o risco de infecção ascendente.
- O “Dreno Falante”: Na cirurgia biliar ou pancreática, a cor do efluente (bilioso, entérico ou “água de lavagem de carne”) é o diagnóstico visual de uma fístula muito antes das alterações laboratoriais.
2. Sondas: Descompressão e Aporte Metabólico
- Sonda Nasogástrica (SNG): O dogma da descompressão gástrica rotineira “até o retorno dos ruídos hidroaéreos” caiu. Atualmente, a SNG é reservada para casos de íleo paralítico prolongado, obstrução intestinal ou no pós-operatório de gdp que evoluiu com gastroparesia prolongada.
- Sondas Nasoenterais e de Ostomia (Gastrostomia/Jejunostomy): São as linhas de suprimento logístico. Em pacientes oncológicos desnutridos, a manutenção do aporte enteral precoce é o fator decisivo para a cicatrização e prevenção de translocação bacteriana.
3. Acessos Vasculares: A Logística de Suporte Vital
- Acessos Periféricos: Suficientes para cirurgias de baixo risco e hidratação de curto prazo.
- Acesso Venoso Central (CVC): Essencial em cirurgias de alta complexidade para monitorização da Pressão Venosa Central (PVC), administração de drogas vasoativas e suporte de Nutrição Parenteral Total (NPT), quando a via enteral está contraindicada.
Avaliação Diária dos Dispositivos: O que avaliar e sinais de alerta
A avaliação diária deve ser metódica, seguindo a lógica da Consciência Situacional tática. O cirurgião deve “ler” o dispositivo como um relatório de inteligência do campo de batalha.
| Dispositivo | O que Avaliar (Checklist) | Sinais de Alerta (Red Flags) |
| Drenos | Volume (curva de débito 24h), coloração, consistência, odor, local da inserção e manutenção do vácuo. | Sangue rutilante (>100ml/h); conteúdo bilioso, entérico ou purulento; perda súbita de vácuo; secreção purulenta no óstio. |
| Sondas | Posicionamento (marcação de profundidade), fixação cutânea, permeabilidade e tolerância à dieta. | Deslocamento/saída acidental; distensão abdominal com sonda “parada”; refluxo de dieta por SNG; dor súbita à infusão. |
| Acessos | Fluxo e refluxo, integridade do curativo, sinais flogísticos no trajeto venoso. | Dor à infusão; edema de membro ipsilateral; febre sem foco aparente; secreção purulenta no sítio de inserção. |
Detalhamento dos Sinais de Alerta
- Hemorragia Sentinela: Um aumento súbito de débito hemático no dreno, mesmo que em volume moderado, pode preceder uma hemorragia maciça (frequentemente por erosão enzimática de vasos no caso de fístulas pancreáticas).
- A “Parada” Suspeita: Um dreno que para de oscilar ou drenar subitamente em um paciente que mantém dor ou distensão sugere obstrução do dispositivo por coágulos ou fibrina, mascarando uma complicação interna.
- Isquemia do Estoma: Em casos de ostomias, a mucosa deve ser avaliada diariamente. Mudança para tons violáceos ou escuros indica sofrimento vascular iminente.
Aplicação na Cirurgia Digestiva
Na cirurgia digestiva brasileira, a racionalização destes dispositivos tem impactado diretamente os indicadores hospitalares. Dados do Projeto ACERTO mostram que a abolição da SNG e do dreno abdominal em colecistectomias e ressecções colorretais eletivas sem intercorrências reduziu o tempo de internação em média 25% a 30%. Entretanto, em cenários de “Teatro de Operações” hostil — como em reoperações por peritonite generalizada ou fístulas de alto débito —, o manejo correto desses dispositivos é o que permite o controle do dano (damage control). Saber posicionar um dreno de Sump para aspiração contínua ou converter uma SNG em sonda de alimentação trans-anastomótica exige um domínio da anatomia e da mecânica de fluidos que é essencial ao cirurgião digestivo.
Pontos-Chave
- Finalidade Específica: Todo dreno ou sonda deve ter uma indicação clara (diagnóstica, descompressiva ou nutritiva). Se você não sabe o que está esperando do dispositivo, ele não deve estar lá.
- Vigilância Qualitativa: O aspecto do conteúdo é tão importante quanto o volume. Mudanças súbitas na cor ou odor são sinais de alerta (red flags).
- Remoção Precoce: A permanência prolongada de drenos e sondas aumenta o risco de infecção hospitalar e formação de fístulas mecânicas.
- Fixação e Mobilidade: Dispositivos mal fixados causam dor e limitam a deambulação precoce, pilar fundamental da recuperação acelerada.
- Acesso Central: Deve ser removido assim que o paciente atinge estabilidade hemodinâmica e tolerância à via oral/enteral, minimizando o risco de sepse relacionada ao cateter.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
Drenos, sondas e acessos não são apenas apêndices do ato operatório; são ferramentas de precisão para a gestão da incerteza. O cirurgião de excelência planeja o posicionamento desses dispositivos ainda na fase de estratégia operacional, antecipando as possíveis complicações que eles deverão denunciar ou tratar. Adoção de protocolos de “desmame” precoce de dispositivos, integrada à vigilância clínica atenta, permite que o paciente cirúrgico digestivo recupere sua autonomia funcional mais rapidamente. No final, o objetivo é que o paciente deixe o hospital com o mínimo de cicatrizes — físicas e sistêmicas — de sua jornada cirúrgica.
“O dreno é um informante; quando ele para de falar, deve ser retirado. Quando ele começa a gritar, o cirurgião deve estar pronto para agir.” — Aforismo clássico da Cirurgia Abdominal.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#ClinicaCirurgica #DrenosESondas #CirurgiaDigestiva #CuidadosPosOperatorios #ProjetoACERTO
Nutrição Perioperatória no Câncer Digestivo
Estratégias para Mitigar Riscos e Otimizar Desfechos Cirúrgicos
Autor: Prof. Dr. Ozimo Gama
Categoria: Nutrição Clínica / Oncologia Cirúrgica / Cirurgia do Aparelho Digestivo
Tempo de Leitura: 12 minutos
Introdução
No âmbito da cirurgia oncológica do aparelho digestivo, a desnutrição não é apenas uma comorbidade; é um fator de risco independente e modificável que impacta diretamente a morbimortalidade operatória. Estimativas globais e dados consolidados apontam que a prevalência de desnutrição em pacientes com câncer varia entre 20% e 85%, atingindo seu ápice justamente nas neoplasias gastrointestinais e hepáticas. No Brasil, onde o Instituto Nacional de Câncer (INCA) estima para o triênio 2023-2025 cerca de 45 mil novos casos de câncer colorretal e 21 mil de câncer gástrico por ano, o cirurgião do aparelho digestivo assume o papel de “arquiteto metabólico”. Compreender que a intervenção nutricional deve começar no momento do diagnóstico — e não apenas no pós-operatório — é fundamental para reduzir taxas de infecção, tempo de internação e custos hospitalares. Este artigo revisa os fundamentos da nutrição perioperatória sob a luz das evidências mais recentes.
Triagem, Sarcopenia e Imunonutrição
1. Triagem e Avaliação Nutricional
A identificação do risco nutricional deve ser universal e precoce. Ferramentas validadas como o MUST (Malnutrition Universal Screening Tool) e o NRS-2002 (Nutritional Risk Screening) são fundamentais para estratificar o paciente. Mais do que a simples perda de peso, devemos atentar para a Sarcopenia (perda de massa e função muscular). Atualmente, a análise da área muscular ao nível da terceira vértebra lombar (L3) em exames de Tomografia Computadorizada é considerada o padrão-ouro para o diagnóstico de miopenia em pacientes oncológicos, permitindo identificar a “obesidade sarcopênica”, onde o excesso de tecido adiposo mascara a depleção muscular proteica.
2. Abreviatura do Jejum e Carga de Carboidratos
O dogma do “NPO após a meia-noite” foi definitivamente substituído por protocolos de aceleração da recuperação, como o ERAS (Enhanced Recovery After Surgery) e o brasileiro Projeto ACERTO. A recomendação atual permite a ingestão de líquidos claros até 2 horas antes da indução anestésica. A oferta de uma bebida rica em carboidratos (maltodextrina a 12,5%) nesse período reduz a resistência insulínica pós-operatória, preserva a massa magra e diminui o desconforto e a ansiedade do paciente, sem aumentar o risco de aspiração broncopulmonar.
3. Imunonutrição
O uso de fórmulas imunomoduladoras — enriquecidas com Arginina, Ácidos Graxos Ômega-3 e Nucleotídeos — tem demonstrado benefícios robustos. A suplementação pré-operatória por 5 a 7 dias em pacientes candidatos a grandes cirurgias digestivas está associada a uma redução significativa nas complicações infecciosas e na deiscência de anastomoses. A arginina, especificamente, atua na melhora da resposta das células T e na síntese de colágeno, essencial para a cicatrização.
Aplicação na Cirurgia Digestiva: O Contexto da Reabilitação
Na prática da cirurgia digestiva de alta complexidade, a nutrição perioperatória é o pilar central da Pré-habilitação. Pacientes com câncer de pâncreas ou esôfago, frequentemente sarcopênicos ao diagnóstico, apresentam melhora drástica nos desfechos quando submetidos a um programa que associa suporte nutricional hiperproteico a exercícios físicos e suporte psicológico antes do ato operatório. A via de escolha deve ser sempre a enteral, preservando a barreira mucosa intestinal e evitando a translocação bacteriana. A Nutrição Parenteral Total (NPT) deve ser reservada para casos de obstrução intestinal completa ou quando a meta calórico-proteica não pode ser atingida por via digestiva em 7 a 10 dias.
Pontos-Chave
- Fator Modificável: A desnutrição é um dos poucos riscos perioperatórios que o cirurgião pode intervir ativamente para melhorar o prognóstico oncológico.
- Triagem Obrigatória: Nenhum paciente oncológico deve ser operado sem uma avaliação de risco nutricional prévia (NRS-2002 ou similar).
- Sarcopenia Oculta: O IMC isolado é insuficiente; a avaliação da massa muscular via imagem (TC em L3) é decisiva para o prognóstico.
- Jejum Moderno: Líquidos claros com carboidratos até 2h antes da cirurgia é o padrão de segurança e conforto metabólico.
- Imunonutrição: Suplementação de 5 a 7 dias pré-operatórios reduz complicações infecciosas em grandes ressecções GI.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
A excelência técnica no bloco operatório — a anastomose perfeita ou a linfadenectomia D2 rigorosa — perde eficácia se o terreno biológico do paciente estiver exaurido. O cirurgião do aparelho digestivo moderno deve prescrever nutrição com o mesmo rigor com que planeja a tática operatória. Integrar os protocolos de nutrição perioperatória à rotina clínica não apenas salva vidas, mas devolve ao paciente a capacidade de enfrentar o tratamento oncológico complementar com maior resiliência. A nutrição deixou de ser um cuidado adjuvante para se tornar uma etapa mandatória da estratégia cirúrgica oncológica.
“A nutrição é o braço direito da medicina e o esquerdo da cirurgia; sem ela, o bisturi mais brilhante corta apenas a carne, mas não cura o organismo.” — Adaptado dos princípios de sustentação vital em cirurgia.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#NutricaoPerioperatória #CirurgiaDigestiva #OncologiaCirurgica #ProjetoACERTO #SegurancaDoPaciente
Princípios Estratégicos Militares
Uma Abordagem Operacional Aplicada às Decisões Complexas em Cirurgia Digestiva
Autor: Prof. Dr. Ozimo Gama
Categoria: Gestão de Risco / Técnica Cirúrgica / Educação Médica Continuada
Tempo de Leitura: 15 minutos
Introdução
No campo da cirurgia do aparelho digestivo de alta complexidade, o cirurgião não é apenas um técnico de mãos habilidosas; ele é, essencialmente, um estrategista. A sala de operações, tal como o campo de batalha, é um ambiente de incerteza, pressão temporal e consequências irrevogáveis. A transposição dos princípios da estratégia militar para o planejamento e execução cirúrgica não é uma mera analogia intelectual, mas uma ferramenta de gestão de risco fundamental para a sobrevivência do paciente. Historicamente, a cirurgia e a guerra caminharam juntas. Contudo, a evolução contemporânea exige que o cirurgião digestivo vá além da tática (o ato de costurar ou dissecar) e domine a Arte Operacional. Conforme os ensinamentos de pensadores como Clausewitz, Sun Tzu e Liddell Hart, a vitória — no nosso caso, a cura e a recuperação plena do doente — depende da capacidade de antecipar o “atrito”, gerenciar a “névoa da guerra” anatômica e aplicar a força (técnica cirúrgica) no ponto de maior impacto com o menor dano colateral. Este artigo visa sistematizar como os pilares da estratégia militar podem ser aplicados às decisões complexas na nossa especialidade.
A Filosofia Estratégica no Teatro de Operações Abdominais
A estratégia, conforme definida por Lawrence Freedman, é a “arte de criar poder” para alcançar objetivos em cenários de conflito. Na cirurgia, o conflito se dá contra a patologia, a inflamação e a variabilidade anatômica.
1. Clausewitz e a “Fricção” Cirúrgica
Carl von Clausewitz, em sua obra clássica Da Guerra, introduziu o conceito de fricção: “Tudo na guerra é muito simples, mas a coisa mais simples é difícil”. Na cirurgia digestiva, a fricção é o sangramento inesperado, a falha de um grampeador, a fadiga da equipe ou a descoberta de uma invasão vascular não detectada na imagem. O cirurgião estrategista deve planejar contando com a fricção. Isso significa ter planos de contingência (Planos B e C) prontos. Se a “missão” original (uma duodenopancreatectomia com preservação pilórica) encontrar uma invasão tumoral da veia porta, o cirurgião deve estar taticamente preparado para a reconstrução vascular, e não ser pego de surpresa.
2. Sun Tzu e a Inteligência (Reconhecimento)
“Se você conhece o inimigo e conhece a si mesmo, não precisa temer o resultado de cem batalhas”. A inteligência militar é o equivalente à nossa propedêutica armada. O uso exaustivo de exames de imagem de alta definição (TC e RM com reconstrução 3D) e biomarcadores é o reconhecimento aéreo do terreno. Operar um tumor sem o estadiamento molecular ou anatômico completo é como enviar tropas para um território desconhecido sem mapas: é um convite ao desastre.
3. Liddell Hart e a “Abordagem Indireta”
B. H. Liddell Hart defendia que o objetivo da estratégia é deslocar o inimigo, não atacá-lo onde ele é mais forte. Na cirurgia oncológica digestiva, a Neoadjuvância (quimioterapia ou radioterapia pré-operatória) é a aplicação máxima deste princípio. Ao invés de um ataque direto a um tumor “borderline” ou localmente avançado — o que poderia resultar em uma cirurgia mutilante e de alto risco —, utilizamos a estratégia indireta para reduzir o tumor, facilitando uma ressecção mais segura e preservadora de órgãos (como no GIST ou no câncer de reto).
Aplicação na Cirurgia Digestiva: Casos Táticos
O Planejamento na Oncologia Digestiva
No Brasil, o cenário epidemiológico é desafiador. Segundo dados do INCA (Estimativa 2023-2025), o câncer colorretal é o segundo mais frequente em homens e mulheres (excetuando pele não melanoma), com cerca de 45.630 novos casos anuais. O câncer gástrico segue com mais de 21.000 casos. Perante esses números, o cirurgião atua em uma campanha de longa duração. A estratégia exige que a Linfadenectomia (D2 no estômago, por exemplo) seja executada com precisão militar. Deixar território inimigo (linfonodos comprometidos) para trás é garantir a contraofensiva da doença (recidiva).
A Disciplina da “Visão Crítica de Segurança” (CVS)
Na colecistectomia laparoscópica, a lesão da via biliar é o equivalente a um “fogo amigo”. A aplicação do CVS de Strasberg é um protocolo de disciplina operacional. O cirurgião é obrigado a completar três critérios objetivos (limpeza do triângulo de Calot, separação do leito hepático e identificação das duas únicas estruturas) antes de “disparar” os clipes. É a vitória da doutrina sobre a pressa.
O “Bail-out” como Retirada Estratégica
Na estratégia militar, saber quando recuar para preservar as tropas é um sinal de liderança superior, não de fraqueza. Na cirurgia complexa, quando a anatomia está “congelada” ou a instabilidade hemodinâmica do paciente é crítica, o cirurgião deve optar por procedimentos de saída (bail-out), como a colecistectomia subtotal ou a cirurgia de controle de danos (damage control). O objetivo estratégico é a sobrevivência do paciente, não a conclusão de uma técnica específica a qualquer custo.
Pontos-Chave para a Prática Diária
- Unidade de Comando: O cirurgião principal deve liderar a equipe multidisciplinar de forma clara, garantindo que anestesistas, enfermeiros e auxiliares conheçam os objetivos da missão.
- Simplicidade Operacional: Planos excessivamente complexos falham sob pressão. Busque a tática mais direta e segura para alcançar o objetivo oncológico ou funcional.
- Logística de Retaguarda: Garanta que o “armamento” (grampeadores, energia, fios) e o suporte (Banco de Sangue, UTI) estejam prontos antes do início da operação.
- Consciência Situacional: Mantenha a calma durante a “fricção”. Se o sangramento ocorrer, a primeira manobra é o controle (compressão), seguida da análise tática da solução, nunca o pânico.
- Debriefing (Análise Pós-Ação): Cada cirurgia deve ser revisada pela equipe para identificar falhas táticas e melhorar os processos para o próximo “combate”.
Conclusões Aplicadas à Prática do Cirurgião Digestivo
A excelência na cirurgia digestiva de alta complexidade exige uma mudança de mentalidade. Devemos abandonar a visão puramente técnica e abraçar a visão estratégica. O bisturi é apenas o instrumento; a inteligência estratégica é o que dita onde e como ele deve ser usado. Integrar os princípios militares de reconhecimento, disciplina operacional e abordagem indireta permite que o cirurgião navegue com segurança por anatomias distorcidas e biologias agressivas. Como líderes no teatro de operações do abdome, nosso dever é converter a incerteza em resultados previsíveis, garantindo que cada decisão complexa seja fundamentada em princípios que resistiram ao teste do tempo, tanto nos campos de batalha quanto nos centros cirúrgicos.
“Tudo na guerra é simples, mas a coisa mais simples é difícil. As dificuldades se acumulam e acabam produzindo um tipo de atrito que é impensável para quem não presenciou a guerra.” — Carl von Clausewitz. Na cirurgia digestiva, o atrito é a realidade; a estratégia é a nossa única defesa.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#EstrategiaCirurgica #CirurgiaDigestiva #GestaoDeRisco #OncologiaCirurgica #DecisaoMedica
Colecistectomia: O perigo da falsa “Simplicidade”
A cirurgia de retirada da vesícula biliar é a mais comum da especialidade digestiva, mas a percepção de que é um procedimento “simples” esconde riscos catastróficos que exigem uma nova cultura de segurança.
Todos conhecemos alguém que já “tirou a vesícula”. No Brasil, apenas pelo Sistema Único de Saúde (SUS), são realizadas mais de 200 mil colecistectomias anualmente. A introdução da técnica laparoscópica — a cirurgia por vídeo — na década de 1990, trouxe benefícios inquestionáveis: cicatrizes mínimas, menos dor e um retorno quase imediato ao trabalho. No entanto, essa aura de facilidade criou uma armadilha perigosa tanto para pacientes quanto para cirurgiões: a banalização de um procedimento que, em segundos, pode transformar uma patologia benigna em uma tragédia crônica.
O paradoxo é alarmante. Apesar do avanço tecnológico e da vasta experiência acumulada em três décadas, a incidência de lesão da via biliar (LVB) — o dano aos canais que transportam a bile do fígado ao intestino — permanece obstinadamente estável, ocorrendo em cerca de 0,3% a 0,5% dos casos por vídeo. Surpreendentemente, esta taxa é superior à da antiga era da cirurgia aberta. O que a literatura médica qualifica como a “lesão clássica” não é, em regra, fruto de imperícia manual ou falta de conhecimento anatômico, mas sim de uma “ilusão de percepção visual”.
Estudos seminais indicam que 97% das lesões ocorrem porque o cérebro do cirurgião, enganado pela tração e pela inflamação, identifica o ducto biliar principal como se fosse o ducto cístico. É um erro cognitivo, não técnico. Por isso, a colecistectomia não pode ser tratada como um procedimento de “entrada” ou de menor importância. Ela exige o que chamamos de Visão Crítica de Segurança (CVS), uma doutrina sistematizada pelo cirurgião Steven Strasberg que obriga a identificação cabal de estruturas antes de qualquer corte. Sem CVS, não há segurança; há apenas sorte.
A banalização também se manifesta na resistência em adotar as chamadas “manobras de resgate” (bailout). Diante de uma vesícula hostil, com inflamação severa que impede a visão clara da anatomia, o cirurgião prudente deve ter a humildade e a sabedoria de interromper a dissecação clássica. Técnicas como a colecistectomia subtotal — onde parte do órgão é deixada para preservar a via biliar — devem ser vistas como um sinal de maturidade clínica e “sabedoria cirúrgica”, e não como um fracasso. O objetivo final nunca deve ser “tirar a vesícula a qualquer custo”, mas sim “não lesar o paciente”.
O custo humano de uma lesão biliar é imenso. O paciente, outrora saudável, pode tornar-se o que a literatura tragicamente apelida de “aleijado biliar”, enfrentando múltiplas reoperações, internações prolongadas e o risco de cirrose biliar secundária. O impacto médico-legal e o custo para o sistema de saúde são igualmente devastadores.
Felizmente, estamos em uma nova fronteira. O uso de fluorescência com verde de indocianina (ICG), que permite “enxergar” os canais biliares através do tecido, e a integração da Inteligência Artificial como um “segundo par de olhos” no monitor, prometem reduzir a margem para o erro humano. Todavia, a tecnologia sozinha não basta.
É preciso consolidar uma Cultura de Segurança em Colecistectomia (COSIC). Isso envolve desde a documentação fotográfica rigorosa dos passos cirúrgicos até a coragem de pedir ajuda ou converter o procedimento quando a anatomia se torna um enigma. A colecistectomia laparoscópica é uma vitória da medicina moderna, mas sua eficácia depende do reconhecimento de que, sob sua aparente simplicidade, reside uma das operações mais perigosas da cirurgia abdominal. Respeitar essa complexidade é o primeiro passo para proteger a vida de milhares de brasileiros que passam por nossas mesas de operação todos os dias.
Prof. Dr. Ozimo Gama | Cirurgião Digestivo
Planejamento da Cirurgia Digestiva de Alta Complexidade
Adaptação Estratégica das Operações Militares Especiais
Autor: Prof. Dr. Ozimo Gama Categoria: Gestão de Risco / Técnica Cirúrgica / Educação Médica
Tempo de Leitura: 12 minutos
Introdução
No campo da cirurgia do aparelho digestivo de alta complexidade — como em duodenopancreatectomias, ressecções hepáticas maiores ou exenterações pélvicas —, o cirurgião não entra apenas em uma sala de operações; ele adentra um “Teatro de Operações”. A intersecção entre a ciência médica e a estratégia militar não é apenas metafórica; é uma aplicação prática de princípios de elite para mitigar riscos catastróficos. A filosofia das Operações Especiais (SpecOps) foca na obtenção de superioridade relativa em ambientes hostis e incertos. Para o cirurgião digestivo, o abdome “congelado” por múltiplas cirurgias ou por invasão neoplásica é esse ambiente. Este artigo propõe uma transposição da doutrina tática para o planejamento cirúrgico, visando elevar a taxa de sucesso da “missão” e a segurança do paciente.

A Doutrina das Operações Especiais na Cirurgia
A estratégia de operações de elite baseia-se em pilares como Inteligência, Simplicidade, Repetição e Velocidade. Transpostos para a prática cirúrgica de um especialista em Cirurgia do Aparelho Digestivo, esses conceitos transformam a condução do caso:
1. Inteligência (Propedêutica e Reconhecimento)
Em Operações Especiais, nenhuma missão avança sem o reconhecimento profundo do terreno. Na cirurgia digestiva complexa, isso se traduz no uso exaustivo de biomarcadores e exames de imagem de última geração, como a Tomografia Computadorizada (TC) e a Ressonância Magnética (RM) com reconstrução tridimensional. No Brasil, onde o volume de câncer gástrico e colorretal é expressivo, a identificação precisa das relações vasculares e da invasão de órgãos adjacentes é o “reconhecimento aéreo” que define a ressecabilidade.
2. Simplicidade e Tática
A estratégia militar ensina que planos excessivamente complexos falham sob pressão. O planejamento deve ser cirurgicamente simples: identificar as estruturas vitais (pontos de controle) e isolar o alvo (tumor ou processo inflamatório). A técnica de “no-touch” em tumores como o GIST é uma aplicação tática de proteção do perímetro para evitar a sementeira peritoneal.
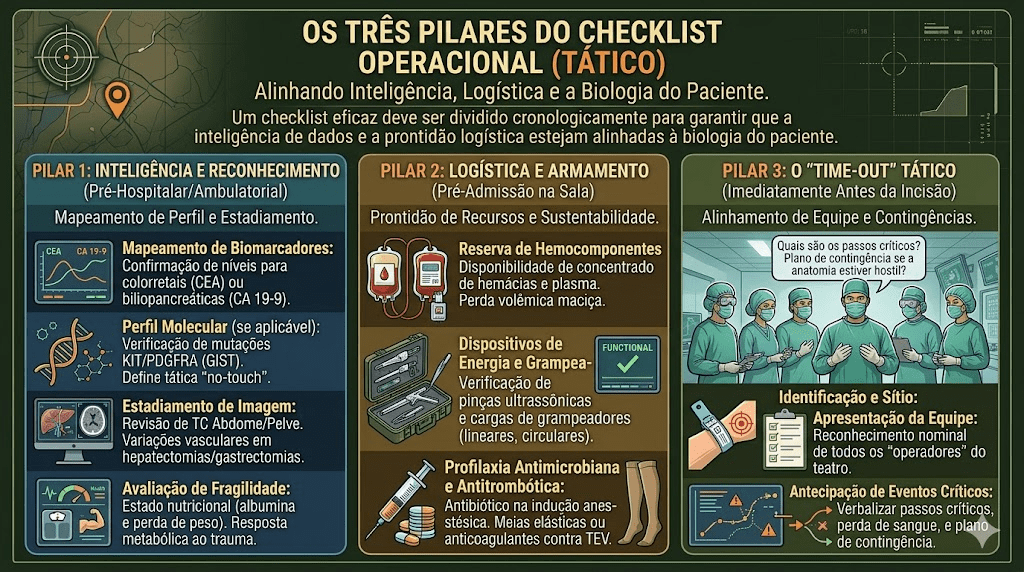
CHECKLIST TÁTICO
Um checklist eficaz deve ser dividido cronologicamente para garantir que a inteligência de dados e a prontidão logística estejam alinhadas à biologia do paciente.
2.1. Inteligência e Reconhecimento (Pré-Hospitalar/Ambulatorial)
- Mapeamento de Biomarcadores: Confirmação dos níveis de CEA para tumores colorretais ou CA 19-9 para lesões biliopancreáticas.
- Perfil Molecular (se aplicável): Verificação de mutações KIT ou PDGFRA em casos de suspeita de GIST para definição de tática de ressecção “no-touch”.
- Estadiamento de Imagem: Revisão da Tomografia de abdome e pelve para identificar variações anatômicas vasculares, cruciais em hepatectomias ou gastrectomias.
- Avaliação de Fragilidade: Checagem do estado nutricional (albumina e perda de peso) para prever a resposta metabólica ao trauma.
2.2. Logística e Armamento (Pré-Admissão na Sala)
- Reserva de Hemocomponentes: Garantia de disponibilidade de concentrado de hemácias e plasma, especialmente em casos com potencial de perda volêmica maciça.
- Dispositivos de Energia e Grampeamento: Verificação da funcionalidade de pinças ultrassônicas e disponibilidade de cargas para grampeadores lineares e circulares.
- Profilaxia Antimicrobiana e Antitrombótica: Confirmação da administração do antibiótico na indução anestésica e início das medidas mecânicas (meias elásticas) ou farmacológicas contra o tromboembolismo venoso.
2.3. O “Time-out” Tático (Imediatamente Antes da Incisão)
- Identificação e Sítio: Confirmação verbal do nome do paciente, procedimento e local da incisão (lateralidade).
- Apresentação da Equipe: Reconhecimento nominal de todos os “operadores” do teatro (cirurgiões, anestesista, instrumentador e circulante).
- Antecipação de Eventos Críticos: O cirurgião deve verbalizar: “Quais são os passos críticos? Qual a perda de sangue esperada? Qual o plano de contingência se a anatomia estiver hostil?”
3. Ensaio e Simulação (O “Sand Table”)
Antes de uma incursão, equipes de elite realizam ensaios exaustivos. O cirurgião moderno deve realizar o “ensaio mental” ou simulação computacional, antecipando cada passo da dissecção e as possíveis contraofensivas da patologia (ex: sangramento massivo inadvertido).
O Plano de Contingência
A aplicação prática dessa estratégia exige que o cirurgião atue com uma mentalidade de comando:
- Superioridade Relativa: Alcançar o controle vascular antes da manipulação da massa tumoral. Em cirurgias hepáticas, a manobra de Pringle é um exemplo de interdição logística temporária para garantir a segurança no terreno principal.
- Gestão da “Névoa da Guerra”: Durante a operação, surgem achados imprevistos (aderências firmes, variações anatômicas). O cirurgião deve possuir a Flexibilidade Tática para alterar a via de acesso ou realizar procedimentos de saída (bail-out), como a colecistectomia subtotal, se a anatomia se tornar inidentificável.
- Estatísticas e Realidade Brasileira: No Brasil, a oncologia cirúrgica digestiva enfrenta o desafio do diagnóstico tardio. Operar pacientes com doenças avançadas exige um planejamento que considere a Logística de Resgate — a capacidade da equipe multidisciplinar e da UTI em manejar a resposta metabólica ao trauma sistêmico.
Pontos-Chave para a Prática Diária
- Unidade de Comando: O cirurgião principal deve liderar a equipe multidisciplinar de forma clara e direta no bloco.
- Checklist Tático: Não é apenas uma burocracia; é a verificação de que todo o “armamento” (grampeadores, energia avançada, fios específicos) está funcional e disponível.
- Consciência Situacional: Avaliar constantemente o tempo cirúrgico e o estado hemodinâmico do paciente, sabendo quando recuar para preservar a vida.
- Análise Pós-Ação: Revisar o vídeo da cirurgia ou o relato cirúrgico detalhado para identificar falhas táticas e melhorar na próxima missão.
Conclusões Aplicadas
A cirurgia digestiva de alta complexidade é um exercício de ética e estratégia. Ao incorporar a disciplina e o planejamento rigoroso das Operações Militares Especiais, o cirurgião deixa de ser um mero executor técnico para se tornar um estrategista da cura. A missão nunca é apenas remover um órgão; a missão é restaurar a homeostase e a dignidade do paciente com a menor agressão possível. Em um país com a diversidade epidemiológica do Brasil, onde o câncer colorretal é o segundo mais comum em mulheres e o terceiro em homens, a precisão tática não é um diferencial — é uma obrigação de sobrevivência.
“A vitória pertence àqueles que mais acreditam nela e a planejam pelo tempo mais longo.” — Napoleão Bonaparte, cujas táticas de organização e logística ainda ecoam na estruturação de grandes serviços cirúrgicos mundiais.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
1º Dia de Pós-Operatório
(PO1): O Mapa de Navegação na Cirurgia Digestiva Complexa
Autor: Prof. Dr. Ozimo Gama
Categoria: Cuidados Perioperatórios / Semiologia Cirúrgica / Cirurgia do Aparelho Digestivo
Tempo de Leitura: 12 minutos
Introdução
O término de uma cirurgia digestiva de alta complexidade — seja uma duodenopancreatectomia, uma gastrectomia total oncológica ou uma hepatectomia maior — não marca o fim da batalha, mas o início de uma nova e crítica fase: a recuperação metabólica e fisiológica. Para o cirurgião, o Primeiro Dia de Pós-Operatório (PO1), geralmente transcorrido em uma Unidade de Terapia Intensiva (UTI), é as “24 horas de ouro”. Neste período, o organismo do paciente está imerso na resposta endócrino-metabólica ao trauma (REMIT). A linha que separa a evolução fisiológica esperada da complicação catastrófica é extremamente tênue. Para o estudante de medicina e o residente de cirurgia, dominar a semiologia cirúrgica do PO1 não significa apenas olhar para exames laboratoriais ou monitores multiparamétricos; significa resgatar a essência da beira do leito. A mão que opera deve ser a mesma mão que examina. Neste artigo, detalharemos o que buscar, o que tocar e como interpretar os sinais de alerta no paciente cirúrgico grave.
1. Avaliação Sistêmica: O Paciente como um Todo
A avaliação do abdome começa muito antes de tocar no abdome do paciente. O exame inicia-se na porta do quarto.
- Estado Neurológico e Nível de Consciência: Um paciente agitado, confuso ou torporoso no PO1 não está simplesmente “sob efeito residual da anestesia”. O delirium hipo ou hiperativo pode ser o primeiro sinal de hipóxia, hipercapnia ou choque (hipoperfusão cerebral). A avaliação do despertar e da orientação (escala de Glasgow) é inegociável.
- Perfusão Periférica e Diurese: A pele fala. Extremidades frias, pegajosas e tempo de enchimento capilar lentificado (> 3 segundos) indicam má perfusão tecidual. Simultaneamente, o débito urinário é a “janela dos rins” para a volemia. A oligúria (< 0,5 ml/kg/h) no PO1 de uma grande cirurgia exige diagnóstico diferencial imediato entre hipovolemia (sangramento/desidratação) e falência renal aguda.
- Sinais Vitais (O Radar do Cirurgião):
- Taquicardia: É o sinal vital mais subestimado. Nunca atribua uma taquicardia (> 100 bpm) apenas à “dor” ou “ansiedade” sem antes descartar as duas maiores ameaças do PO1: Hemorragia e Vazamento Anastomótico Precoce.
- Febre: Temperaturas de até 38°C nas primeiras 24-48h são frequentemente decorrentes da atelectasia pulmonar ou da resposta inflamatória fisiológica ao trauma. Infecções de sítio cirúrgico são raras no PO1. Contudo, febre alta acompanhada de instabilidade hemodinâmica exige descartar lesão inadvertida de alça intestinal ou infecção necrosante.
2. O Exame Físico Abdominal Direcionado
A semiologia do abdome operado difere da semiologia clássica. A dor incisional confunde a avaliação de irritação peritoneal. O cirurgião deve ser sutil e metódico.
- Inspeção: O abdome está distendido? Uma distensão progressiva e tensa no PO1 levanta forte suspeita de hemoperitônio (sangramento interno) ou dilatação gástrica aguda.
- Palpação e Percussão: A palpação deve começar distante da incisão cirúrgica. O objetivo é diferenciar a dor da ferida (esperada) da dor peritonítica profunda (sinal de alarme). A percussão dolorosa (sinal de irritação peritoneal) generalizada em uma cirurgia que deveria ser limpa é um grito de socorro do abdome.
- Ausculta: O íleo adinâmico é fisiológico nas primeiras 24 a 72 horas após grande manipulação entérica. A ausência de ruídos hidroaéreos é esperada, mas a sua presença precoce é um excelente prognóstico.
- Ferida Operatória: Inspecionar o curativo. Um sangramento que encharca o curativo repetidamente nas primeiras horas exige exploração. Observar sinais precoces de isquemia das bordas da ferida ou hematoma expansivo.
3. A Janela da Cavidade: Drenos e Estomas
Os dispositivos deixados no paciente são os relatores da cavidade abdominal. Eles devem ser examinados com rigor obsessivo.
- Drenos Cavitários: Não anote apenas o “volume”, mas a qualidade do efluente.
- Sero-hemático: Esperado no PO1 de grandes dissecções (ex: linfadenectomia).
- Sangue vivo (Hemático): Um débito hemático > 100 a 150 ml/hora no dreno tubular é indicativo de hemorragia ativa (falha na hemostasia, deslizamento de ligadura arterial).
- Bilioso, Entérico ou Purulento: É indicativo de desastre. Uma fístula entérica/biliar no PO1 geralmente significa falha técnica da anastomose ou lesão iatrogênica não reconhecida no intraoperatório.
- Estomas (Colostomia/Ileostomia): A vitalidade do estoma deve ser atestada no PO1. A mucosa deve ser de coloração vermelho-rósea e úmida. Uma coloração violácea, pálida ou enegrecida é diagnóstico de isquemia ou necrose do estoma, exigindo reintervenção cirúrgica de urgência.
4. Sinais de Alerta para Eventos Adversos
O cirurgião do aparelho digestivo deve estar programado para identificar padrões sindrômicos que indicam catástrofes:
- A Síndrome Hemorrágica: Taquicardia progressiva + hipotensão + palidez + oligúria + queda abrupta de Hemoglobina/Hematócrito + dreno com saída de sangue rutilante. Conduta: Ressuscitação volêmica, transfusão maciça e reoperação hemostática imediata.
- A Síndrome Isquêmica Intestinal: Dor abdominal atroz, refratária a doses elevadas de opioides, muitas vezes desproporcional aos achados do exame físico abdominal, associada a acidose metabólica grave (lactato elevado). Comum após revascularizações mesentéricas ou cirurgias com baixo débito prolongado.
- A Síndrome da Deiscência Catastrófica: Instabilidade hemodinâmica súbita, taquicardia inexplicada e abdome em tábua (se não houver analgesia peridural que mascare o quadro).
Pontos-Chave para a Prática Diária do Residente
- A dor nunca é subestimável: Se a dor operatória mudou de padrão, piorou subitamente ou não cede à analgesia potente, presuma uma complicação (isquemia, perfuração, sangramento) até prova em contrário.
- O Dreno fala a verdade: Conheça a localização exata de cada dreno que você deixou na cavidade. Um dreno próximo a uma anastomose pancreática que apresenta débito de “água de lavagem de carne” espessa pode ser o prenúncio de uma fístula.
- O Exame é Seriado: A semiologia no PO1 não é uma “fotografia” tirada no round da manhã; é um “filme”. Avaliar o paciente de manhã, à tarde e à noite é a única forma de perceber a deterioração clínica antes do choque irreversível.
- Laboratório não substitui o dedo: Uma tomografia ou um exame de sangue não substituem a mão do cirurgião no abdome e a reavaliação clínica constante.
Conclusões Aplicadas
A semiologia cirúrgica no primeiro dia de pós-operatório é uma dança complexa entre a ciência da fisiologia e a arte da observação clínica. Na cirurgia digestiva de alta complexidade, o sucesso oncológico e técnico obtido no centro cirúrgico precisa ser consolidado na UTI através da vigilância implacável do cirurgião. Delegar a avaliação do paciente exclusivamente aos intensivistas, eximindo-se de tocar o abdome e checar os drenos, é o primeiro passo para o fracasso. A intuição do cirurgião que operou, baseada numa semiologia apurada, é insubstituível na detecção precoce do evento adverso, permitindo a transição de um “resgate heroico” para um “manejo planejado”.
“Aumente o seu poder de observação… Veja a cor da pele, sinta a pulsação, observe a respiração. Não delegue as suas mãos e os seus olhos para as máquinas. O diagnóstico precoce das complicações cirúrgicas está escrito no rosto e no abdome do paciente, para quem tiver olhos para ler.” — Adaptação dos princípios semiológicos de John B. Murphy, pioneiro da cirurgia abdominal moderna.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags:
#SemiologiaCirurgica #PosOperatorio #CirurgiaDigestiva #CuidadosIntensivos #ResidenciaMedica
Fundamentos da Oncologia Digestiva
Epidemiologia, Marcadores Tumorais e Princípios Cirúrgicos
Por: Prof. Dr. Ozimo Gama
1. Introdução: O Panorama da Oncologia Digestiva
O aumento progressivo da expectativa de vida e o consequente envelhecimento populacional trouxeram consigo um incremento significativo na incidência das neoplasias malignas. Na prática clínica e acadêmica, observamos que, embora os avanços na propedêutica diagnóstica e os sistemas de triagem tenham evoluído, uma parcela considerável de pacientes ainda é diagnosticada em estágios avançados. Esse cenário impõe desafios terapêuticos complexos, elevando a morbimortalidade e os custos para o sistema de saúde. O diagnóstico precoce, idealmente em fases pré-neoplásicas, permanece como o objetivo primordial para a melhoria dos desfechos clínicos. De acordo com os dados mundiais do projeto GLOBOCAN (WHO, 2008), a estimativa global superou os 12 milhões de novos casos de câncer, com mais de 7 milhões de óbitos anuais. No cenário brasileiro, as projeções do Instituto Nacional do Câncer (INCA, 2012) ratificam a magnitude do problema no aparelho digestivo, com destaque para as seguintes incidências:
- Câncer Colorretal: 30.140 casos.
- Câncer de Estômago: 20.090 casos.
- Câncer de Esôfago: 10.420 casos.
2. Desenvolvimento: Biologia Tumoral e Biomarcadores
Os biomarcadores, ou marcadores tumorais, são estruturas moleculares ou teciduais que permitem prever o comportamento biológico de uma neoplasia. No contexto da oncologia digestiva, sua utilidade reside primordialmente na avaliação prognóstica e no seguimento pós-operatório para detecção de recidivas. É imperativo ressaltar que, devido às limitações de sensibilidade e especificidade — especialmente em fases precoces —, a maioria desses marcadores não é indicada para o rastreamento (screening) populacional.
Abaixo, elenco os principais marcadores, seus valores referenciais superiores (conforme Tabela 18.2) e nuances clínicas:
- CEA (Antígeno Carcinoembrionário): Marcador fundamental no carcinoma colorretal. Valor referencial: < 3 ng/mL. Deve-se atentar que níveis elevados podem ser encontrados em tabagistas, o que exige cautela na interpretação.
- AFP (Alfa-fetoproteína): Crucial no diagnóstico do carcinoma hepatocelular. Valor referencial: < 9 U/L. Sua aplicação em screening é aceita apenas em grupos de alto risco, como pacientes com cirrose hepática ou portadores crônicos de Hepatite B e C. Gestação e doenças hepáticas não neoplásicas são causas comuns de falso-positivos.
- CA 19-9: Utilizado na propedêutica de tumores de pâncreas e vias biliares. Valor referencial: < 37 U/mL.
- CA 72-4: Marcador com alta especificidade para o carcinoma gástrico, útil no monitoramento da resposta terapêutica. Valor referencial: < 4 U/mL.
- SCCA (Squamous Cell Carcinoma Antigen): Indicado para o seguimento de carcinomas de células escamosas, notadamente no esôfago e canal anal. Valor referencial: < 1,5 mg/L.
3. GIST e Tumores Neuroendócrinos (TNE)
GIST (Tumor Estromal Gastrointestinal)
O GIST é a neoplasia mesenquimal mais comum do trato digestório, originando-se das células intersticiais de Cajal. Sua patogenia molecular é marcada por mutações nos genes c-kit (proteína KIT/CD117, presente em cerca de 95% dos casos) e PDGFRA (em 5-10% dos casos). O potencial de malignidade e o risco de comportamento agressivo são determinados tecnicamente pelo tamanho tumoral e pelo índice mitótico (Tabela 19.2). O advento do Mesilato de Imatinibe revolucionou o tratamento como terapia-alvo eficaz para ambas as mutações citadas.
TNE (Tumores Neuroendócrinos)
Os TNE constituem um grupo heterogêneo classificado conforme o índice mitótico e a expressão do Ki-67. A diferenciação é vital para o prognóstico:
- G1 e G2: Tumores Neuroendócrinos bem diferenciados.
- G3: Denominados Carcinomas Neuroendócrinos (NEC), caracterizados por comportamento altamente agressivo e Ki-67 > 20%.
A Síndrome Carcinoide (rubor facial, diarreia e valvulopatia) é mediada pela serotonina. O marcador pan-neuroendócrino de eleição é a Cromogranina A, uma proteína presente nos grânulos secretórios das células neuroendócrinas.
4. Aplicação na Cirurgia Digestiva
A ressecção cirúrgica é o pilar do tratamento curativo. O objetivo técnico é a obtenção de margens microscopicamente negativas (Ressecção R0).
No manejo do GIST, a estratégia cirúrgica possui particularidades: a linfadenectomia de rotina não é indicada devido à raridade da disseminação linfática. A técnica deve priorizar a ressecção em bloco com uma margem de segurança de 1 cm, garantindo a integridade da pseudocápsula tumoral para evitar a disseminação peritoneal por ruptura.
Para os Tumores Neuroendócrinos, a conduta é multidisciplinar. Em pacientes com doença avançada e sintomas hormonais intratáveis, a cirurgia citorredutora (debulking) pode ser empregada para controle clínico e ganho de sobrevida.
5. Pontos-Chave para a Prática Médica
Para a formação técnica de residentes e pós-graduandos, os seguintes conceitos são fundamentais:
- Estadiamento TNM: Permanece como o principal determinante prognóstico e guia soberano para indicação de terapias neoadjuvantes e adjuvantes.
- Seguimento Pós-operatório: O CEA é o marcador padrão no seguimento do câncer colorretal, mas sua interpretação deve considerar o status tabágico do paciente.
- Biologia Molecular do GIST: A análise das mutações KIT e PDGFRA é indispensável para o planejamento da terapia biológica com Imatinibe.
- Margens Cirúrgicas: No GIST, a margem R0 com 1 cm de segurança é o parâmetro técnico ideal para evitar recidivas locais.
- Impacto do Estágio na Sobrevida: A disparidade na sobrevida de 5 anos reforça a urgência do diagnóstico precoce. No Câncer de Esôfago, por exemplo, a sobrevida cai drasticamente de 37% em doença localizada para apenas 3% em casos metastáticos (Tabela 17.3).
6. Considerações Finais
A oncologia digestiva moderna exige que o cirurgião domine conhecimentos que transcendem a técnica operatória pura, integrando epidemiologia, biologia molecular e princípios de farmacogenômica. A educação médica continuada e o entendimento rigoroso dos biomarcadores são as ferramentas capazes de mitigar as disparidades nas taxas de sobrevida.
Como bem afirmou Theodor Billroth: “Apenas o homem que está familiarizado com a arte e a ciência do passado é capaz de auxiliar no progresso do futuro.”
Gostou ❔ Nos deixe um comentário ✍️, compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
#OncologiaDigestiva #CirurgiaGeral #EducaçãoMédica #GIST #ResidênciaMédica
Semiologia Cirúrgica do Aparelho Digestivo
A Arte do Diagnóstico Clínico
1. Introdução à Semiologia do Aparelho Digestivo
A semiologia é a pedra angular da prática cirúrgica de excelência. Ela transcende a mera coleta de dados, constituindo-se na harmoniosa composição entre a anamnese — a fase subjetiva em que decodificamos a percepção do paciente — e o exame físico, a fase objetiva na qual o cirurgião exerce sua soberania técnica. Vivemos em uma era de avanços tecnológicos vertiginosos, contudo, o raciocínio clínico permanece insubstituível. Através da semiotécnica apurada, somos capazes de transformar sintomas específicos em hipóteses diagnósticas seguras. Para o cirurgião do aparelho digestivo, a semiologia não é apenas o prelúdio para a propedêutica armada; é o filtro que direciona a solicitação racional de exames complementares e define o diagnóstico diferencial, garantindo que o bisturi nunca preceda o raciocínio clínico apurado.
2. A Anamnese e a História Clínica Detalhada
O diagnóstico clínico diferencial inicia-se na meticulosidade da história clínica. Além da identificação e da queixa principal, o cirurgião deve aprofundar-se na história médica e, crucialmente, na história odontológica. Não negligenciem a investigação de tratamentos prévios: a realização de cirurgias orais, maiores ou menores, pode revelar defeitos ósseos na região bucomaxilofacial ou ausência de elementos dentários que comprometem a primeira fase da digestão. Questionem sobre hábitos de higiene (frequência de escovação e uso de fio dental), pois estes são marcadores indiretos da saúde sistêmica do indivíduo. É imperativo registrar, sob absoluto sigilo profissional, o uso de álcool, fumo e drogas ilícitas. Observem que a via de administração de certas substâncias pode gerar lesões mucosas específicas. Na investigação farmacológica, o uso de Anti-inflamatórios Não Esteroides (AINEs) e Ácido Acetilsalicílico (AAS) deve ser exaustivamente pesquisado. Em pacientes idosos (acima de 65 anos), tais medicamentos elevam exponencialmente o risco de úlceras pépticas complicadas, manifestando-se frequentemente por hemorragias graves ou perfurações sem pródromos exuberantes.
3. Semiologia da Cavidade Oral: A Porta de Entrada
O exame da cavidade oral é o primeiro passo da exploração física. Devemos dominar os recursos semiotécnicos fundamentais:
- Inspeção: Exige iluminação adequada e auxílio de afastadores para avaliar simetria, cor e mensuração.
- Palpação: O tato revela a textura (lisa ou rugosa) e a consistência (mole, fibrosa ou dura).
- Olfação: Embora subestimada, é soberana ao identificar o odor cetônico do diabetes descompensado ou o fétido odor de necrose em carcinomas avançados.
Lesões Fundamentais da Mucosa
Para uma linguagem técnica universal, devemos ser precisos em nossas definições:
- Mancha ou Mácula: Alteração de cor sem alteração de relevo.
- Pápula: Formação sólida elevada de até 5 mm.
- Placa: Formação sólida, plana e elevada, superior a 5 mm.
- Nódulo: Formação sólida, com elevação ou profundidade, de tamanho variado.
- Vesícula e Bolha: Acúmulo de líquido intratecidual (limite de 3 mm para diferenciação).
- Erosão: Perda parcial do tecido epitelial que não ultrapassa a muscularis mucosae.
- Úlcera: Perda total do epitélio com exposição do tecido conjuntivo, frequentemente recoberta por uma membrana fibrinosa amarela ou esbranquiçada.
Atenção Clínica: O cirurgião deve estar alerta para a Leucoplasia, a principal desordem cancerizável, e o Carcinoma de Células Escamosas, que frequentemente se apresenta como uma úlcera de bordas elevadas e endurecidas no assoalho bucal ou bordas laterais da língua.
4. Semiologia do Esôfago: Disfagia e Refluxo
As patologias esofágicas derivam primordialmente de distúrbios na condução do bolo alimentar ou na falha do mecanismo antirrefluxo.
| Tipo de Disfagia | Características Clínicas | Achados Associados & Causas |
| Orofaríngea | Dificuldade inicial; engasgos, tosse, regurgitação nasal. | AVE, Miastenia Gravis, Divertículo de Zenker. |
| Esofágica Obstrutiva | Parada do alimento após deglutição; progressão rápida para líquidos. | Neoplasia (tabagismo/etilismo), Estenose Péptica (pirose crônica). |
| Esofágica Motora | Progressão lenta ou intermitente para sólidos e líquidos. | Acalasia (Chagas), Esclerose Sistêmica (Raynaud/Esclerodactilia). |
Nuance Diagnóstica na DRGE: É vital compreender que sintomas típicos como pirose e regurgitação apresentam elevada sensibilidade (89-95%), porém sua especificidade é baixa (6-38%). Tal fato justifica a necessidade de exames complementares como a pH-metria ou pH-impedanciometria para a confirmação diagnóstica antes de qualquer conduta cirúrgica invasiva.
5. Semiologia do Estômago e Duodeno: A Dor e o “Dia Gástrico”
O raciocínio clínico na úlcera péptica é guiado pela ritmicidade da dor epigástrica em queimação ou “dor de fome”. Observem a pontualidade do “Dia Gástrico”, onde a sequência “dói, come, passa” ocorre em horários clássicos: 10:00h, entre 15:00h e 17:00h, e o despertar noturno entre 01:00h e 03:00h (clocking).
Manobras e Sinais de Alarme
Se o paciente apresenta anorexia, emagrecimento, hematêmese ou história familiar de neoplasia, a investigação deve ser imediata. Ao exame físico do abdome, o cirurgião deve buscar sinais de complicações:
- Rigidez Abdominal (Abdome em Tábua): Indica perfuração com peritonite.
- Sacolejo Gástrico: Realizado movimentando-se lateralmente o abdome do paciente em jejum (>6h) com o ouvido próximo à parede abdominal. A percepção de ruídos hidroaéreos de líquido retido é um sinal inequívoco de obstrução pilórica.
- Peristaltismo Visível: Ondas contráteis na parede abdominal que tentam vencer um obstáculo mecânico distal.
6. O Papel do Helicobacter pylori e Métodos de Diagnóstico
No Brasil, a prevalência do H. pylori na população adulta atinge 65%. Trata-se de um bacilo Gram-negativo classificado pela OMS como Carcinógeno do Grupo I por sua correlação direta com o adenocarcinoma gástrico e o linfoma MALT.
Propedêutica para H. pylori:
- Teste da Urease: Baseia-se na produção da enzima pela bactéria. Atenção: Exige alta densidade bacteriana (10^5 microrganismos) e pode sofrer interferência de hemorragia digestiva ativa, resultando em falsos-negativos.
- Histologia: Permite a visualização direta da bactéria em forma de “S” ou vírgula.
- Teste Respiratório (^{13}C): O padrão-ouro não invasivo para diagnóstico e controle de cura.
- Sorologia (ELISA): Útil em estudos epidemiológicos, mas não distingue infecção ativa de passada.
7. Semiologia do Intestino Delgado e Síndromes de Má Absorção
O intestino delgado é um órgão de adaptação fascinante, medindo de 3,5 a 4 metros in vivo. Sua arquitetura maximiza a absorção através de quatro mecanismos: comprimento tubular, pregas de Kerkring (válvulas coniventes), vilosidades e as microvilosidades (bordadura em escova). Manifestações sistêmicas são fundamentais no diagnóstico diferencial. A presença de artrite ou artralgia associada à diarreia crônica deve nos remeter imediatamente à Doença de Crohn ou à Doença de Whipple. Além disso, o cirurgião deve investigar se processos infecciosos prévios, como tuberculose ou paracoccidioidomicose ganglionar, deixaram sequelas como a linfangiectasia secundária, culminando em perda entérica proteica e má absorção.
8. Conclusão
A semiologia cirúrgica é a base para a solicitação ética e racional de exames como endoscopia, ecoendoscopia e manometria. Dominar a arte do diagnóstico clínico é o que diferencia o verdadeiro cirurgião de um técnico operatório. A precisão diagnóstica nasce da escuta atenta e da observação rigorosa.
——————————————————————————–
“O cirurgião deve ter olhos de águia, coração de leão e mãos de fada.” — Sir John Erichsen
Gostou ❔ Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Semiologia do Abdome Agudo
A Arte do Diagnóstico Clínico na Era da Tecnologia
Caros acadêmicos e colegas cirurgiões, é com o rigor que a ciência exige e o acolhimento que a medicina impõe que iniciamos esta reflexão. No cenário frenético das emergências brasileiras, a dor abdominal não é apenas uma queixa; é um enigma que responde por 5% a 10% de todas as admissões. Embora vivamos a era da imagem (radiologia), é imperativo recordar que, se 30% dos casos desafiam o diagnóstico inicial, 70% são plenamente resolvíveis apenas com as mãos, os olhos e a percepção clínica. Negligenciar a semiologia em prol da tecnologia não é apenas um erro metodológico; é um risco à vida, dada a morbi-mortalidade associada a diagnósticos tardios.
1. A Fisiopatologia da Dor: O Alerta da Lesão Tecidual
Para compreendermos o abdome agudo, devemos interpretar a dor sob a ótica da quebra da homeostase. Observem bem o raciocínio: a dor é um mecanismo de proteção. Quando um estímulo nocivo atinge o organismo, ele ativa nociceptores localizados no mesentério, nas superfícies peritoneais e na mucosa das vísceras. O ponto fundamental aqui é a dualidade do fenômeno. Existe o componente sensorial discriminativo, que nos permite aferir intensidade e localização, e o componente emocional/afetivo, processado pelo sistema límbico. Por que o exame físico deve começar com um aperto de mão e a palpação do pulso? Não apenas para checar a perfusão, mas para o acolhimento. Ao acolher o emocional do paciente, o cirurgião “limpa” o sinal neural, permitindo que o componente sensorial surja com clareza para a anamnese.
Se analisarmos o Homúnculo de Penfield, notaremos que a representação cortical das vísceras é minúscula se comparada à pele. Vejam a lógica: se a representação no córtex é reduzida, o cérebro tem dificuldade em localizar o sinal. É por essa razão fisiopatológica que a dor visceral é vaga e mal definida, enquanto a dor parietal, vastamente representada no homúnculo, é precisa e cortante.
2. A Trindade da Dor: Visceral, Parietal e Referida
A diferenciação dos padrões de dor é o que separa o diagnóstico brilhante da confusão clínica.
- Dor Visceral: Conduzida por Fibras C (lentas), é a dor da distensão ou torção. Como a inervação visceral é tipicamente bilateral e sua origem é embrionária, ela se manifesta na linha média. O Ligamento de Treitz é o nosso marco: dores do intestino anterior (estômago, duodeno, sistema hepatobiliar) surgem no epigástrio; do intestino médio (do Treitz à flexura hepática, incluindo o apêndice) na região periumbilical; e do intestino posterior no hipogástrio.
- Dor Parietal (Somática): Decorre da irritação do peritônio parietal por processos inflamatórios ou químicos (sangue, pus, bile). Diferente da visceral, é conduzida por fibras aferentes somáticas, sendo bem localizada e indicando, quase invariavelmente, gravidade e potencial cirúrgico.
- Dor Referida: Um fenômeno de convergência medular. As fibras aferentes da víscera e as somáticas da pele entram no corno posterior da medula no mesmo nível. O cérebro, confuso, projeta a dor em uma área distante da origem. Recordem-se do Sinal de Kehr (dor no ombro por irritação diafragmática).
Nota de mestre: Considerem a pelve como uma “Muralha Óssea”. Por ser uma estrutura de difícil palpação, a dor referida é, muitas vezes, o único sinal de alerta para patologias pélvicas graves. Nestes casos, o toque retal e vaginal são as únicas janelas para transpor essa muralha.
3. O Método Osleriano e o Exame Físico
Sir William Osler ensinava: “Cultive o seu poder de observação”. O exame não começa na palpação, mas na fácies de dor, na posição antálgica e na sudorese. O paciente com peritonite está imóvel; o que tem cólica, agita-se. O toque médico deve ser o primeiro ato de tratamento. Ao palpar o pulso e sentir uma taquicardia ou um pulso fino, você já está diagnosticando o choque autonômico antes mesmo de olhar o monitor. O acolhimento reduz a agitação, permitindo que você identifique a defesa abdominal (arco reflexo involuntário) ou a irritação peritoneal (percepção cerebral de dor à descompressão).
4. Diagnóstico Sindrômico: O Norte da Conduta
Antes de buscarmos a etiologia exata, devemos classificar o paciente em um dos cinco grandes grupos:
- Inflamatório: Dor insidiosa que se localiza com o tempo (Ex: Apendicite).
- Perfurativo: Dor súbita, em “facada”, com irritação peritoneal franca. Atenção: processos químicos podem ser lentos se bloqueados pelo mesentério.
- Obstrutivo: Dor em cólica, distensão e parada de eliminação de flatos e fezes.
- Vascular (Isquêmico): Caracteriza-se por uma dor desproporcional ao exame físico. Comum em idosos com comorbidades cardiovasculares.
- Hemorrágico: Dor associada a sinais inequívocos de hipovolemia.
5. Armadilhas e o Triunfo da Clínica
Devemos ter vigilância extrema com os “Pacientes de Alto Risco”: idosos, imunodeprimidos, gestantes e, sobretudo, o paciente que retorna. Qualquer indivíduo que volta à unidade com a mesma queixa é, por definição, de altíssimo risco. Lembrem-se: os exames são complementares. A “rotina de abdome agudo” solicitada sem critério é uma muleta para quem não soube examinar. Como dizemos na cirurgia: “Ausência de evidência não é evidência de ausência.”
6. A Regra de Ouro
O diagnóstico de um abdome agudo deve ser um filme, não uma fotografia. Se o diagnóstico não estiver claro, a observação seriada é o caminho. O prontuário deve ser o registro fiel desse cuidado, contendo a história de vida daquela dor. Encerro com a máxima de Sir Zachary Cope, que deve ecoar em cada plantão:
“Qualquer dor abdominal que perdure por mais de 6 horas em paciente previamente saudável é de importância cirúrgica até prova em contrário.”
O diagnóstico precoce é o que define a fronteira entre a vida e o óbito. Honrem a semiologia.
Gostou ❔ Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e/ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Extra | Epônimos Semiológicos Abdominais
A
- Sinal de Aaron
Dor ou sensação de desconforto no epigástrio/precordial provocada por pressão contínua no ponto de McBurney; classicamente ligado à apendicite.
Descrito por: Charles Dettie Aaron — norte-americano — 1913. - Sinal de Alders
Na dor parietal/aderencial, o ponto doloroso tende a permanecer fixo quando a paciente muda de posição; útil no diferencial de dor abdominal na gestação.
Descrito por: Nicholas Alders — húngaro de origem, naturalizado britânico — 1951.
B
- Sinal de Ballance
Macicez fixa no flanco esquerdo e macicez móvel no flanco direito; sugere ruptura esplênica com hemoperitônio.
Descrito por: Charles Alfred Ballance — britânico/inglês — 1898. - Sinal de Bassler
Dor à compressão do ponto apendicular por trás da linha médio-axilar; descrito em contexto de apendicite crônica.
Descrito por: Anthony Bassler — norte-americano — 1913. - Sinal de Bastedo
Dor em FID desencadeada por insuflação do cólon; empregado na investigação de apendicite.
Descrito por: Walter Bastedo — canadense radicado nos EUA / canadense-americano — 1910. - Sinal de Blumberg
Dor à descompressão brusca; indica irritação peritoneal.
Descrito por: Jacob Moritz Blumberg — alemão — 1907. - Sinal de Boas
Hiperestesia subescapular direita; clássico em colecistite aguda.
Descrito por: Ismar Isidor Boas — alemão — 1894. - Sinal de Bryant
Equimose azulada escrotal por rastreamento de sangue retroperitoneal/hemoperitônio.
Descrito por: John Henry Bryant — britânico/inglês — 1903. - Sinal de Bryan
Dor em FID à tração do útero ou da vagina em gestante; descrito em apendicite na gravidez.
Descrito por: R. Bryan — norte-americano — 1955.
C
- Sinal de Carnett
A dor piora ou não se altera com contração da parede abdominal, favorecendo origem na parede abdominal.
Descrito por: John Berton Carnett — norte-americano — 1926. - Sinal de Chutro
Desvio umbilical para a direita por contratura antálgica; descrito em apendicite aguda.
Descrito por: Pedro Chutro — argentino — 1912. - Sinal do obturador de Cope
Dor hipogástrica/FID com rotação interna da coxa fletida, sugerindo apêndice pélvico inflamado.
Descrito por: Zachary Cope — britânico/inglês — 1919. - Sinal do psoas de Cope
Dor à extensão passiva da coxa direita, associada a apendicite retrocecal.
Descrito por: Zachary Cope — britânico/inglês — 1921. - Sinal de Courvoisier–Terrier
Vesícula biliar palpável, aumentada e indolor em paciente ictérico; sugere obstrução biliar maligna mais que litíase crônica.
Descrito por: Ludwig Georg Courvoisier — suíço — 1890; antecedente histórico associado a Louis-Félix Terrier — francês — 1889. - Sinal de Cullen
Equimose periumbilical, típica de hemorragia intra/retroperitoneal, incluindo pancreatite hemorrágica e gravidez ectópica rota.
Descrito por: Thomas Stephen Cullen — canadense — 1918.
D
- Sinal de Dance
“Vazio” à palpação na fossa ilíaca direita; clássico em intussuscepção.
Descrito por: Jean-Baptiste Hippolyte Dance — francês — 1826. - Sinal de Danforth
Dor no ombro à inspiração por irritação diafragmática; associado a hemoperitônio, especialmente em gravidez ectópica rota.
Descrito por: William C. Danforth — norte-americano — década de 1920. - Sinal de Dunphy
A tosse exacerba a dor abdominal, sugerindo irritação peritoneal localizada.
Descrito por: geralmente atribuído a John Englebert Dunphy — norte-americano — 1953; a atribuição histórica não é totalmente uniforme nas fontes secundárias.
F
- Sinal de Fothergill
Massa da parede abdominal que permanece palpável com contração do reto e não cruza a linha média; típico de hematoma da bainha do reto.
Descrito por: William Edward Fothergill — britânico/inglês — 1926. - Sinal de Fox
Equimose abaixo do ligamento inguinal; indica hemorragia retroperitoneal.
Descrito por: John Adrian Fox — britânico/inglês — 1966.
G
- Sinal de Grey Turner
Equimose em flancos, típica de hemorragia retroperitoneal, sobretudo na pancreatite hemorrágica.
Descrito por: George Grey Turner — britânico/inglês — descrito em 1919 e publicado em 1920.
H
- Sinal de Howship–Romberg
Dor irradiada para a face medial da coxa por compressão do nervo obturatório; clássico de hérnia obturatória.
Descrito por: John Howship — britânico/inglês — 1840; complementado por Moritz Heinrich Romberg — alemão — 1847/1848.
J
- Sinal de Jobert
Desaparecimento da macicez hepática à percussão, sugerindo pneumoperitônio.
Descrito por: Antoine Joseph Jobert de Lamballe — francês — tradicionalmente atribuído à década de 1830; a data primária exata não ficou inequívoca nas fontes abertas consultadas.
K
- Sinal de Kehr
Dor referida no ombro esquerdo por irritação diafragmática, típica de ruptura esplênica ou hemoperitônio.
Descrito por: Hans Kehr — alemão — epônimo consolidado entre o fim do século XIX e início do XX.
L
- Sinal de Lapinsky
Dor em FID agravada por compressão local enquanto o paciente eleva o membro inferior direito estendido; associado à apendicite retrocecal.
Descrito por: Michael Lapinsky — russo — tradicionalmente situado no fim do século XIX; a data exata não foi confirmada com segurança nas fontes abertas consultadas. - Sinal de Lennander
Diferença entre temperatura retal e axilar, usada historicamente em processos inflamatórios abdominais, incluindo apendicite.
Descrito por: Karl Gustaf Lennander — sueco — fim do século XIX. - Sinal de Lockwood
Sensação de gorgolejo ou “borbulhamento” à palpação na FID em apendicite.
Descrito por: Charles Barrett Lockwood — britânico/inglês — epônimo difundido em publicação de 1932, baseada em seu ensino clínico prévio.
M
- Sinal de Mallet-Guy
Dor profunda no hipocôndrio esquerdo/ângulo costovertebral esquerdo, associada à pancreatite crônica.
Descrito por: Pierre Mallet-Guy — francês — 1943. - Sinal de Markle
Dor provocada pela queda sobre os calcanhares (“heel drop test”), sugerindo irritação peritoneal.
Descrito por: George B. Markle IV — norte-americano — 1973. - Sinal de Mayo-Robson
Dor à palpação no ângulo costovertebral esquerdo/“ponto de Mayo-Robson”, associado a doença pancreática.
Descrito por: Arthur William Mayo-Robson — britânico/inglês — início do século XX. - Sinal de McBurney
Dor máxima no ponto de McBurney, típica de apendicite aguda.
Descrito por: Charles Heber McBurney — norte-americano — 1889. - Sinal de Moynihan
Dor/hipersensibilidade no ponto cístico ou sob o rebordo costal direito, em contexto de colecistite.
Descrito por: Berkeley George Andrew Moynihan — britânico/inglês — 1905. - Sinal de Murphy
Interrupção inspiratória por dor à palpação do ponto cístico; clássico em colecistite aguda.
Descrito por: John Benjamin Murphy — norte-americano — 1903.
P
- Sinal de Perman
Dor em FID desencadeada por manobras compressivas à esquerda; historicamente, antecipa o que depois se difundiu como “Rovsing”.
Descrito por: Emil Samuel Perman — sueco — 1904.
R
- Sinal de Rovsing
Hoje descrito como dor em FID à palpação/compressão do lado esquerdo; usado no diagnóstico de apendicite aguda, embora a descrição original de 1907 fosse mecanicamente mais específica.
Descrito por: Niels Thorkild Rovsing — dinamarquês — 1907. - Sinal de Rosenstein / Sitkovskiy
Dor em FID ao decúbito lateral esquerdo; clássico em apendicite.
Descrito por: Piotr Porfiryevich Sitkovskiy — russo — 1922; associação histórica com Paul Rosenstein — alemão.
S
- Triângulo de Sherren
Área triangular de hiperestesia cutânea na FID, descrita na apendicite aguda.
Descrito por: James Sherren — britânico — 1903.
T
- Sinal de Torres Homem
Dor intensa à percussão digital na projeção hepática; classicamente associado a abscesso hepático.
Descrito por: João Vicente Torres Homem — brasileiro — século XIX; a data primária exata não foi localizada de forma confiável nas fontes abertas consultadas.
V
- Sinal de Volkovich–Kocher
Migração da dor do epigástrio/periumbilical para a FID, típica da apendicite aguda.
Descrito por: Nikolay Markianovich Volkovich — ucraniano — epônimo consolidado no início do século XX; frequentemente associado também à tradição clínica de Theodor Kocher — suíço. - Sinal de Voskresensky
Dor em FID durante deslizamento rápido da mão sobre a parede abdominal (“sinal da camisa”); descrito em apendicite.
Descrito por: Vladimir Mikhailovich Voskresensky — russo — 1940.