A Dualidade da Humanização Cirúrgica
Era da Inteligência Artificial e da Robótica: Desafios e Perspectivas
Por Prof. Dr. Ozimo Gama
Coordenador do Curso de Medicina da Universidade Federal do Maranhão
O Cenário Atual e a Necessidade do “Toque Humano”
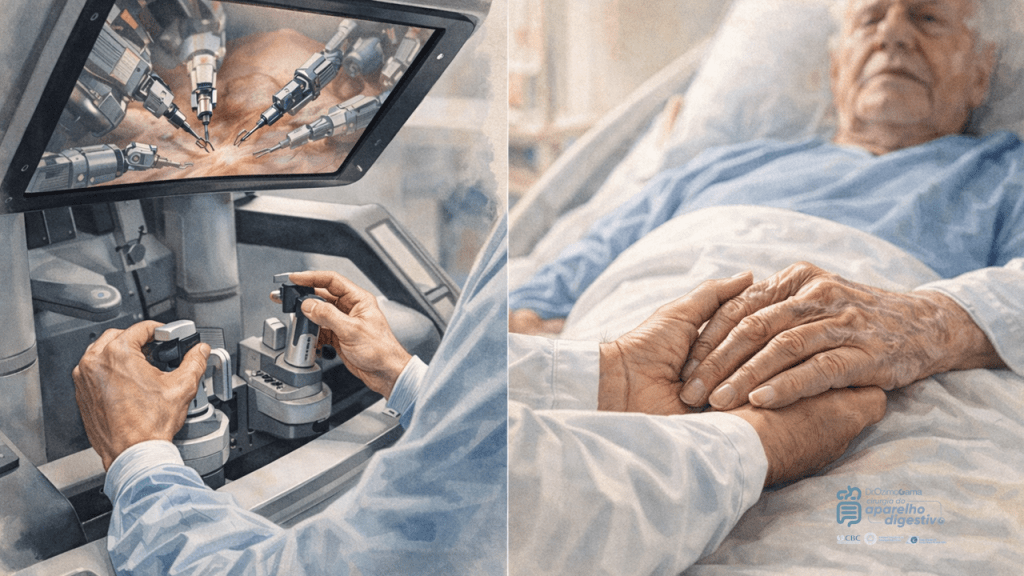
A prática da cirurgia do aparelho digestivo vive um momento de paradoxo fascinante. Por um lado, testemunhamos avanços tecnológicos sem precedentes, com a cirurgia robótica e a inteligência artificial (IA) redefinindo os limites do possível. Por outro, enfrentamos uma crise silenciosa na relação médico-paciente. No Brasil, segundo dados do DATASUS e do Conselho Federal de Medicina, realizamos milhões de procedimentos cirúrgicos anuais pelo Sistema Único de Saúde (SUS), onde a alta demanda muitas vezes colide com a necessidade de um atendimento individualizado.
A “humanização” não é apenas um conceito abstrato ou uma “soft skill” desejável; é um imperativo clínico. Estudos epidemiológicos demonstram que pacientes que estabelecem uma relação de confiança sólida com seus cirurgiões apresentam melhor adesão ao tratamento pós-operatório, menores índices de litígios médicos e, subjetivamente, uma percepção de dor reduzida.
O desafio contemporâneo, como bem alertava o Prof. Alcino Lázaro da Silva, é evitar que o “fascínio das máquinas e dos botões” transforme o jovem cirurgião em um “sectário ou robô”. Precisamos integrar a tecnologia sem permitir que ela congele nossos sentimentos ou desqualifique a essência da nossa profissão: o cuidado com o ser humano.
Tecnologia, Ontoética e Controvérsias
A Inteligência Artificial e a Despersonalização
A IA chegou para auxiliar na tomada de decisão, predizendo complicações e otimizando fluxos em centros cirúrgicos. No entanto, existe o risco real da “atrofia da empatia”. Quando confiamos excessivamente em algoritmos para o prognóstico, corremos o risco de tratar o paciente como um conjunto de dados biométricos, e não como uma biografia. A tecnologia deve ser uma ferramenta de meio, nunca de fim. O cirurgião que se esconde atrás da tela do computador perde a oportunidade de exercer a “Ontoética” — a ética do ser, o respeito intrínseco à vida humana que transcende a técnica.
Aspectos Médico-Legais e o Consentimento
A humanização tem implicações jurídicas diretas. O Prof. Milton Glezer destaca que o paciente tem o direito de recusar tratamento (salvo risco iminente de morte) e de ter acesso irrestrito ao seu prontuário. No Brasil, a judicialização da medicina tem crescido exponencialmente. Uma parte significativa desses processos não decorre de erro técnico (imperícia), mas de falha na comunicação. O Consentimento Livre e Esclarecido não deve ser apenas um formulário burocrático assinado na admissão. Ele deve ser um processo contínuo de diálogo, onde o cirurgião traduz o “tecniquês” para a realidade do doente, respeitando sua autonomia e dignidade.
Controvérsias Filosóficas
A controvérsia reside na formação médica atual. Os currículos de graduação e residência muitas vezes privilegiam a técnica em detrimento da humanística. Criamos excelentes técnicos capazes de realizar gastrectomias complexas, mas que, por vezes, falham em comunicar um diagnóstico de câncer gástrico com a compaixão necessária. A escola médica deve ensinar que o doente prefere, acima do tecnocrata, o amigo; acima do executor de procedimentos, o médico que orienta e acolhe.
Aplicação Prática na Cirurgia do Aparelho Digestivo
Na nossa especialidade, a humanização possui facetas muito específicas e impactantes:
- Ostomias e Imagem Corporal: Ao indicar uma colostomia definitiva, por exemplo, o cirurgião digestivo não está apenas alterando a anatomia, mas a autoimagem e a vida social do paciente. A abordagem humanizada exige preparar este paciente psicologicamente, envolvendo a equipe multidisciplinar e a família antes mesmo do ato cirúrgico.
- Oncologia Cirúrgica: O diagnóstico de neoplasias do trato gastrointestinal carrega um estigma de mortalidade. A forma como a notícia é dada (protocolo SPIKES, por exemplo) é tão crucial quanto a linfadenectomia realizada.
- Cirurgia Bariátrica: O paciente obeso muitas vezes carrega anos de preconceito, inclusive dentro do sistema de saúde. A humanização aqui significa enxergar a obesidade como doença crônica, despindo-se de julgamentos morais e oferecendo um suporte que vai além da perda de peso.
Pontos-Chave para a Prática Diária
Para o residente e o jovem cirurgião, a humanização se traduz em atos concretos:
- Olho no Olho: A tecnologia (computadores, tablets) não deve ser uma barreira física durante a consulta. Sente-se, olhe para o paciente e escute ativamente antes de examinar.
- Identificação Clara: Como preconizado nas diretrizes hospitalares, apresente-se, diga sua função e certifique-se de que o paciente sabe quem é o responsável pelo seu tratamento (titularidade médica).
- Gestão da Expectativa: Explique riscos e benefícios reais. A frustração do paciente muitas vezes nasce de uma expectativa irrealista não corrigida pelo cirurgião no pré-operatório.
- O “Não” Terapêutico: Saber a hora de não operar (obstinação terapêutica) em casos de carcinomatose ou doenças terminais é, talvez, a maior prova de humanidade e ética cirúrgica.
Perspectivas Futuras
O futuro da Cirurgia do Aparelho Digestivo não será definido apenas pela precisão dos robôs ou pela acurácia dos algoritmos de IA, mas pela nossa capacidade de manter a essência humana em um ambiente cada vez mais digital. A “Ontoética” deve guiar nossas mãos tanto quanto a anatomia.
Precisamos formar cirurgiões “híbridos”: exímios operadores da tecnologia, mas profundos conhecedores da alma humana. Como discutido nos textos bases, o hospital deve buscar trazer esperança, e o médico deve lembrar que, ao tratar um doente, está lidando com uma unidade indivisível de medos, histórias e sentimentos. A tecnologia passa, a máquina obsoleta é trocada, mas o impacto de um atendimento humano perdura na memória do paciente e de seus familiares.
#CirurgiaDigestiva #HumanizaçãoMédica #Bioética #EducaçãoMédica #OncologiaCirurgica
“O único meio de combater a praga da impessoalidade e da frieza na medicina moderna é cultivar as humanidades no médico, pois o segredo do cuidado com o paciente é importar-se com o paciente.” — Adaptado de Francis Peabody (embora clínico, sua máxima é a pedra angular para a humanização cirúrgica moderna).
Gostou? ❔ Nos deixe um comentário ✍️, compartilhe em suas redes sociais e/ou mande sua dúvida pelo 💬 Chat Online em nossa DM do Instagram.
Princípios Fundamentais da Oncologia Cirúrgica Digestiva
Uma Abordagem Contemporânea e Baseada em Evidências
O Cenário Atual do Câncer Digestivo no Brasil
A Cirurgia do Aparelho Digestivo vive um momento de transformação sem precedentes. Não somos mais apenas “técnicos de ressecção”, mas parte integrante de uma complexa engrenagem multidisciplinar. A relevância deste tema é sublinhada pelos dados epidemiológicos alarmantes. Se no passado nos baseávamos em estimativas modestas, hoje a realidade é desafiadora: segundo a Estimativa 2023-2025 do Instituto Nacional de Câncer (INCA), esperam-se 704 mil casos novos de câncer por ano no Brasil.
Destaque-se que as neoplasias do trato gastrointestinal ocupam posições cimeiras. O câncer colorretal figura como o segundo mais incidente em mulheres e homens na maioria das regiões, com cerca de 45 mil novos casos anuais, seguido de perto pelo câncer de estômago (21 mil casos) e esôfago. Estes números não são apenas estatísticas; representam uma demanda crescente por cirurgiões oncológicos altamente qualificados, capazes de compreender não apenas a anatomia, mas a biologia tumoral.
A Biologia como Norte da Técnica Cirúrgica
Fisiopatologia e Disseminação
O entendimento clássico da cirurgia oncológica, herdado dos princípios de William Halsted no final do século XIX, baseava-se na premissa de que o câncer era uma doença puramente local que se disseminava centrifugamente. Embora a radicalidade (ressecção em bloco) permaneça um pilar, hoje compreendemos a doença como sistêmica desde fases precoces em muitos casos.
A disseminação ocorre por três vias principais que o cirurgião deve dominar:
- Linfática: Predominante em carcinomas (ex: adenocarcinoma gástrico e cólon).
- Hematogênica: Preferencial em sarcomas e carcinomas avançados (fígado e pulmões como sítios-alvo).
- Transcelômica (Peritoneal): Comum em neoplasias gástricas T3/T4, ovário e apêndice, exigindo estratégias específicas como a peritoniectomia.
O Princípio da Radicalidade e Margens (R0)
O objetivo primário da cirurgia oncológica curativa é a ressecção R0 (ausência de doença residual macroscópica e microscópica). A cirurgia R1 (doença microscópica residual) ou R2 (macroscópica) impacta drasticamente o prognóstico.
- Ressecção em Bloco: O tumor nunca deve ser violado. A peça deve ser removida envolta por tecido saudável, respeitando as fáscias anatômicas e os pedículos vasculares na sua origem.
- Linfadenectomia: Não serve apenas para estadiamento, mas tem papel terapêutico. No câncer gástrico, por exemplo, a linfadenectomia D2 é o padrão-ouro em centros especializados, associada a menor recidiva locorregional.
Neoadjuvância vs. Adjuvância
A decisão entre operar primeiro (upfront surgery) ou indicar terapia neoadjuvante é um dos grandes debates atuais.
- Vantagens da Neoadjuvância: Tratamento precoce de micrometástases, redução do tumor (downstaging) facilitando a ressecção R0 e teste in vivo da quimiossensibilidade. É o padrão atual para câncer de esôfago localmente avançado e câncer de reto médio/baixo.
- Vantagens da Adjuvância: Baseada no estadiamento patológico preciso (pTNM), evitando tratamento excessivo em estádios precoces.
Aplicação Prática na Cirurgia Digestiva
A prática moderna exige que o cirurgião diferencie dois conceitos cruciais frequentemente confundidos: Ressecabilidade e Operabilidade.
- Ressecabilidade: É uma característica do tumor (relação com estruturas vitais).
- Operabilidade: É uma característica do paciente (reserva funcional, comorbidades, status performance). Um tumor pode ser ressecável, mas o paciente inoperável.
O Papel da Citorredução e HIPEC
Para a carcinomatose peritoneal, historicamente considerada uma condição terminal, houve uma mudança de paradigma. Em neoplasias selecionadas (como pseudomixoma peritoneal, mesotelioma e alguns casos de câncer colorretal), a combinação de Cirurgia de Citorredução (Peritoniectomia) com Quimioterapia Intraperitoneal Hipertérmica (HIPEC) tem oferecido sobrevida em longo prazo, transformando uma doença fatal em uma condição crônica tratável.
Planejamento Multidisciplinar
O cirurgião oncológico não atua isolado. A discussão em Tumor Boards é mandatória. A indicação cirúrgica deve considerar a biologia molecular (ex: status do gene APC em colorretal, superexpressão de HER2 em gástrico) e a resposta a terapias sistêmicas.
Pontos-Chave para a Prática Cirúrgica
- Estadiamento Preciso: Nunca leve um paciente à sala sem um estadiamento completo. A laparoscopia diagnóstica é fundamental em tumores gástricos e pancreáticos para evitar laparotomias desnecessárias em casos de carcinomatose oculta.
- Margens Cirúrgicas: A margem circunferencial (radial) no câncer de reto e a margem proximal no câncer gástrico e esofágico são preditores independentes de sobrevida.
- Manuseio da Peça (“No-touch technique”): Evite a manipulação direta do tumor. A ligadura vascular prévia e a mobilização cuidadosa previnem a embolização tumoral intraoperatória.
- Documentação: O relatório cirúrgico deve detalhar as cadeias linfáticas dissecadas e as estruturas preservadas ou ressecadas, orientando o patologista e o oncologista clínico.
Perspectivas Futuras
A cirurgia digestiva na sua área de atuação oncológica evoluiu de amputações extensas para procedimentos de precisão, muitas vezes minimamente invasivos (laparoscópicos ou robóticos), sem perder a radicalidade oncológica. O futuro aponta para uma integração ainda maior com a biologia molecular e a imunoterapia. O cirurgião do futuro deverá ser, antes de tudo, um oncologista que opera: alguém que entende que o bisturi é apenas uma das armas, e que saber quando não operar é tão vital quanto a técnica operatória refinada.
Como nos ensinou o pai da cirurgia oncológica moderna:
“O cirurgião deve ser o médico do paciente oncológico, e não apenas o técnico que remove o tumor.” — William Stewart Halsted
Hashtags
#CirurgiaDigestiva #OncologiaCirurgica #EducaçãoMédica #ResidenciaCirurgia #CancerDigestivo
Gostou? ❔ Nos deixe um comentário ✍️, compartilhe em suas redes sociais e/ou mande sua dúvida pelo 💬 Chat Online em nossa DM do Instagram.
Efeito Cascata do Transplante Hepático
Introdução
O transplante hepático é universalmente reconhecido como o “padrão-ouro” para o tratamento de doenças hepáticas terminais. No entanto, o impacto deste procedimento transcende a substituição de um órgão doente. O sucesso fenomenal do transplante nas últimas cinco décadas produziu o que chamamos de ripple effect (efeito cascata) sobre toda a cirurgia geral e, especificamente, sobre a cirurgia hepatobiliar. Muitos dos princípios anatômicos, refinamentos técnicos e bases científicas que hoje aplicamos rotineiramente em hepatectomias regradas e cirurgias de trauma foram desenvolvidos ou aperfeiçoados nas salas de transplante. O objetivo desta exposição é dissecar como essa “escola” transformou a nossa prática diária, convertendo procedimentos outrora considerados de risco proibitivo em operações seguras e eficazes.
Desenvolvimento: Anatomia e Fisiologia Aplicadas
A base de qualquer cirurgia hepática segura é o domínio absoluto da anatomia e da fisiologia. O transplante nos forçou a olhar para o fígado não apenas como uma massa parenquimatosa, mas como uma estrutura segmentar com variações vasculares frequentes.
1. O Novo Mapa Anatômico
A experiência com doadores vivos e hepatectomias em cadáveres nos ensinou que a anatomia “de livro” é a exceção, não a regra.
- Variações Arteriais: Estudos clássicos de grandes centros transplantadores, como a série da UCLA, demonstram que aproximadamente 24% dos fígados possuem anomalias arteriais significativas. As mais comuns incluem a artéria hepática direita acessória ou substituída (originada da artéria mesentérica superior) e a esquerda (originada da artéria gástrica esquerda). O cirurgião que ignora essas variantes durante uma duodenopancreatectomia ou gastrectomia corre o risco de desvascularizar o fígado.
- Variações Biliares: A trifurcação do ducto hepático comum ocorre em cerca de 12% dos casos. O reconhecimento dessas nuances é vital para evitar estenoses e fístulas biliares, as complicações mais temidas no pós-operatório.
2. Regeneração e Isquemia
O transplante impulsionou a pesquisa sobre a capacidade regenerativa do fígado. O conceito de síndrome small-for-size (insuficiência hepática pós-resecção por remanescente pequeno) migrou do transplante intervivos para a oncologia. Hoje, calculamos com precisão o volume do fígado remanescente antes de grandes ressecções tumorais, utilizando estratégias como a embolização prévia da veia porta para hipertrofiar o lobo que ficará no paciente — uma aplicação direta do conhecimento de regeneração hepática. Além disso, o manuseio da lesão de isquemia-reperfusão evoluiu. Técnicas de precondicionamento isquêmico (clampeamento intermitente) permitem que realizemos ressecções complexas com menor perda sanguínea e menor dano hepatocelular.
Aplicação na Cirurgia Digestiva Geral e Oncológica
A transferência de tecnologia do transplante para a cirurgia digestiva geral é evidente em três pilares principais:
1. Ressecções Hepáticas Complexas e Preservação Caval
Antigamente, tumores no lobo caudado ou que envolviam a veia cava retro-hepática eram considerados irressecáveis. A técnica de “piggyback” (preservação da veia cava inferior do receptor durante o transplante) ensinou aos cirurgiões oncológicos como dissecar o fígado da veia cava com segurança, permitindo a ressecção de tumores centrais e posteriores com margens livres.
2. Controle Vascular no Trauma
O cirurgião de trauma moderno utiliza manobras de exclusão vascular total (clampeamento da porta e da veia cava supra e infra-hepática) para reparar lesões venosas complexas em fígados traumatizados. Esta é uma manobra derivada diretamente da hepatectomia do receptor no transplante. Em pacientes estáveis, isso permite reparos exangues; em instáveis, técnicas de damage control com shunts portocavais temporários podem ser salvadoras.
3. Cirurgia Ex Situ
Para casos extremos de tumores invadindo a confluência cavo-hepática, a técnica de hepatectomia total, seguida de perfusão fria do órgão na bancada (bench surgery), ressecção do tumor ex vivo e reimplante do fígado (autotransplante), é a fronteira final da cirurgia hepatobiliar, tornada possível apenas pelo domínio das técnicas de preservação de órgãos.
Cenário Brasileiro: Uma Potência Mundial 🇧🇷
É fundamental contextualizar nossa realidade. O Brasil possui o maior sistema público de transplantes do mundo.
- Segundo dados recentes da Associação Brasileira de Transplante de Órgãos (ABTO) e do Ministério da Saúde, o Brasil realiza mais de 2.000 transplantes hepáticos anualmente, posicionando-se consistentemente entre as três nações com maior número absoluto de procedimentos no mundo.
- Essa estatística não é apenas um número; ela representa um volume crítico de treinamento. Residentes brasileiros em centros de excelência têm uma exposição prática à anatomia hepática complexa superior à de muitos países desenvolvidos. O “Cirurgião SUS” é, por necessidade e oportunidade, um especialista em variações anatômicas e manuseio de situações complexas.
Pontos-Chave para o Cirurgião em Formação
- Identificação Pré-operatória: Sempre investigue variações arteriais (ex: artéria hepática direita vindo da mesentérica) em exames de imagem antes de qualquer cirurgia do andar supramesocólico.
- Manobras de Exclusão: Familiarize-se com a Manobra de Pringle e a exclusão vascular total; elas são suas ferramentas de segurança em sangramentos maciços.
- Dissecção Hilar: A técnica de baixar a placa hilar e dissecar as estruturas glissonianas extra-hepáticas é mais segura e oncológica do que a dissecção intraparenquimatosa cega.
- Interdisciplinaridade: A cirurgia moderna não é um ato solitário. Radiologia intervencionista, hepatologia e terapia intensiva são extensões do braço do cirurgião.
Conclusão
O transplante hepático não deve ser visto pelos estudantes e residentes apenas como uma subespecialidade de nicho, mas como a “Universidade da Cirurgia Abdominal”. As lições aprendidas com a preservação de órgãos, a dissecção meticulosa de vasos de calibre milimétrico e o manejo fisiológico do paciente hepatopata elevaram o padrão técnico de toda a cirurgia digestiva. Dominar esses conceitos é o que diferencia o operador técnico do verdadeiro cirurgião cientista.
“A história da medicina é que o que era inconcebível ontem, e apenas alcançável hoje, muitas vezes torna-se rotina amanhã.” — Thomas Starzl (Pioneiro do Transplante Hepático)
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags: #CirurgiaHepatobiliar #TransplanteHepatico #EducacaoMedica #ResidenciaCirurgia #CirurgiaDigestiva
A Importância da Competência em Endoscopia Flexível na Formação e Prática do Cirurgião do Aparelho Digestivo
Introdução
A endoscopia digestiva flexível transcende a sua definição clássica de método diagnóstico. Na contemporaneidade, ela se consolida como uma extensão essencial da propedêutica e da terapêutica cirúrgica. Historicamente, é imperativo recordar que a endoscopia é um campo desbravado por cirurgiões. Grandes marcos, como a polipectomia colônica (Dr. Hiromi Shinya), a ligadura elástica de varizes (Dr. Goffredo Steigman) e a gastrostomia percutânea (Dr. Jeffrey Ponsky), foram estabelecidos por mentes cirúrgicas que vislumbravam além da incisão convencional. No entanto, observa-se um fenômeno preocupante na formação médica atual: a delegação progressiva dessa competência quase exclusivamente à gastroenterologia clínica e aos Endoscopistas. Este artigo, direcionado a estudantes, residentes e pós-graduandos, visa reafirmar a premissa de que a habilidade endoscópica não é opcional, mas intrínseca à prática do cirurgião do aparelho digestivo de excelência. Discutiremos as bases técnicas, a aplicabilidade clínica e a necessidade premente de retomar o protagonismo nesta área.
Desenvolvimento: O Cirurgião e a Habilidade Endoscópica
A Curva de Aprendizado e a Visão Cirúrgica
A competência em endoscopia flexível depende da fusão entre conhecimento cognitivo e habilidade técnica (psicomotora). O cirurgião, habituado à manipulação tecidual e à anatomia tridimensional (seja por via aberta ou laparoscópica), possui, intrinsecamente, uma coordenação olho-mão refinada. Estudos demonstram que cirurgiões tendem a apresentar uma curva de aprendizado acelerada para procedimentos endoscópicos devido à sua familiaridade com a anatomia topográfica e patológica, permitindo uma transição fluida entre a visão bidimensional da tela e a realidade espacial do órgão.
O Cenário Brasileiro e a Demografia Médica
No contexto do Brasil, um país de dimensões continentais, a distribuição de especialistas é heterogênea. Segundo dados da Demografia Médica no Brasil (CFM/USP, 2023), a concentração de gastroenterologistas clínicos | endoscopistas é significativamente menor e mais centralizada em grandes capitais do que a de cirurgiões gerais. O cirurgião geral, muitas vezes, é o único provedor de saúde especializado em regiões remotas. Portanto, capacitar o cirurgião em endoscopia não é apenas uma questão de reserva de mercado, mas uma estratégia de saúde pública para garantir o rastreamento de neoplasias (como o câncer colorretal) e o atendimento de urgências (Hemorragia Digestiva Alta) em todo o território nacional.
Do “Cirurgião de Resgate” ao “Cirurgião Estrategista”
Tradicionalmente, o cirurgião é chamado apenas quando ocorre uma complicação endoscópica, como perfuração ou sangramento incontrolável. Este paradigma do “cirurgião de resgate” deve evoluir para o de “cirurgião estrategista”. Ao dominar a endoscopia, o profissional torna-se o capitão do navio terapêutico, capaz de indicar, executar e, se necessário, converter procedimentos com total autonomia e continuidade do cuidado (Continuity of Care), otimizando desfechos e minimizando a fragmentação do tratamento.
Aplicação na Cirurgia Digestiva
A integração da endoscopia na rotina cirúrgica pode ser categorizada em três momentos cruciais:
1. Endoscopia Pré-Operatória: O Planejamento
Na cirurgia oncológica gástrica e esofágica, a endoscopia realizada pelo próprio cirurgião permite uma avaliação precisa das margens tumorais, da extensão para a cárdia ou piloro, influenciando diretamente a decisão entre uma gastrectomia total ou subtotal. Na cirurgia bariátrica, a identificação prévia de hérnias hiatais, esofagites severas ou patologias gástricas altera o algoritmo de tratamento, contraindicando, por exemplo, uma gastrectomia vertical (Sleeve) em favor de um bypass gástrico em Y de Roux.
2. Endoscopia Intraoperatória: A Segurança
O uso transoperatório é uma ferramenta de segurança inestimável. Exemplos clássicos incluem:
- Cardiomiotomia de Heller: Confirmação da adequação da miotomia e teste de vazamento (air leak test) para exclusão de perfurações mucosas.
- Exploração de Vias Biliares: O uso do coledocoscópio flexível permite a visualização direta e a certeza da remoção completa de cálculos, superior à colangiografia em casos complexos.
- Localização de Lesões: Em cirurgias colorretais laparoscópicas, a tatuagem prévia pode ser imprecisa; a colonoscopia intraoperatória garante a ressecção do segmento correto.
3. Endoscopia Pós-Operatória e Manejo de Complicações
O cirurgião que realiza a endoscopia está melhor posicionado para tratar as complicações de seus próprios procedimentos ou de seus pares. O arsenal terapêutico inclui:
- Dilatação com balão de estenoses de anastomoses (gástricas ou colorretais).
- Tratamento de fístulas e deiscências pós-Sleeve ou Bypass com uso de próteses autoexpansíveis ou clips endoscópicos.
- Hemostasia de linhas de sutura sangrantes.
A Era da Cirurgia Sem Cicatrizes (NOTES e Endoterapia)
Caminhamos para a era da intervenção minimamente invasiva máxima. Procedimentos como o POEM (Peroral Endoscopic Myotomy) substituem a miotomia laparoscópica; o Endoscopic Sleeve Gastroplasty (ESG) surge como alternativa à cirurgia bariátrica convencional. O cirurgião do futuro deve dominar estas técnicas para oferecer o tratamento “estado da arte” aos seus pacientes.
Pontos-Chave para o Residente e o Cirurgião Jovem
- Necessidade de Treinamento: As sociedades cirúrgicas (como o CBC e a CBCD no Brasil) têm enfatizado a importância de currículos de residência que contemplem carga horária prática em endoscopia.
- Visão Integral: O domínio da luz luminal (endoscopia) e da cavidade peritoneal (laparoscopia/robótica) cria um cirurgião completo.
- Autonomia: A capacidade de diagnosticar, estadiar, tratar e resolver complicações sem depender de terceiros é o ápice da eficiência clínica.

Conclusão
A endoscopia flexível não é uma especialidade à parte, mas uma ferramenta cirúrgica, tal qual o bisturi ou a pinça laparoscópica. Para o cirurgião do aparelho digestivo, delegar essa competência é abdicar de uma parte fundamental da sua herança histórica e do seu futuro profissional. A formação médica deve encorajar a retomada deste espaço, garantindo que as novas gerações de cirurgiões sejam proficientes tanto na ciência da cirurgia quanto na arte da endoscopia. Como mentores e instituições de ensino, nosso dever é prover o acesso e a estrutura para que essa integração seja a norma, e não a exceção.
“Nenhum homem pode ser um grande cirurgião sem ser também um grande médico; e o inverso é igualmente verdadeiro no que tange ao diagnóstico e compreensão da fisiopatologia.” > — Adaptado de Theodor Billroth, pai da cirurgia gástrica moderna, refletindo a necessidade do conhecimento integral.
Gostou ❔Nos deixe um comentário ✍️ , compartilhe em suas redes sociais e|ou mande sua dúvida pelo 💬 Chat On-line em nossa DM do Instagram.
Hashtags: #CirurgiaDigestiva #EndoscopiaTerapeutica #ResidenciaMedica #CirurgiaGeral #EducacaoMedica
Epônimos da Anatomia Abdominal: A Linguagem Clássica da Prática Cirúrgica
Resumo Apesar dos esforços contínuos da Federative International Programme on Anatomical Terminologies (FIPAT) para padronizar a nomenclatura médica através da Terminologia Anatômica, a linguagem operatória permanece, em essência, histórica. Este artigo revisa os epônimos fundamentais da anatomia abdominal, correlacionando a definição topográfica precisa com a aplicação prática na cirurgia do aparelho digestivo, demonstrando que o domínio destes termos é imperativo para a segurança cirúrgica e a comunicação clínica eficaz.
Introdução
A anatomia topográfica é o alicerce da cirurgia. Contudo, existe uma dicotomia persistente entre a taxonomia descritiva moderna e a tradição oral dos centros cirúrgicos. Enquanto a academia privilegia termos locativos e funcionais, a prática diária — da passagem de plantão à descrição operatória — é dominada por epônimos. Estes nomes não são meros vestígios históricos; funcionam como “atalhos cognitivos” que evocam, simultaneamente, uma localização, uma relação anatômica complexa e, frequentemente, uma manobra cirúrgica específica. Este estudo revisa os principais epônimos do abdome, dissecando sua anatomia estrutural e sua relevância crítica na cirurgia geral e digestiva.
1. Parede Abdominal e Região Inguinal
A compreensão da estratigrafia da parede abdominal é o primeiro passo para o acesso seguro à cavidade peritoneal e para o reparo eficaz dos defeitos herniários.
Estratigrafia Subcutânea e Fascial
- Fáscia de Camper
- Anatomia: Camada superficial, de espessura variável e consistência adiposa, do tecido subcutâneo da parede abdominal anterior.
- Relevância Cirúrgica: A sua aproximação é frequentemente negligenciada, mas o manejo adequado do espaço morto nesta camada é vital na prevenção de seromas e infecções de sítio cirúrgico superficiais em laparotomias.
- Fáscia de Scarpa
- Anatomia: Camada membranosa profunda do tecido subcutâneo, contendo fibras elásticas amarelas, que se funde com a fáscia lata da coxa inferiormente e continua como Fáscia de Colles no períneo.
- Relevância Cirúrgica: Estrutura de fixação essencial no fechamento da parede abdominal. A sutura desta camada reduz a tensão sobre a pele e melhora o resultado estético da cicatriz. Devido à sua continuidade perineal, orienta a disseminação de extravasamentos de urina (fraturas de uretra) ou infecções necrotizantes (Síndrome de Fournier).
- Fáscia Inominada de Gallaudet
- Anatomia: A fáscia profunda aderida intimamente à aponeurose do músculo oblíquo externo e bainha do reto.
- Relevância Cirúrgica: Define o plano de dissecção “limpo” sobre a aponeurose durante o reparo de hérnias ou a confecção de retalhos miocutâneos.
Anatomia Inguinal e o Assoalho Pélvico
- Ligamento de Poupart (Ligamento Inguinal)
- Anatomia: A borda inferior espessa e recorvada da aponeurose do oblíquo externo, estendendo-se da Espinha Ilíaca Antero-Superior (EIAS) ao tubérculo púbico.
- Relevância Cirúrgica: O marco anatômico absoluto que diferencia hérnias inguinais (acima) de femorais (abaixo) e serve como âncora inferior para reparos teciduais clássicos (técnica de Bassini) e fixação de telas (técnica de Lichtenstein).
- Ligamento de Gimbernat (Ligamento Lacunar)
- Anatomia: Uma extensão triangular das fibras do ligamento inguinal que se reflete posteriormente e se insere na linha pectínea.
- Relevância Cirúrgica: Forma a borda medial do anel femoral. Em casos de hérnia femoral encarcerada, este ligamento é frequentemente a estrutura constritora que deve ser incisada (com cautela devido à presença eventual da Corona Mortis vascular) para redução do conteúdo.
- Ligamento de Cooper (Ligamento Pectíneo)
- Anatomia: Espessamento do periósteo e fáscia ao longo da crista pectínea (pecten do púbis), posterior ao ligamento inguinal.
- Relevância Cirúrgica: Estrutura de ancoragem robusta utilizada na técnica de McVay e ponto de fixação crítico para telas em reparos laparoscópicos (TAPP/TEP), prevenindo a recidiva direta.
- Triângulo de Hesselbach
- Anatomia: Delimitado inferiormente pelo ligamento inguinal, lateralmente pelos vasos epigástricos inferiores e medialmente pela borda lateral do músculo reto abdominal.
- Relevância Cirúrgica: Local anatômico das hérnias inguinais diretas, resultantes da fraqueza da fáscia transversal, sem passagem pelo anel inguinal profundo.
- Orifício Miopectíneo de Fruchaud
- Anatomia: Área de fraqueza da parede abdominal inferior que engloba tanto a região inguinal quanto a femoral, delimitada pelo músculo oblíquo interno (superior), reto abdominal (medial), iliopsoas (lateral) e osso púbico (inferior).
- Relevância Cirúrgica: Conceito fundamental para a cirurgia moderna de hérnia. Estabelece que o tratamento definitivo deve cobrir toda esta área com material protético (tela) para prevenir todos os tipos de hérnias da virilha, princípio base das abordagens pré-peritoneais (Stoppa, TEP, TAPP).
2. Peritônio e Topografia Gastrointestinal
A semiologia abdominal e o acesso cirúrgico baseiam-se em projeções de superfície e recessos cavitários.
- Linha de Monro-Richter e Ponto de McBurney
- Anatomia: Linha traçada da EIAS à cicatriz umbilical. O Ponto de McBurney localiza-se na união do terço lateral com os dois terços mediais desta linha.
- Relevância Cirúrgica: Projeção clássica da base do apêndice cecal. Guia a incisão oblíqua (McBurney) para apendicectomias abertas e é o ponto de máxima dor à descompressão na apendicite aguda.
- Ponto de Lanz
- Anatomia: Ponto na junção do terço direito com o terço médio da linha bi-ilíaca.
- Relevância Cirúrgica: Representa a projeção variável do ápice de um apêndice pélvico longo, importante no diagnóstico diferencial de patologias anexiais em mulheres.
- Ponto de Murphy
- Anatomia: Ponto situado abaixo do rebordo costal direito, na linha hemiclavicular (borda lateral do reto abdominal).
- Relevância Cirúrgica: Local de palpação do fundo da vesícula biliar. A interrupção súbita da inspiração à palpação profunda (Sinal de Murphy) é altamente sugestiva de colecistite aguda.
- Espaços Peritoneais (Morison, Douglas, Proust, Winslow)
- Bolsa de Morison (Recesso Hepatorrenal): Espaço virtual entre o fígado e o rim direito. É o local mais dependente do abdome superior em decúbito dorsal; local primário de acúmulo de líquido livre (sangue/pus) detectável pelo FAST em trauma.
- Fundo de Saco de Douglas (Retouterino): Ponto mais declive da cavidade peritoneal em mulheres. Local de acúmulo de líquido e de implantes metastáticos palpáveis ao toque retal/vaginal (Prateleira de Blumer).
- Espaço de Proust (Retovesical): Correspondente masculino ao de Douglas, entre o reto e a bexiga/próstata. Relevante na dissecção oncológica do reto baixo.
- Forame de Winslow (Forame Epiploico): Comunicação entre a grande cavidade e a retrocavidade dos epíplons (bolsa omental). Clinicamente, é a via de acesso para a Manobra de Pringle (clampeamento do pedículo hepático para controle de hemorragia) e local potencial para hérnias internas.
3. Trato Digestório e Glândulas Anexas
Nesta região, os epônimos descrevem marcos críticos para ressecções oncológicas e reconstruções.
- Ângulo de His
- Anatomia: Ângulo agudo formado entre o esôfago abdominal e o fundo gástrico.
- Relevância Cirúrgica: Componente anatômico crucial do mecanismo valvular anti-refluxo. A restauração ou acentuação deste ângulo é o objetivo central das fundoplicaturas (Nissen, Toupet) no tratamento da DRGE.
- Espaço de Traube e Triângulo de Labbé
- Anatomia: Áreas de projeção gástrica na parede toracoabdominal.
- Relevância Cirúrgica: O Espaço de Traube (timpânico à percussão) torna-se maciço em casos de esplenomegalia ou derrame pleural. O Triângulo de Labbé é a área de contato do estômago com a parede abdominal anterior, local seguro para gastrostomias percutâneas ou cirúrgicas.
- Ligamento de Treitz
- Anatomia: Músculo suspensor do duodeno, marcando a transição duodeno-jejunal (ângulo de Treitz).
- Relevância Cirúrgica: Divisor anatômico e clínico entre hemorragia digestiva alta e baixa. Marco fundamental para a mobilização do intestino delgado e identificação da primeira alça jejunal em reconstruções (ex: Y de Roux).
- Vias Biliares: Calot, Heister, Vater, Oddi
- Triângulo de Calot (Cisto-Hepático): Delimitado pelo ducto cístico, ducto hepático comum e borda inferior do fígado. Contém a artéria cística e, frequentemente, o linfonodo de Mascagni. Sua dissecção meticulosa para obter a “Visão Crítica de Segurança” (Critical View of Safety) é mandatória para prevenir lesões iatrogênicas da via biliar principal na colecistectomia.
- Válvulas de Heister: Pregas espirais na mucosa do ducto cístico que podem dificultar a cateterização durante a colangiografia intraoperatória.
- Ampola de Vater e Esfíncter de Oddi: A confluência biliopancreática e seu aparelho esfincteriano. Alvo terapêutico nas papilotomias endoscópicas (CPRE) para tratamento de coledocolitíase ou pancreatite biliar.
- Ductos Pancreáticos (Wirsung e Santorini)
- Anatomia: Wirsung é o ducto principal; Santorini é o acessório.
- Relevância Cirúrgica: A variante Pancreas Divisum (falha na fusão dos ductos) drena a maior parte do pâncreas pelo ducto menor (Santorini), sendo causa de pancreatites recorrentes inexplicadas.
- Marcos Hepáticos (Glisson e Cantlie)
- Cápsula de Glisson: Bainha de tecido conjuntivo que envolve o fígado e a tríade portal intra-hepática. Importante na manobra de Pringle e nas hepatectomias.
- Linha de Cantlie: Linha imaginária que divide o fígado funcionalmente em lobos direito e esquerdo, estendendo-se do leito da vesícula biliar à veia cava inferior. Base para hepatectomias anatômicas maiores.
4. Vascularização Abdominal e Colateralização
O conhecimento das arcadas vasculares é determinante para a viabilidade de anastomoses intestinais.
- Tripus Halleri (Tronco Celíaco)
- Anatomia: Trifurcação da aorta abdominal em artéria gástrica esquerda, esplênica e hepática comum.
- Relevância Cirúrgica: O controle vascular proximal em cirurgias de trauma, gastrectomias e pancreatectomias. Variações anatômicas são frequentes e devem ser antecipadas em planejamentos pré-operatórios.
- Arcada de Riolan e Artéria Marginal de Drummond
- Anatomia: Sistemas de anastomose entre a artéria cólica média (ramo da mesentérica superior) e a cólica esquerda (ramo da mesentérica inferior).
- Relevância Cirúrgica: Garantem a irrigação do cólon, especialmente na flexura esplênica (ponto crítico de Griffiths). A preservação ou a integridade funcional destas arcadas é vital para evitar isquemia do coto colônico em retossigmoidectomias e cirurgias de aneurisma de aorta.
- Veias de Sappey e Retzius
- Anatomia: Veias acessórias do sistema porta. As de Sappey correm no ligamento falciforme; as de Retzius são anastomoses retroperitoneais.
- Relevância Cirúrgica: Em pacientes com hipertensão portal, estas veias dilatam-se dramaticamente. As veias de Sappey podem causar hemorragia maciça na incisão supraumbilical. A dissecção do retroperitônio em cirróticos pode encontrar o “sangramento em lençol” das veias de Retzius, de difícil controle.
5. Retroperitônio e Rins
A anatomia dos planos fasciais renais é a chave para a cirurgia oncológica retroperitoneal radical.
- Fáscia de Gerota (e suas lâminas Toldt e Zuckerkandl)
- Anatomia: A fáscia renal envolve o rim e a adrenal em um compartimento fechado. A lâmina anterior é frequentemente associada à Fáscia de Toldt (no contexto da fusão com o mesocólon), e a posterior à Fáscia de Zuckerkandl.
- Relevância Cirúrgica: A “Fáscia de Toldt” (ou linha de Toldt) representa o plano de clivagem avascular embrionário entre o mesocólon e o retroperitônio. A dissecção neste plano permite a mobilização incruenta do cólon direito e esquerdo, essencial em colectomias oncológicas laparoscópicas e abertas. A violação da Fáscia de Gerota propriamente dita é indicativa de invasão tumoral renal ou necessária para nefrectomias radicais.
Conclusão
O domínio dos epônimos da anatomia abdominal transcende o exercício de erudição histórica; constitui uma ferramenta de precisão técnica. Falar em “Triângulo de Calot” ou “Fáscia de Toldt” evoca, instantaneamente, uma estratégia cirúrgica e um plano de segurança. Para o cirurgião do aparelho digestivo, a fluência nesta linguagem clássica é tão fundamental quanto a destreza manual, permitindo a integração segura entre o conhecimento anatômico estático e a dinâmica do ato operatório.
Referência-Base: ten Donkelaar HJ, Quartu M, Kachlík D. An Illustrated Guide to Anatomical Eponyms. Springer, 2025.
Índice Biográfico dos Epônimos Citados
Abaixo listam-se os dados biográficos dos anatomistas e cirurgiões cujos epônimos foram discutidos neste artigo.
- Blumer, George (Reino Unido/EUA, 1858–1940)
- Calot, Jean-François (França, 1861–1944)
- Camper, Pieter (Holanda, 1722–1789)
- Cantlie, James (Escócia, 1851–1926)
- Colles, Abraham (Irlanda, 1773–1843)
- Cooper, Astley Paston (Reino Unido, 1768–1841)
- Douglas, James (Escócia, 1675–1742)
- Drummond, Hamilton (Reino Unido, 1882–1925)
- Fruchaud, Henri (França, 1894–1960)
- Gallaudet, Bern Budd (EUA, 1860–1934)
- Gerota, Dimitrie (Romênia, 1867–1939)
- Gimbernat, Antoni de (Espanha, 1734–1816)
- Glisson, Francis (Reino Unido, 1597–1677)
- Griffiths, Joseph (País de Gales, 1863–1945)
- Haller, Albrecht von (Suíça, 1708–1777)
- Heister, Lorenz (Alemanha, 1683–1758)
- Hesselbach, Franz Kaspar (Alemanha, 1759–1816)
- His, Wilhelm Jr. (Suíça, 1863–1934)
- Labbé, Léon (França, 1832–1916)
- Lanz, Otto (Suíça, 1865–1935)
- Mascagni, Paolo (Itália, 1755–1815)
- McBurney, Charles (EUA, 1845–1913)
- Monro, Alexander III (Escócia, 1773–1859)
- Morison, James Rutherford (Reino Unido, 1853–1939)
- Murphy, John Benjamin (EUA, 1857–1916)
- Oddi, Ruggero (Itália, 1864–1913)
- Poupart, François (França, 1661–1709)
- Pringle, James Hogarth (Escócia, 1863–1941)
- Proust, Robert (França, 1873–1935)
- Retzius, Anders (Suécia, 1796–1860)
- Richter, August Gottlieb (Alemanha, 1742–1812)
- Riolan, Jean (o Jovem) (França, 1580–1657)
- Santorini, Giovanni Domenico (Itália, 1681–1737)
- Sappey, Marie Philibert Constant (França, 1810–1896)
- Scarpa, Antonio (Itália, 1752–1832)
- Toldt, Carl (Áustria, 1840–1920)
- Traube, Ludwig (Alemanha, 1818–1876)
- Treitz, Václav (República Tcheca/Áustria, 1819–1872)
- Vater, Abraham (Alemanha, 1684–1751)
- Winslow, Jacob Benignus (Dinamarca/França, 1669–1760)
- Wirsung, Johann Georg (Alemanha, 1589–1643)
- Zuckerkandl, Emil (Áustria, 1849–1910)
Lifelong Learning na Cirurgia: como a Aprendizagem Autorregulada Define o Cirurgião que Você Vai Ser
Introdução
A cirurgia é uma das áreas da medicina que mais muda ao longo do tempo. Técnicas, tecnologias, diretrizes e condutas são revisadas continuamente. Ninguém termina a residência “pronto para tudo”. O que diferencia o cirurgião que se mantém competente e atualizado ao longo da carreira não é apenas o que aprendeu na formação inicial, mas a capacidade de continuar aprendendo de forma ativa, intencional e estruturada.
Esse é o núcleo do conceito de Lifelong Learning: o compromisso de adquirir, revisar e integrar novos conhecimentos desde o primeiro dia de faculdade até o último dia de atividade profissional. E, na prática, o que sustenta isso é um conjunto de habilidades chamado aprendizagem autorregulada.
O problema: bons alunos, maus aprendizes
Grande parte dos estudantes que chegam à residência é formada por “altos desempenhos acadêmicos”. Mas muitos:
- atribuem sucesso e fracasso quase sempre ao professor, ao serviço ou ao tipo de prova;
- não conseguem descrever com clareza como estudam;
- acreditam que aprender é algo que “acontece com eles”, não algo que podem controlar.
Esse modelo funciona em um ambiente escolar tradicional, com provas previsíveis e conteúdo delimitado. Em cirurgia, não. No centro cirúrgico, na UTI ou no pronto-socorro, o cirurgião depende de outra coisa: da capacidade de identificar o que não sabe, de estudar com foco e de ajustar a própria prática a partir de resultados reais.
É aqui que entra a aprendizagem autorregulada.
O que é aprendizagem autorregulada?
Aprendizagem autorregulada é o conjunto de hábitos, estratégias e atitudes que fazem o aluno assumir o controle do próprio processo de aprendizagem.
Um aprendiz autorregulado:
- pensa sobre como aprende (metacognição);
- acredita que é capaz de melhorar com esforço e estratégia (autoeficácia realista);
- organiza o ambiente, o tempo e os recursos para aprender melhor (comportamento ativo).
Na prática, isso aparece em três dimensões:
1. Metacognitiva
- Define objetivos de aprendizado (“quero entender critérios de indicação de neoadjuvância no pâncreas”, “quero melhorar decisão em vesícula difícil”).
- Planeja como chegar lá (o que ler, que casos observar, que vídeos rever).
- Monitora se está, de fato, avançando.
- Se autoavalia com honestidade ao final.
2. Motivacional
- Liga esforço a desempenho.
- Não se vê como “bom” ou “ruim”, mas como alguém em processo de desenvolvimento.
- Usa erros como feedback, não como sentença.
3. Comportamental
- Seleciona ativamente casos, plantões e oportunidades que trazem aprendizado.
- Busca ajuda, feedback e coaching quando necessário.
- Usa estratégias de estudo estruturadas, não apenas leitura passiva.
O ciclo da aprendizagem autorregulada
Você pode enxergar esse processo como um ciclo contínuo:
- Planejamento (forethought)
- O que quero aprender?
- Por que isso é importante agora?
- Quanto tempo vou dedicar? Com que materiais?
- Execução (performance)
- Implementar o plano (leitura, vídeo, simulação, prática supervisionada).
- Monitorar em tempo real: estou entendendo? estou apenas decorando? estou aplicando?
- Reflexão (self-reflection)
- O que funcionou? O que não funcionou?
- O problema foi falta de esforço, estratégia inadequada, falta de recurso ou algo fora do meu controle?
- O que vou manter, o que vou mudar no próximo ciclo?
Quem atribui tudo a “azar”, “caso difícil”, “erro do serviço” sai mais fraco do caso.
Quem atribui a fatores ajustáveis (estratégia, preparação, decisão) sai mais forte, mesmo depois de um erro.
Ferramentas práticas para residentes e cirurgiões
1. Autoavaliação de como você aprende
Não é apenas “sou bom ou ruim”, mas:
- eu planejo o que estudar ou vou “apagando incêndio”?
- eu mudo de estratégia quando não entendo um tema?
- eu reviso os casos difíceis depois do plantão?
- eu procuro ativamente feedback objetivo sobre minha performance?
Transformar isso em rotina escrita (um caderno, um app, uma planilha) ajuda a tirar a aprendizagem do improviso e colocá-la em modo profissional.
2. Coaching cirúrgico
Coaching não é “mais uma aula”; é uma conversa estruturada para:
- definir objetivos de melhoria claros (ex.: decisão de conversão; planejamento de colecistectomia difícil; comunicação com a equipe);
- identificar pontos cegos (o que você não está vendo sobre a própria prática);
- desenhar um plano concreto de treinamento e estudo.
Ferramentas de vídeo-coaching (assistir a uma operação sua com um colega experiente e revisar decisões, tempos e manobras) têm efeito duplo: refinam a técnica e amplificam a sua metacognição.
3. Leitura inteligente: saindo do “sublinhar tudo”
Um exemplo prático é a estratégia SQ3R para capítulos e diretrizes:
- Survey (percurso) – passar rapidamente pelos subtítulos, tabelas, figuras.
- Question (perguntas) – transformar subtítulos em perguntas (“quando indicar intervalo apendicectomia?”, “como manejar abscesso apendicular?”).
- Read (leitura) – ler com foco em responder suas próprias perguntas.
- Recall (recordar) – fechar o texto e anotar o que lembra de cabeça.
- Review (revisar) – conferir no texto e corrigir lacunas.
É mais trabalhoso do que reler passivamente, mas a retenção é muito maior — e é isso que interessa na prática cirúrgica.
Aplicando isso na formação cirúrgica
Na rotina de um serviço de cirurgia, aprendizagem autorregulada se traduz em ações muito concretas:
- Antes do plantão: definir 1–2 objetivos de aprendizado (por exemplo, “revisar escore de Alvarado e conduta em apendicite complicada”).
- Durante o plantão: escolher conscientemente 1–2 casos para estudar em profundidade depois.
- Após a cirurgia: registrar rapidamente:
- o que foi bem,
- o que não foi,
- o que você precisa estudar para a próxima situação semelhante.
No nível do serviço, vale estimular:
- discussão de M&M com foco em análise de processo, não apenas em “culpa”;
- preceptores que verbalizam seu raciocínio e seus próprios erros;
- metas claras por ano de residência (o que se espera que o R1, R2, R3 saiba de fato).
Pontos-chave para o cirurgião que quer ser lifelong learner
- Assuma o comando do próprio aprendizado – ninguém fará isso por você.
- Planeje o estudo como planeja uma cirurgia – com objetivo, estratégia e checagem.
- Use erro e desconforto como combustível, não como fonte de paralisia.
- Busque feedback específico, não elogios genéricos.
- Padronize suas estratégias de leitura e revisão, fuja do improviso.
Conclusão
Formar um cirurgião tecnicamente competente é obrigatório.
Formar um cirurgião capaz de continuar aprendendo, se adaptando e se avaliando ao longo da vida é o verdadeiro diferencial.
Lifelong learning não é um slogan bonito de documento institucional.
É uma competência prática, treinável, que começa na residência, mas precisa acompanhar cada decisão, cada leitura, cada caso difícil.
Quanto mais cedo você organizar o próprio processo de aprender, mais preparado estará para os desafios que ainda nem existem hoje – mas que certamente farão parte da cirurgia de amanhã.
Hashtags (SEO)
#LifelongLearningEmCirurgia #AprendizagemAutorregulada #FormaçãoDoCirurgião #EducaçãoMédicaContinuada #ResidênciaEmCirurgia
Gostou❔ Deixe seu comentário ✍️, compartilhe com seus colegas e mande sua dúvida pelo 💬 Chat On-line em nossa DM no Instagram.










